前四周期元素X、Y、Z、W核电荷数依次增加,核电荷数之和为58;Y 原子的M层p轨道有3个未成对电子;Z与Y同周期,且在该周期中电负性最大;W原子的L层电子数与最外层电子数之比为4:1,其d轨道中的电子数与最外层电子数之比为5:2。
(1)X的元素符号为_________ ,Z元素位于周期表_______ 周期_______ 族。
(2)Y和Z各自形成的简单气态氢化物中,热稳定性较强的是_______ (写分子式)。
(3)Z和Y各自形成的最高价氧化物对应的水化物中,酸性较强的是_________ (写分子式)。
(4)12.4 g单质Y4与0.3 mol O2在一定条件下恰好完全反应生成0.1 mol化合物C,每mol C分子中所含有的σ键数目为_________ mol。
(5)W形成的最高价含氧酸根离子的化学式为_________ ,写出它在酸性条件下与Fe2+反应的离子方程式_________ 。
(1)X的元素符号为
(2)Y和Z各自形成的简单气态氢化物中,热稳定性较强的是
(3)Z和Y各自形成的最高价氧化物对应的水化物中,酸性较强的是
(4)12.4 g单质Y4与0.3 mol O2在一定条件下恰好完全反应生成0.1 mol化合物C,每mol C分子中所含有的σ键数目为
(5)W形成的最高价含氧酸根离子的化学式为
更新时间:2016-12-09 00:09:32
|
【知识点】 元素周期表 元素周期律
相似题推荐
填空题
|
较难
(0.4)
【推荐1】【物质结构与性质】2014 年10 月7 日,赤崎勇、天野浩和中村修二因发明“高亮度蓝色发光二极管(LED)”获得2014 年诺贝尔物理学奖。制作LED 首先在衬底上制作氮化镓(GaN)基的外延片,常用的衬底主要有蓝宝石(Al2O3)、碳化硅和硅,还有砷化镓(GaAs)、AlN、ZnO 等材料。回答下列问题:
(1)氮和砷(As)位于同一主族,二者中电负性较大的是____________ (填元素符号,下同),第一电离能较大的是________________ 。
(2)基态Zn 原子的价电子排布式为______________ ,价层电子占有的原子轨道数为_________________ 。
(3)Al2O3的熔点很高,Al2O3属于______________ 晶体。Al2O3的熔点比NaCl 高,其原因是__________ 。
(4)碳化硅的晶胞结构如图所示,其中白球代表的是__________________ 原子,一个晶胞中含有该原子的个数为_____________________ 。

(1)氮和砷(As)位于同一主族,二者中电负性较大的是
(2)基态Zn 原子的价电子排布式为
(3)Al2O3的熔点很高,Al2O3属于
(4)碳化硅的晶胞结构如图所示,其中白球代表的是

您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】现有部分短周期元素的原子结构如下表:
(1)写出X的元素符号:________ ,元素Y的最简单氢化物的化学式为_________ 。
(2)Z元素原子的质量数为_______ 。
(3)X和Z两种元素的最高价氧化物对应的水化物相互反应的离子方程式为______________________
| 元素符号 | 元素原子结构 |
| X | 原子结构示意图为 |
| Y | 最外层电子数是次外层电子数的2倍 |
| Z | 原子核内含有12个中子,且其离子的结构示意图为 |
(1)写出X的元素符号:
(2)Z元素原子的质量数为
(3)X和Z两种元素的最高价氧化物对应的水化物相互反应的离子方程式为
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐3】下表列出了A~M 13种元素在周期表中的位置:
(1)这些元素中,金属性最强的元素是_______ (填元素符号,下同),非金属性最强的是_______ 。
(2)写出H元素的最高价氧化物与F元素最高价氧化物对应水化物反应的离子方程式_______ 。
(3)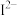 、
、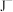 、
、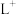 、
、 等微粒中,半径最大的是
等微粒中,半径最大的是_______ ,最小的是_______ 。
(4)A与D形成的化合物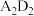 是
是_______ 化合物,其电子式为_______ 。
| 1 | A | |||||||
| 2 | B | C | D | E | ||||
| 3 | F | G | H | I | J | K | ||
| 4 | L | M |
(2)写出H元素的最高价氧化物与F元素最高价氧化物对应水化物反应的离子方程式
(3)
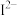 、
、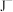 、
、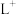 、
、 等微粒中,半径最大的是
等微粒中,半径最大的是(4)A与D形成的化合物
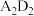 是
是
您最近一年使用:0次



