【化学—选修3:物质结构与性质】金属铝、铁、铜与人类生产、生活息息相关。
(1)基态铝原子核外处在能量最高的能级上的电子共有______ 种不同的运动状态,工业电解熔融氧化铝时要添加助熔剂Na3[AlF6]。由氟化钠和硫酸铝可以制取Na3[AlF6],反应的化学方程式为____________ 。
(2)聚合硫酸铁(简称PFS)的化学式为[Fe(OH)n(SO4)(3—n)/2]m,是常用的水处理剂,与PFS中铁元素价态相同的铁离子的电子排布式为__________________ ,SO42-的空间构型是_____________ 。
(3)下列关于[Cu(NH3)4]SO4、K4[Fe(CN)6]、Na3[AlF6]的说法中正确的有_____ (填字母)。
a.三种物质中含有的化学键类型均有离子键和配位键
b.三种物质的组成元素中电负性最大与最小的两种非金属元素形成的晶体属于离子晶体
c.三种物质的组成元素中第一电离能最大的是氮元素
d.K4[Fe(CN)6]与Na3[AlF6]的中心离子具有相同的配位数
(4)某种含Cu2+的化合物可催化氧化丙烯醇(HOCH2CH=CH2)制备丙醛(CH3CH2CHO),在丙烯醇分子中共有____ 个σ键,其中碳原子的杂化方式是_________________ 。
(5)用晶体的X射线衍射法可以测得阿伏加德罗常数的值。对金属铜的测定得到以下结果:铜晶胞为面心立方最密堆积,边长为361 pm。又知铜的密度为9.0 g/cm3,则铜原子的直径约为________ pm,阿伏加德罗常数的值为_______ 。
(1)基态铝原子核外处在能量最高的能级上的电子共有
(2)聚合硫酸铁(简称PFS)的化学式为[Fe(OH)n(SO4)(3—n)/2]m,是常用的水处理剂,与PFS中铁元素价态相同的铁离子的电子排布式为
(3)下列关于[Cu(NH3)4]SO4、K4[Fe(CN)6]、Na3[AlF6]的说法中正确的有
a.三种物质中含有的化学键类型均有离子键和配位键
b.三种物质的组成元素中电负性最大与最小的两种非金属元素形成的晶体属于离子晶体
c.三种物质的组成元素中第一电离能最大的是氮元素
d.K4[Fe(CN)6]与Na3[AlF6]的中心离子具有相同的配位数
(4)某种含Cu2+的化合物可催化氧化丙烯醇(HOCH2CH=CH2)制备丙醛(CH3CH2CHO),在丙烯醇分子中共有
(5)用晶体的X射线衍射法可以测得阿伏加德罗常数的值。对金属铜的测定得到以下结果:铜晶胞为面心立方最密堆积,边长为361 pm。又知铜的密度为9.0 g/cm3,则铜原子的直径约为
更新时间:2016-12-09 08:17:16
|
【知识点】 物质结构与性质
相似题推荐
填空题
|
较难
(0.4)
解题方法
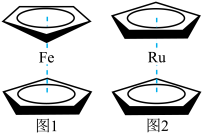
【推荐1】自从1951年发现的第一个金属茂配合物二茂铁 (如图1所示)后,研究者对三明治式配合物的兴趣迅速增长。图2是某研究人员得到的Ru的二茂合物。
(如图1所示)后,研究者对三明治式配合物的兴趣迅速增长。图2是某研究人员得到的Ru的二茂合物。
(1)该二茂Ru可在氮气保护下,在95%的乙醇溶液中,用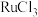 、Zn粉和环戊二烯反应获得,下列方程式能表示该反应的是
、Zn粉和环戊二烯反应获得,下列方程式能表示该反应的是
(2)推断该二茂Ru的核磁共振氢谱
(3)该二茂Ru是一种重叠夹心型结构,不同于二茂铁具有交错型结构的原因
 (如图1所示)后,研究者对三明治式配合物的兴趣迅速增长。图2是某研究人员得到的Ru的二茂合物。
(如图1所示)后,研究者对三明治式配合物的兴趣迅速增长。图2是某研究人员得到的Ru的二茂合物。
(1)该二茂Ru可在氮气保护下,在95%的乙醇溶液中,用
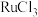 、Zn粉和环戊二烯反应获得,下列方程式能表示该反应的是
、Zn粉和环戊二烯反应获得,下列方程式能表示该反应的是 A.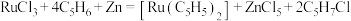 |
B.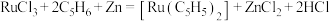 |
C.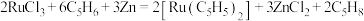 |
D.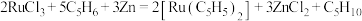 |
| A.出现一种信号 | B.出现2种信号 | C.出现3种信号 | D.出现4种信号 |
| A.由于Ru离子的价电子数与铁离子不同,导致环戊二烯环的立体作用增大 |
| B.由于Ru离子的价电子数与铁离子不同,导致环戊二烯环的立体作用减少 |
| C.由于钌的离子半径较大,导致环戊二烯环的立体作用增大 |
| D.由于钌的离子半径较大,导致环戊二烯环的立体作用减少 |
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】(4-5必做)根据已学知识,请你回答下列问题:
(1)最外层电子排布为4s24p1的原子的核电荷数为__________ 。某元素被科学家称之为人体微量元素中的“防癌之王”,其原子的外围电子排布是4s24p4,该元素的名称是_________ 。
(2)根据VSEPR模型,PO43-的分子立体结构为:________ ;乙醇易溶于水的原因是__________ ;HClO4的酸性强于HClO的原因是________ ;
(3)三氯化铁常温下为固体,熔点282°C,沸点315°,在300°C以上易升华。易溶于水,也易溶于乙醚、丙酮等有机溶剂。据此判断三氯化铁晶体为________ 。
(4)某元素核外有三个电子层,最外层电子数是核外电子总数的1/6,写出该元素原子的电子排布式是_____ 。写出铬元素在周期表中的位置________ ,它位于______ 区。
(5)如图是氯化铯晶体的晶胞示意图(晶体中最小的重复结构单元),已知晶体中2个最近的Cs+核间距为a pm,氯化铯(CsCl)的相对分子质量M,NA为阿伏加德罗常数,则氯化铯晶体的密度为______ g/cm3。

(1)最外层电子排布为4s24p1的原子的核电荷数为
(2)根据VSEPR模型,PO43-的分子立体结构为:
(3)三氯化铁常温下为固体,熔点282°C,沸点315°,在300°C以上易升华。易溶于水,也易溶于乙醚、丙酮等有机溶剂。据此判断三氯化铁晶体为
(4)某元素核外有三个电子层,最外层电子数是核外电子总数的1/6,写出该元素原子的电子排布式是
(5)如图是氯化铯晶体的晶胞示意图(晶体中最小的重复结构单元),已知晶体中2个最近的Cs+核间距为a pm,氯化铯(CsCl)的相对分子质量M,NA为阿伏加德罗常数,则氯化铯晶体的密度为

您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐3】已知Al、Mg、Na为第三周期元素,其原子的第一至第四电离能如下表:
(1)则Al、Mg、Na的电负性从大到小的顺序为_____________ 。
(2) C、N、O、H是周期表中前10号元素,它们的原子半径依次减小,H能分别与C、N、O形成电子总数相等的分子CH4、NH3、H2O。
①在CH4、NH3、H2O分子中,C、N、O三原子都采取_______ 杂化;
②CH4是含有_____ 键(填“极性”或“非极性”)的____ 分子(填“极性”或“非极性”);
③NH3是一种易液化的气体,请简述其易液化的原因_______ 。
④H2O分子的VSEPR模型的空间构型为_____ ;H2O分子的空间构型为______ 。
(3) K、Cr、 Cu三元素的原子序数依次增大,三原子的核外的最外层电子排布均为4s1。
①K元素组成的单质的晶体堆积模型为______ (填代号);
a.简单立方堆积 b.体心立方堆积 c.六方最密堆积 d.面心立方最密堆积
②Cr元素在其化合物中最高化合价为_____ ;
③Cu2+离子的核外电子排布式为______ ;
| 电离能/kJ‧mol-1 | I1 | I2 | I3 | I4 |
| X | 578 | 1817 | 2745 | 11578 |
| Y | 738 | 1451 | 7733 | 10540 |
| Z | 496 | 4562 | 6912 | 9543 |
(1)则Al、Mg、Na的电负性从大到小的顺序为
(2) C、N、O、H是周期表中前10号元素,它们的原子半径依次减小,H能分别与C、N、O形成电子总数相等的分子CH4、NH3、H2O。
①在CH4、NH3、H2O分子中,C、N、O三原子都采取
②CH4是含有
③NH3是一种易液化的气体,请简述其易液化的原因
④H2O分子的VSEPR模型的空间构型为
(3) K、Cr、 Cu三元素的原子序数依次增大,三原子的核外的最外层电子排布均为4s1。
①K元素组成的单质的晶体堆积模型为
a.简单立方堆积 b.体心立方堆积 c.六方最密堆积 d.面心立方最密堆积
②Cr元素在其化合物中最高化合价为
③Cu2+离子的核外电子排布式为
您最近一年使用:0次



