(1)铜器表面有时会生成铜绿[Cu2(OH)2CO3],这层铜绿可用化学方法除去。试写出除去铜绿而不损伤器物的化学方程式 _________________________ 。
(2)工业上常用铝热反应产生的“铁水”来焊接铁轨,请写出铝热反应的化学方程式_________ 。
(3)冶金工业中,常用焦炭来冶炼铁。写出赤铁矿(Fe2O3)被CO还原成铁的化学方程式_____ 。
(2)工业上常用铝热反应产生的“铁水”来焊接铁轨,请写出铝热反应的化学方程式
(3)冶金工业中,常用焦炭来冶炼铁。写出赤铁矿(Fe2O3)被CO还原成铁的化学方程式
更新时间:2016-12-09 00:18:40
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】已知有关物质的熔、沸点数据如下表:
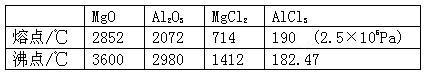
请参考上述数据回答下列问题:
(1)工业上常用电解熔融MgCl2的方法生产金属镁,电解Al2O3与冰晶石熔融混合物的方法生产铝。为什么不用电解MgO的方法生产镁;也不用电解AlCl3的方法生产铝?
答___________ 。
(2)设计可靠的实验证明MgCl2、AlCl3所属的晶体类型,其实验方法是__ _____。

请参考上述数据回答下列问题:
(1)工业上常用电解熔融MgCl2的方法生产金属镁,电解Al2O3与冰晶石熔融混合物的方法生产铝。为什么不用电解MgO的方法生产镁;也不用电解AlCl3的方法生产铝?
答___________ 。
(2)设计可靠的实验证明MgCl2、AlCl3所属的晶体类型,其实验方法是__ _____。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)铝热反应可用于定向爆破,写出铝和四氧化三铁反应的化学方程式___________________ ;
(2)利用金属活泼性的不同,可采用不同的冶炼方法,写出工业制铝的化学方程式___________________ 。
(2)利用金属活泼性的不同,可采用不同的冶炼方法,写出工业制铝的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】铜是生命必需的元素,也是人类最早使用的金属之一,铜的生产和使用对国计民生各个方面产生了深远的影响,请回答下列问题:
(1)西汉古籍中曾有记载:曾青(硫酸铜)得铁则化为铜。
该反应的化学方程式是____________________ ;
该反应的离子方程式是______________________ 。
(2)铜器表面有时会生成铜绿,其化学式为Cu2(OH)2CO3。
请写出生成铜绿的化学方程式:______________ ;铜绿可用化学方法除去,请写出除去铜绿而不损伤器物的化学方程式:_________ 。铜制品的保护方法是___________ 。
(3)铜钱在历史上曾经是一种广泛流通的货币。试从物理性质和化学性质的角度分析铜常用于制造货币的原因(已知铜的熔点是1183.4 ,铁的熔点是1534.8 ):_________________ 。
(1)西汉古籍中曾有记载:曾青(硫酸铜)得铁则化为铜。
该反应的化学方程式是
该反应的离子方程式是
(2)铜器表面有时会生成铜绿,其化学式为Cu2(OH)2CO3。
请写出生成铜绿的化学方程式:
(3)铜钱在历史上曾经是一种广泛流通的货币。试从物理性质和化学性质的角度分析铜常用于制造货币的原因(已知铜的熔点是1183.4 ,铁的熔点是1534.8 ):
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】古代青铜器的修复主旨是“修旧如旧”。
(1)铜锈为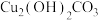 ,俗称铜绿,可溶于酸。铜绿在一定程度上可以提升青铜器的艺术价值,推测参与形成铜绿的物质有Cu和
,俗称铜绿,可溶于酸。铜绿在一定程度上可以提升青铜器的艺术价值,推测参与形成铜绿的物质有Cu和_______ 。
(2)铜锈的成分非常复杂,主要成分有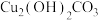 和
和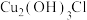 ,考古学家将铜锈分为无害锈和有害锈,结构如图所示:
,考古学家将铜锈分为无害锈和有害锈,结构如图所示:

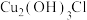 属于
属于_______ (填“无害”或“有害”锈,请解释原因:_______ 。
(3)青铜器的修复方法之——碳酸钠法:将腐蚀文物置于含 的缓冲溶液中浸泡,使CuCl(白色不溶于水的固体)转化为难溶的
的缓冲溶液中浸泡,使CuCl(白色不溶于水的固体)转化为难溶的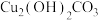 。写出碳酸钠法的离子方程式:
。写出碳酸钠法的离子方程式:_______ 。
(1)铜锈为
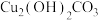 ,俗称铜绿,可溶于酸。铜绿在一定程度上可以提升青铜器的艺术价值,推测参与形成铜绿的物质有Cu和
,俗称铜绿,可溶于酸。铜绿在一定程度上可以提升青铜器的艺术价值,推测参与形成铜绿的物质有Cu和(2)铜锈的成分非常复杂,主要成分有
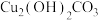 和
和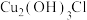 ,考古学家将铜锈分为无害锈和有害锈,结构如图所示:
,考古学家将铜锈分为无害锈和有害锈,结构如图所示:
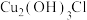 属于
属于(3)青铜器的修复方法之——碳酸钠法:将腐蚀文物置于含
 的缓冲溶液中浸泡,使CuCl(白色不溶于水的固体)转化为难溶的
的缓冲溶液中浸泡,使CuCl(白色不溶于水的固体)转化为难溶的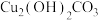 。写出碳酸钠法的离子方程式:
。写出碳酸钠法的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】回答下列问题
(1)标准状况下,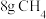 与
与___________ L的 气体含有相同的氢原子数。
气体含有相同的氢原子数。
(2)某气体氧化物的化学式为 ,在标准状况下,
,在标准状况下, 该氧化物的体积为
该氧化物的体积为 ,则该氧化物的摩尔质量为
,则该氧化物的摩尔质量为___________ 。
(3)在一定的温度和压强下,1体积气体 与3体积气体
与3体积气体 化合生成2体积气体化合物,则该化合物的化学式是
化合生成2体积气体化合物,则该化合物的化学式是___________ (用X、Y表示)。
(4)在150℃加热高氯酸铵发生分解反应;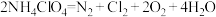 ,在150℃时其气态生成物组成的混合气的平均相对分子质量为
,在150℃时其气态生成物组成的混合气的平均相对分子质量为___________ (保留1位小数)。
(5)配制250mL0.1mol/L的 溶液,需5mol/LHAc溶液的体积为
溶液,需5mol/LHAc溶液的体积为___________ mL。
(6)下列关于 容量瓶的操作,正确的是___________。
容量瓶的操作,正确的是___________。
(7)古代青铜器的修复主旨是“修旧如旧”。
①铜锈为 ,俗称铜绿,可溶于酸。铜绿在一定程度上可以提升青铜器的艺术价值,推测参与形成铜绿的物质有Cu和
,俗称铜绿,可溶于酸。铜绿在一定程度上可以提升青铜器的艺术价值,推测参与形成铜绿的物质有Cu和___________ 。
②铜锈的成分非常复杂,主要成分有 和
和 ,考古学家将铜锈分为无害锈和有害锈,结构如图所示:
,考古学家将铜锈分为无害锈和有害锈,结构如图所示:

 属于
属于___________ (填“无害”或“有害”)锈,请解释原因:___________ 。
(1)标准状况下,
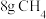 与
与 气体含有相同的氢原子数。
气体含有相同的氢原子数。(2)某气体氧化物的化学式为
 ,在标准状况下,
,在标准状况下, 该氧化物的体积为
该氧化物的体积为 ,则该氧化物的摩尔质量为
,则该氧化物的摩尔质量为(3)在一定的温度和压强下,1体积气体
 与3体积气体
与3体积气体 化合生成2体积气体化合物,则该化合物的化学式是
化合生成2体积气体化合物,则该化合物的化学式是(4)在150℃加热高氯酸铵发生分解反应;
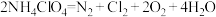 ,在150℃时其气态生成物组成的混合气的平均相对分子质量为
,在150℃时其气态生成物组成的混合气的平均相对分子质量为(5)配制250mL0.1mol/L的
 溶液,需5mol/LHAc溶液的体积为
溶液,需5mol/LHAc溶液的体积为(6)下列关于
 容量瓶的操作,正确的是___________。
容量瓶的操作,正确的是___________。A.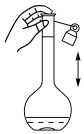 | B.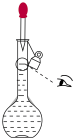 | C.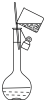 | D.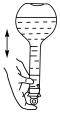 |
①铜锈为
 ,俗称铜绿,可溶于酸。铜绿在一定程度上可以提升青铜器的艺术价值,推测参与形成铜绿的物质有Cu和
,俗称铜绿,可溶于酸。铜绿在一定程度上可以提升青铜器的艺术价值,推测参与形成铜绿的物质有Cu和②铜锈的成分非常复杂,主要成分有
 和
和 ,考古学家将铜锈分为无害锈和有害锈,结构如图所示:
,考古学家将铜锈分为无害锈和有害锈,结构如图所示:
 属于
属于
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】海洋是巨大的化学资源宝库。把海水淡化和化工生产结合起来,可以得到淡水资源和钠、镁及氯气等工业产品。回答下列问题:
(1)海水淡化的方法主要有蒸馏法、电渗析法和___________ 。
(2)从海水制备精盐和金属锤的流程如下图所示:


①用电解法制取金属镁时,需要无水氯化镁。若直接加热 ·
· ,会发生非氧化还原反应,镁全部以
,会发生非氧化还原反应,镁全部以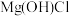 的形式存在,写出该反应的化学方程式:
的形式存在,写出该反应的化学方程式:___________ 。
②提取镁的过程中,将海水中的 转变为
转变为 ,再转变为
,再转变为 ,其目的是
,其目的是___________ 。
③与工业制镁类似,常用电解熔融 制钙(Sr)单质,写出制单质锶的化学方程式:
制钙(Sr)单质,写出制单质锶的化学方程式:___________ 。
(3)有人提出了一种综合氯碱工业循环治理含二氧化硫废气并回收二氧化硫的方法,该方法的流程如下:
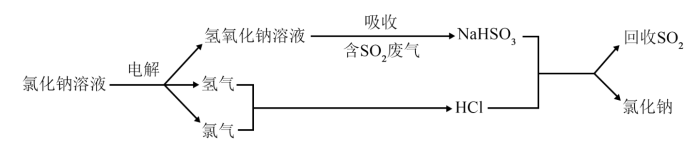
①写出氢氧化钠溶液吸收 生成
生成 反应的离子方程式:
反应的离子方程式:___________ ;
②该流程中可循环使用的物质是___________ 。
(1)海水淡化的方法主要有蒸馏法、电渗析法和
(2)从海水制备精盐和金属锤的流程如下图所示:


①用电解法制取金属镁时,需要无水氯化镁。若直接加热
 ·
· ,会发生非氧化还原反应,镁全部以
,会发生非氧化还原反应,镁全部以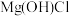 的形式存在,写出该反应的化学方程式:
的形式存在,写出该反应的化学方程式:②提取镁的过程中,将海水中的
 转变为
转变为 ,再转变为
,再转变为 ,其目的是
,其目的是③与工业制镁类似,常用电解熔融
 制钙(Sr)单质,写出制单质锶的化学方程式:
制钙(Sr)单质,写出制单质锶的化学方程式:(3)有人提出了一种综合氯碱工业循环治理含二氧化硫废气并回收二氧化硫的方法,该方法的流程如下:

①写出氢氧化钠溶液吸收
 生成
生成 反应的离子方程式:
反应的离子方程式:②该流程中可循环使用的物质是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】锰及其化合物主要用于锰矿的开采、锰铁冶炼、化肥和医药等领域。
(1)早期冶炼金属Mn的一种方法是先煅烧软锰矿(主要成分为MnO2)生成Mn3O4,再利用铝热反应制备金属Mn,该铝热反应的化学方程式为___ 。
(2)工业上通常采用软锰矿与KOH固体在空气中共热生成K2MnO4,再通入CO2的方法制备KMnO4。
各物质的溶解度如表所示:
①K2MnO4与CO2的反应中氧化产物和还原产物的比值为___ 。
②该制备过程需控制通入CO2的量,若CO2过量,还会生成物质A___ (填化学式)。
③从KMnO4和K2CO3混合溶液中分离提纯出KMnO4晶体的步骤为蒸发浓缩、___ 、过滤、洗涤、干燥;物质A的生成会使KMnO4的纯度降低,原因是__ 。
(1)早期冶炼金属Mn的一种方法是先煅烧软锰矿(主要成分为MnO2)生成Mn3O4,再利用铝热反应制备金属Mn,该铝热反应的化学方程式为
(2)工业上通常采用软锰矿与KOH固体在空气中共热生成K2MnO4,再通入CO2的方法制备KMnO4。
各物质的溶解度如表所示:
| 温度/℃ 物质 | 0 | 10 | 20 | 30 | 40 | 60 | 80 | 100 |
| KMnO4 | 2.83 | 4.31 | 6.34 | 9.03 | 12.6 | 22.1 | 41.1 | 50.5 |
| K2CO3 | 105 | 109 | 111 | 114 | 117 | 127 | 140 | 156 |
| A | 22.5 | 27.4 | 33.7 | 39.9 | 47.5 | 65.5 | — | — |
②该制备过程需控制通入CO2的量,若CO2过量,还会生成物质A
③从KMnO4和K2CO3混合溶液中分离提纯出KMnO4晶体的步骤为蒸发浓缩、
您最近一年使用:0次

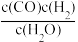 ,写出该反应的化学方程式
,写出该反应的化学方程式

