下图是Na、Cu、Si、H、C、N等元素单质的熔点高低的顺序,其中c、d均是热和电的良导体。

(1)请写出上图中d单质对应元素原子的电子排布式_______ 。
(2)单质a、b、f对应的元素以原子个数比1:1:1形成的分子中含____ σ键,_____ π键。
(3)a与b的元素形成的10电子中性分子X的空间构型为_____ ;将X溶于水后的溶液滴入到含d元素高价离子的溶液中至过量,生成的含d元素离子的化学式为_____ ,其中X与d的高价离子之间以____ 键组合。

(1)请写出上图中d单质对应元素原子的电子排布式
(2)单质a、b、f对应的元素以原子个数比1:1:1形成的分子中含
(3)a与b的元素形成的10电子中性分子X的空间构型为
更新时间:2016-12-09 00:24:41
|
【知识点】 晶体结构与性质
相似题推荐
填空题
|
适中
(0.65)
【推荐1】铁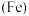 、钴
、钴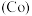 、镍
、镍 是第四周期第Ⅷ族的元素,其单质具有磁性,其化合物常用于制备电池导体.
是第四周期第Ⅷ族的元素,其单质具有磁性,其化合物常用于制备电池导体.
(1)基态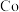 原子的核外电子排布式为
原子的核外电子排布式为
_____________ ,第二周期中基态原子与基态 原子具有相同未成对电子数的元素是
原子具有相同未成对电子数的元素是______________ .
(2) 、
、 、
、 原子半径相似、化学性质相似,原因是
原子半径相似、化学性质相似,原因是_______________ .
(3)配合物 的中心原子价电子数与配体提供电子总数之和为
的中心原子价电子数与配体提供电子总数之和为_________ . 与
与 互为等电子体,
互为等电子体, 分子具有的化学键类型有
分子具有的化学键类型有____________ .
A. 键 B.
键 B. 键 C.离子键 D.金属键
键 C.离子键 D.金属键
(4) 的结构与相关性质见下表,其空间构型为
的结构与相关性质见下表,其空间构型为______________ , 的杂化形式为
的杂化形式为_________ ,其为_____________ 晶体.
(5)钙钛矿中含有 、
、 、O,它们形成的氧化物具有金属-绝缘体相转变特性,其晶胞结构中
、O,它们形成的氧化物具有金属-绝缘体相转变特性,其晶胞结构中 和O如下图所示,
和O如下图所示, 位于O形成正八面体空隙中.晶胞边长为
位于O形成正八面体空隙中.晶胞边长为 ,设
,设 为阿伏加 德罗常数的数值,则该氧化物的密度为
为阿伏加 德罗常数的数值,则该氧化物的密度为________________  (列出计算表达式).
(列出计算表达式).

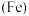 、钴
、钴 、镍
、镍 是第四周期第Ⅷ族的元素,其单质具有磁性,其化合物常用于制备电池导体.
是第四周期第Ⅷ族的元素,其单质具有磁性,其化合物常用于制备电池导体.(1)基态
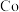 原子的核外电子排布式为
原子的核外电子排布式为
 原子具有相同未成对电子数的元素是
原子具有相同未成对电子数的元素是(2)
 、
、 、
、 原子半径相似、化学性质相似,原因是
原子半径相似、化学性质相似,原因是(3)配合物
 的中心原子价电子数与配体提供电子总数之和为
的中心原子价电子数与配体提供电子总数之和为 与
与 互为等电子体,
互为等电子体, 分子具有的化学键类型有
分子具有的化学键类型有A.
 键 B.
键 B. 键 C.离子键 D.金属键
键 C.离子键 D.金属键(4)
 的结构与相关性质见下表,其空间构型为
的结构与相关性质见下表,其空间构型为 的杂化形式为
的杂化形式为| 相对分子质量 | 熔点 | 沸点 | 结构 |
| 171 | 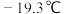 | 43℃ |  |
(5)钙钛矿中含有
 、
、 、O,它们形成的氧化物具有金属-绝缘体相转变特性,其晶胞结构中
、O,它们形成的氧化物具有金属-绝缘体相转变特性,其晶胞结构中 和O如下图所示,
和O如下图所示, 位于O形成正八面体空隙中.晶胞边长为
位于O形成正八面体空隙中.晶胞边长为 ,设
,设 为阿伏加 德罗常数的数值,则该氧化物的密度为
为阿伏加 德罗常数的数值,则该氧化物的密度为 (列出计算表达式).
(列出计算表达式).
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】白云石的化学组成是CaCO3·MgCO3,500℃以下分解成二氧化碳、金属氧化物和碳酸盐,800℃以上则彻底分解成氧化物。
(1)镁和钙在元素周期表中位于___________ 族,它们的价电子轨道式表示式为___________ (用n表示电子层数)。
(2)白云石500℃以下分解的化学方程式为___________ 。
(3)从物质结构角度分析、比较白云石分解生成的MgO和CaO的热稳定性。___________ 。
(4)白云石分解得到的CO2是氨碱法制备纯碱的基本原料之一,写出氨碱法制纯碱主要反应的化学方程式。___________ 、___________ ;向氨碱法的母液中加入生石灰可实现___________ (填化学式)的循环利用。处理后的母液经蒸发、浓缩、冷却、固化可得CaCl2。以质量比为1.44∶1的CaCl2·6H2O与冰水混合,可获得-55℃的低温,配制该制冷剂时不使用无水CaCl2的原因是___________ 。
(1)镁和钙在元素周期表中位于
(2)白云石500℃以下分解的化学方程式为
(3)从物质结构角度分析、比较白云石分解生成的MgO和CaO的热稳定性。
(4)白云石分解得到的CO2是氨碱法制备纯碱的基本原料之一,写出氨碱法制纯碱主要反应的化学方程式。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
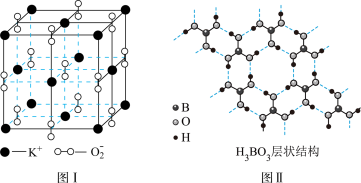
【推荐3】如图表示两种晶体的微观结构:
试回答下列有关问题:
(1)高温下,超氧化钾晶体呈立方体结构。晶体中氧的化合价部分为0价,部分为-2价。图I为超氧化钾晶体的一个晶胞(晶体中最小的重复单元)。则晶体中,与每个K+距离最近的K+有_________ 个,0价氧原子与-2价氧原子的数目比为_________ ;
(2)正硼酸(H3BO3)是一种片层结构的白色晶体,层内的H3BO3分子通过氢键相连(如图II)。下列有关说法正确的有_________ 。
①正硼酸晶体属于原子晶体
②H3BO3分子的稳定性与氢键有关
③在H3BO3分子中各原子未能都满足8e-稳定结构
④含1molH3BO3的晶体中有3mol氢键
⑤含1molH3BO3的晶体中有3mol极性共价键
⑥晶体中每个B与相邻的3个O共平面

试回答下列有关问题:
(1)高温下,超氧化钾晶体呈立方体结构。晶体中氧的化合价部分为0价,部分为-2价。图I为超氧化钾晶体的一个晶胞(晶体中最小的重复单元)。则晶体中,与每个K+距离最近的K+有
(2)正硼酸(H3BO3)是一种片层结构的白色晶体,层内的H3BO3分子通过氢键相连(如图II)。下列有关说法正确的有
①正硼酸晶体属于原子晶体
②H3BO3分子的稳定性与氢键有关
③在H3BO3分子中各原子未能都满足8e-稳定结构
④含1molH3BO3的晶体中有3mol氢键
⑤含1molH3BO3的晶体中有3mol极性共价键
⑥晶体中每个B与相邻的3个O共平面
您最近一年使用:0次



