铁、铝及其化合物在生产和生活中有着广泛的应用。
(1)某研究性学习小组设计了如图所示装置探究钢铁的腐蚀与防护。

为防止金属Fe被腐蚀,可以采用上述________________ (填装置序号)装置原理进行防护;装置③中总反应的离子方程式为______________________ 。
(2)用CH4或其他有机物、O2为原料可设计成原电池,以CnH2nOn、O2为原料,H2SO4溶液为电解质设计成燃料电池,则负极的电极反应式为___________________________ 。
(3)图1是在金属锌板上贴上一张用某溶液浸湿的滤纸,图2是NaBH4/H2O2燃料电池。
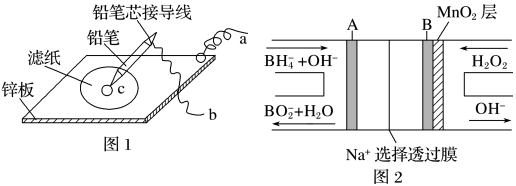
图2电池负极区的电极反应为_________________________ ;若用硫酸钠和酚酞的混合溶液浸湿滤纸,用导线将a、b直接相连,则滤纸出现_____________ 色,C位置的电极反应式为___________________ 若用KI淀粉溶液浸湿滤纸,用导线将a、b与A、B电极相连,铅笔芯C点处出现蓝色,则b接的是__________ (填A或B)电极。
(4)广西治理龙江河镉(Cd2+)污染时,先向河中投入沉淀剂将Cd2+转化为难溶物,再投入氯化铝,试说明氯化铝的作用_______________________________ (用必要的离子方程式和文字进行解释)。
(1)某研究性学习小组设计了如图所示装置探究钢铁的腐蚀与防护。

为防止金属Fe被腐蚀,可以采用上述
(2)用CH4或其他有机物、O2为原料可设计成原电池,以CnH2nOn、O2为原料,H2SO4溶液为电解质设计成燃料电池,则负极的电极反应式为
(3)图1是在金属锌板上贴上一张用某溶液浸湿的滤纸,图2是NaBH4/H2O2燃料电池。

图2电池负极区的电极反应为
(4)广西治理龙江河镉(Cd2+)污染时,先向河中投入沉淀剂将Cd2+转化为难溶物,再投入氯化铝,试说明氯化铝的作用
更新时间:2019-01-30 18:14:09
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】回答下列问题:
(1)如图所示电解装置可使铝表面氧化膜增厚。则阳极的电极反应式为_______ 。

(2)一种用铅蓄电池进行电絮凝净水装置如图所示:
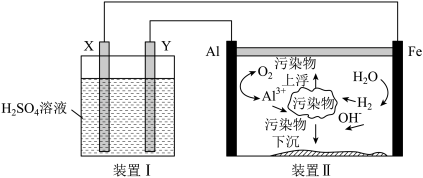
①装置Ⅰ中 电极的电极材料是
电极的电极材料是_______ (填化学式),工作时 向
向_______ (填“X”或“Y”)电极移动;Y电极的电极反应式为_______ 。
②装置Ⅱ中 电极的电极反应式为
电极的电极反应式为_______ 。
(1)如图所示电解装置可使铝表面氧化膜增厚。则阳极的电极反应式为

(2)一种用铅蓄电池进行电絮凝净水装置如图所示:

①装置Ⅰ中
 电极的电极材料是
电极的电极材料是 向
向②装置Ⅱ中
 电极的电极反应式为
电极的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】某探究活动小组想利用原电池反应检测金属的活动性顺序,有甲、乙两位同学均使用镁片与铝片作电极,但甲同学将电极放入6mol·L-1稀硫酸中,乙同学将电极放入6mol·L-1的NaOH溶液中,如图所示。

(1)写出甲池中发生的有关电极反应式:
负极___________ ,正极___________ 。
(2)乙池中负极为___________ ,正极发生___________ 反应(填“氧化”或“还原”),总反应的离子方程式为___________ 。
(3)由此实验,可得到如下哪些结论?___________。
(4)上述实验也反过来证明了“利用金属活动性顺序直接判断原电池中正、负极”的做法___________ (填“可靠”或“不可靠”)。如不可靠,则请你提出另一个判断原电池正、负极可行的实验方案:___________ 。

(1)写出甲池中发生的有关电极反应式:
负极
(2)乙池中负极为
(3)由此实验,可得到如下哪些结论?___________。
| A.利用原电池反应判断金属活动性顺序应注意选择合适的介质 |
| B.镁的金属性不一定比铝的金属性强 |
| C.该实验说明金属活动性顺序表已过时,已没有实用价值 |
| D.该实验说明化学研究对象复杂,反应条件多变,应具体问题具体分析 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】微型纽扣电池在现代生活中有广泛应用。有一种银锌电池,其电极分别是Ag2O和Zn,电解质溶液为KOH溶液,电极反应为Zn+2OH--2e-=ZnO+H2O,Ag2O+H2O+2e-=2Ag+2OH-
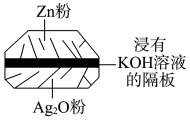
根据上述反应式,完成下列填空。
(1)下列叙述正确的是______ 。
A.在使用过程中,电解质溶液中的KOH被不断消耗,pH减小
B.使用过程中,电子由Ag2O极经外电路流向Zn极
C.Zn是负极,Ag2O是正极
D.Zn电极发生还原反应,Ag2O电极发生氧化反应
(2)写出电池的总反应式:___________ 。
(3)使用时,负极区的pH____ (填“增大”“减小”或“不变”)。

根据上述反应式,完成下列填空。
(1)下列叙述正确的是
A.在使用过程中,电解质溶液中的KOH被不断消耗,pH减小
B.使用过程中,电子由Ag2O极经外电路流向Zn极
C.Zn是负极,Ag2O是正极
D.Zn电极发生还原反应,Ag2O电极发生氧化反应
(2)写出电池的总反应式:
(3)使用时,负极区的pH
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】如图所示,某同学设计一个甲醚( )燃料电池并探究氯碱工业和粗铜精炼的原理,其中乙装置中X为阳离子交换膜。
)燃料电池并探究氯碱工业和粗铜精炼的原理,其中乙装置中X为阳离子交换膜。
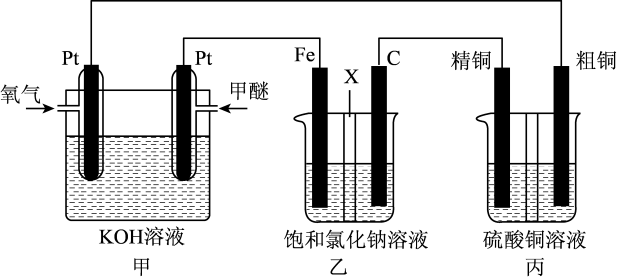
根据要求回答相关问题:
(1)甲装置是_______ 装置(填“电解池”或“原电池”),通 的一极是
的一极是_______ (填“正极”、“负极”、“阴极”或“阳极”),通 一极的电极反应式为
一极的电极反应式为_______ 。
(2)乙装置中石墨电极(C)的电极反应式为_______ 。反应一段时间后,乙装置中主要在_______ (填“铁极”或“石墨极”)区生成氢氧化钠。乙装置中总反应的化学方程式为_______ 。
(3)如果粗铜中含有锌、银、金等杂质,反应一段时间,丙装置中形成阳极泥的成分是_______ (填化学式)。
(4)若甲装置中有2.24 L(标准状况)氧气参加反应,则乙装置中铁电极上生成的气体的物质的量为_______ 。
 )燃料电池并探究氯碱工业和粗铜精炼的原理,其中乙装置中X为阳离子交换膜。
)燃料电池并探究氯碱工业和粗铜精炼的原理,其中乙装置中X为阳离子交换膜。
根据要求回答相关问题:
(1)甲装置是
 的一极是
的一极是 一极的电极反应式为
一极的电极反应式为(2)乙装置中石墨电极(C)的电极反应式为
(3)如果粗铜中含有锌、银、金等杂质,反应一段时间,丙装置中形成阳极泥的成分是
(4)若甲装置中有2.24 L(标准状况)氧气参加反应,则乙装置中铁电极上生成的气体的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
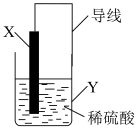
【推荐2】某课外小组利用废旧金属器件制作一个简易的铜锌原电池,为确保实验安全设计了如图装置。___________ 能转化为___________ 能。
(2)该装置中电极X为___________ 极(选填“正”或“负”),电子从电极___________ 转移到电极___________ (填电极物质名称)。
(3)电极Y上发生的电极反应式为___________ 。
(4)把a、b、c、d四种金属浸入稀硫酸中,用导线两两相连可以组成各种原电池。若a、b相连,a为负极;c、d相连,d上有气泡逸出;a、c相连,a质量减少;b、d相连,b为正极。则四种金属的活动性顺序由大到小为___________(填字母)。
(2)该装置中电极X为
(3)电极Y上发生的电极反应式为
(4)把a、b、c、d四种金属浸入稀硫酸中,用导线两两相连可以组成各种原电池。若a、b相连,a为负极;c、d相连,d上有气泡逸出;a、c相连,a质量减少;b、d相连,b为正极。则四种金属的活动性顺序由大到小为___________(填字母)。
| A.a>c>b>d | B.a>c>d>b | C.b>d>c>a | D.a>b>c>d |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】电池是人类生产和生活中的重要能量来源,各式各样的电池的发明是化学对人类的重要贡献。请结合所学知识回答下列问题:
Ⅰ.硅是太阳能电池的重要材料,工业冶炼纯硅的原理是:
粗硅冶炼:①
精炼硅:②
③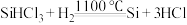
化学反应与能量变化如图所示,回答下列问题:

(1)硅在元素周期表中的位置是___________ 。
(2)已知 的结构与
的结构与 相似,
相似,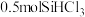 发生反应③时有
发生反应③时有___________  极性键断裂。
极性键断裂。
(3)①是___________ 反应(填“吸热”或“放热”),反应②与反应③是否为可逆反应___________ (填“是”或“否”)。
Ⅱ.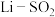 电池具有优良的性能,其工作原理如图所示。
电池具有优良的性能,其工作原理如图所示。
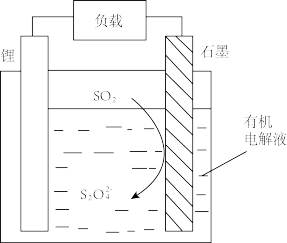
(4)石墨是该电池的___________ 极(填“正”或“负”),其电极反应式为___________ 。
(5)该电池用到的 在工业制备硫酸中可以转化为
在工业制备硫酸中可以转化为 ,其反应方程式为
,其反应方程式为___________ 。
(6)将 设计成燃料电池,其利用率更高,装置如图所示(
设计成燃料电池,其利用率更高,装置如图所示( 为多孔碳棒),已知
为多孔碳棒),已知 电极附近通入的是
电极附近通入的是 ,写出
,写出 电极处发生的电极反应式
电极处发生的电极反应式___________ , 还可以通过加聚反应合成一种材料
还可以通过加聚反应合成一种材料___________ (填“结构简式”)该材料可用于食品、药品的包装。

Ⅰ.硅是太阳能电池的重要材料,工业冶炼纯硅的原理是:
粗硅冶炼:①

精炼硅:②

③
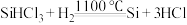
化学反应与能量变化如图所示,回答下列问题:

(1)硅在元素周期表中的位置是
(2)已知
 的结构与
的结构与 相似,
相似,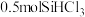 发生反应③时有
发生反应③时有 极性键断裂。
极性键断裂。(3)①是
Ⅱ.
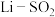 电池具有优良的性能,其工作原理如图所示。
电池具有优良的性能,其工作原理如图所示。
(4)石墨是该电池的
(5)该电池用到的
 在工业制备硫酸中可以转化为
在工业制备硫酸中可以转化为 ,其反应方程式为
,其反应方程式为(6)将
 设计成燃料电池,其利用率更高,装置如图所示(
设计成燃料电池,其利用率更高,装置如图所示( 为多孔碳棒),已知
为多孔碳棒),已知 电极附近通入的是
电极附近通入的是 ,写出
,写出 电极处发生的电极反应式
电极处发生的电极反应式 还可以通过加聚反应合成一种材料
还可以通过加聚反应合成一种材料
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】近几年来关于氮污染的治理倍受关注,根据氮的性质回答以下问题;
(1)Ertl(获2007年诺贝尔化学奖)对合成氨机理进行深入研究,并将研究成果用于汽车尾气处理中,在催化剂存在下可将NO和CO反应转化为两种无色无毒气体,用化学反应方程式 表示这个过程_______ ;
(2)过度排放的氮氧化物易导致硝酸型酸雨,用化学方程式 表示NO2形成酸雨的原因:_______ 。飞机排放的氮氧化物(NO和NO2)会破坏臭氧层,它们和O3和O发生如下反应:O3+NO=NO2+O2;O+NO2=NO+O2,这两个反应反复循环,氮的氧化物在破坏臭氧层的过程中起到了_______ 的作用。
(3)潜艇中使用的液氨-液氧燃料电池工作原理如图所示:

①电极a名称是_______ (填“正极”或“负极”)。
②电解质溶液中OHˉ离子向_______ 移动(填“电极a”或“电极b”)。
③电极a的电极反应式为_______ 。电极b的电极反应式为_______ 。
(1)Ertl(获2007年诺贝尔化学奖)对合成氨机理进行深入研究,并将研究成果用于汽车尾气处理中,在催化剂存在下可将NO和CO反应转化为两种无色无毒气体,用
(2)过度排放的氮氧化物易导致硝酸型酸雨,用
(3)潜艇中使用的液氨-液氧燃料电池工作原理如图所示:

①电极a名称是
②电解质溶液中OHˉ离子向
③电极a的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】氯气在生产生活中有广泛的用途,制取氯气的途径有多种。完成下列填空:
(1)工业上用电解饱和食盐水制取氯气,氯气在电解池的______ 极产生;氯气与氢氧化钠反应得到消毒剂次氯酸钠,发生反应的化学方程式为________ ;向次氯酸钠溶液中加入少量稀盐酸,可以增强消毒效果,这是因为生成了_____ (填物质名称)。
(2)实验室制取氯气的化学方程式为MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O,该反应中,氯气是
MnCl2+Cl2↑+2H2O,该反应中,氯气是______ (填“氧化”或“还原”)产物;若反应过程中转移了2 mol电子,则在标准状况下可以得到_______ L氯气。
(3)实验室常用排饱和食盐水的方法收集氯气,请用平衡移动原理解释用饱和食盐水而不用水的原因。___________
(4)有机化工中会利用反应4HCl(g)+O2(g) 2Cl2(g)+2H2O(g)+Q(Q>0)来产生氯气。向5 L的密闭容器中加入0.5 mol HCl与0.2 mol O2,在一定条件下发生反应,Cl2的物质的量与时间t的关系如图中OA段所示。0~8 min时Cl2的平均反应速率为
2Cl2(g)+2H2O(g)+Q(Q>0)来产生氯气。向5 L的密闭容器中加入0.5 mol HCl与0.2 mol O2,在一定条件下发生反应,Cl2的物质的量与时间t的关系如图中OA段所示。0~8 min时Cl2的平均反应速率为_________________ 。t0时刻改变某一条件,Cl2的物质的量变化曲线如图中AB段所示,则t0时改变的条件一定是__________ 。
a.降低温度 b.增大压强 c.加入HCl
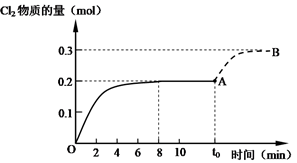
(1)工业上用电解饱和食盐水制取氯气,氯气在电解池的
(2)实验室制取氯气的化学方程式为MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O,该反应中,氯气是
MnCl2+Cl2↑+2H2O,该反应中,氯气是(3)实验室常用排饱和食盐水的方法收集氯气,请用平衡移动原理解释用饱和食盐水而不用水的原因。
(4)有机化工中会利用反应4HCl(g)+O2(g)
 2Cl2(g)+2H2O(g)+Q(Q>0)来产生氯气。向5 L的密闭容器中加入0.5 mol HCl与0.2 mol O2,在一定条件下发生反应,Cl2的物质的量与时间t的关系如图中OA段所示。0~8 min时Cl2的平均反应速率为
2Cl2(g)+2H2O(g)+Q(Q>0)来产生氯气。向5 L的密闭容器中加入0.5 mol HCl与0.2 mol O2,在一定条件下发生反应,Cl2的物质的量与时间t的关系如图中OA段所示。0~8 min时Cl2的平均反应速率为a.降低温度 b.增大压强 c.加入HCl
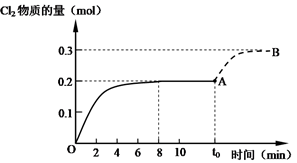
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】电化学方法是化工生产及生活中常用的一种方法。回答下列问题:
(1)二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂。目前已开发出用电解法制取ClO2的新工艺如图所示:

①图中用石墨作电极,在一定条件下电解饱和食盐水制取ClO2。产生ClO2的电极应连接电源的_______ (填“正极”或“负极”),对应的电极反应式为_______ 。
②a极区pH_______ (填“增大”“减小”或“不变”)。
③图中应使用_______ (填“阴”或“阳”)离子交换膜。
(2)电解硝酸工业的尾气NO可制备NH4NO3(NH4NO3溶液显酸性),其工作原理如图所示:
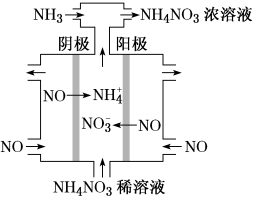
①阴极的电极反应式为_______ 。
②将电解生成的HNO3全部转化为NH4NO3,则通入的NH3与实际参加反应的NO的物质的量之比至少为_______ 。
(1)二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂。目前已开发出用电解法制取ClO2的新工艺如图所示:

①图中用石墨作电极,在一定条件下电解饱和食盐水制取ClO2。产生ClO2的电极应连接电源的
②a极区pH
③图中应使用
(2)电解硝酸工业的尾气NO可制备NH4NO3(NH4NO3溶液显酸性),其工作原理如图所示:

①阴极的电极反应式为
②将电解生成的HNO3全部转化为NH4NO3,则通入的NH3与实际参加反应的NO的物质的量之比至少为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】(1)铁在生产和生活中有着广泛的应用。某研究性学习小组设计了如下图所示装置探究钢铁的腐蚀与防护。
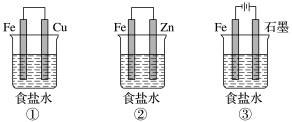
在相同条件下,三组装置中铁电极腐蚀最快的是_____________ (填装置序号),该装置中正极电极反应式为___________________________ ;为防止金属Fe被腐蚀,效果最好的为上述的_____________ (填装置序号)装置原理进行防护;装置③中总反应的离子方程式为__________________________________________________ 。
(2)燃料电池作为新型电池,越来越多地应用于日常生活,该学习小组设计了以下电池:将两个多孔的石墨电极插入KOH溶液中,向两极分别通入CH4和O2,构成燃料电池。其中通入CH4的电极是电极反应式___________________________________ ,电池工作期间,OH-应向_______ 极移动。

在相同条件下,三组装置中铁电极腐蚀最快的是
(2)燃料电池作为新型电池,越来越多地应用于日常生活,该学习小组设计了以下电池:将两个多孔的石墨电极插入KOH溶液中,向两极分别通入CH4和O2,构成燃料电池。其中通入CH4的电极是电极反应式
您最近一年使用:0次



