I.按要求写出对应反应的离子方程式:
(1)硫酸镁溶液与氢氧化钡溶液反应__________________________ ;
(2)用氢氧化钠溶液出去CO中少量的 CO2气_______________________ ;
(3)用稀硫酸除去铁钉上的铁锈(主要成分是Fe2O3)____________________ ;
II.以下8种为中学化学中常见的物质:
①CaO ②H2O ③胆矾 ④CaCO3 ⑤H2SO4 ⑥氨水 ⑦酒精 ⑧Cu
请按下列分类标准回答问题:
(1)属于电解质的是_________ (2)属于盐的是_________
(3)属于氧化物的是_________ (4)属于非电解质的是_________
(1)硫酸镁溶液与氢氧化钡溶液反应
(2)用氢氧化钠溶液出去CO中少量的 CO2气
(3)用稀硫酸除去铁钉上的铁锈(主要成分是Fe2O3)
II.以下8种为中学化学中常见的物质:
①CaO ②H2O ③胆矾 ④CaCO3 ⑤H2SO4 ⑥氨水 ⑦酒精 ⑧Cu
请按下列分类标准回答问题:
(1)属于电解质的是
(3)属于氧化物的是
更新时间:2016/12/09 01:14:15
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】(1)实验室常根据物质分类的原则存放药品,某学校实验室其中的四个药品柜已经存放了如下部分药品,实验室新购进一些晶体碘,应该将它存放在____ (填“甲”、“乙”、“丙”或“丁”)柜,理由是____ 。
(2)磷的一种化合物叫亚磷酸(H3PO3)。已知:0.1mol•L﹣1H3PO3溶液的pH=1.7;H3PO3与NaOH反应只生成NaH2PO3和Na2HPO3两种盐。H3PO3和碘水反应,碘水棕黄色褪去,再加AgNO3有黄色沉淀生成。关于H3PO3的说法:①强酸②弱酸③二元酸④三元酸⑤氧化性酸⑥还原性酸,其中正确的是____ (填序号)。
A.②④⑥ B.②③⑤ C.①④⑤ D.②③⑥
(3)“三酸(硫酸、盐酸、硝酸)”与“两碱(氢氧化钠、碳酸钠)”能发生反应。将一定量的稀硫酸逐滴滴入到氢氧化钠和碳酸钠的混合溶液中,边滴加边搅拌,直至有少量气泡产生,此过程中共发生的离子反应有______ 个,生成气体的离子方程式为_______ 。
| 药品柜 | 甲柜 | 乙柜 | 丙柜 | 丁柜 |
| 药品 | 乙醇、乙酸 | 活性炭、红磷 | 锌粒、铜片 | 氯化钠、氯化钾 |
(2)磷的一种化合物叫亚磷酸(H3PO3)。已知:0.1mol•L﹣1H3PO3溶液的pH=1.7;H3PO3与NaOH反应只生成NaH2PO3和Na2HPO3两种盐。H3PO3和碘水反应,碘水棕黄色褪去,再加AgNO3有黄色沉淀生成。关于H3PO3的说法:①强酸②弱酸③二元酸④三元酸⑤氧化性酸⑥还原性酸,其中正确的是
A.②④⑥ B.②③⑤ C.①④⑤ D.②③⑥
(3)“三酸(硫酸、盐酸、硝酸)”与“两碱(氢氧化钠、碳酸钠)”能发生反应。将一定量的稀硫酸逐滴滴入到氢氧化钠和碳酸钠的混合溶液中,边滴加边搅拌,直至有少量气泡产生,此过程中共发生的离子反应有
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】现有以下物质:① 溶液;②液氨;③
溶液;②液氨;③ 固体;④熔融
固体;④熔融 ;⑤
;⑤ 胶体;⑥铜;⑦
胶体;⑥铜;⑦ ;⑧稀醋酸。
;⑧稀醋酸。
(1)物质中属于电解质的是___________ 。(填序号)
(2)写出①和⑧的水溶液反应的离子方程式:___________ 。
(3)写出④的电离方程式:___________ 。
(4)在足量①的水溶液中通入少量⑦,发生反应的离子方程式为___________ 。现有11g⑦如发生上述反应,至少需要溶质质量分数为20%的①___________ g。
(5)在小烧杯中加入20mL蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和 溶液,继续煮沸至溶液呈
溶液,继续煮沸至溶液呈___________ 色,即制得 胶体。写出制备物质⑤的化学方程式:
胶体。写出制备物质⑤的化学方程式:___________ 。
 溶液;②液氨;③
溶液;②液氨;③ 固体;④熔融
固体;④熔融 ;⑤
;⑤ 胶体;⑥铜;⑦
胶体;⑥铜;⑦ ;⑧稀醋酸。
;⑧稀醋酸。(1)物质中属于电解质的是
(2)写出①和⑧的水溶液反应的离子方程式:
(3)写出④的电离方程式:
(4)在足量①的水溶液中通入少量⑦,发生反应的离子方程式为
(5)在小烧杯中加入20mL蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和
 溶液,继续煮沸至溶液呈
溶液,继续煮沸至溶液呈 胶体。写出制备物质⑤的化学方程式:
胶体。写出制备物质⑤的化学方程式:
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】就这样等到了傍晚,白风终于伸了个懒腰:“完工啦~”
此时你正趴在床上无所事事,听到这话你迫不及待地爬了起来:“好耶,终于可以出去玩啦~”
“不过,咱们上哪里玩呢?”
“要不……去学校的实验室?”
“好呀~刚好我想折腾药品惹~”
“对了,我们学校的实验室管理有个传统,进去之前要先证明自己的实力。”白风还没说完,他们就被负责的老师给拦在了门口。
“如果你们要进有机实验室,至少先把这个做了。”
(1)完成下列物质的系统命名:

___________ ,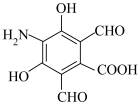
___________ 。
(2)“这瓶钠经历了什么……”看着瓶中已经变质的金属钠,白风皱了皱眉头:“怎么变黄色液体了……?”
实验室的药品摆放都是按照一定分类摆放的,白风在检查“酸”区的时候却意外发现了这样一瓶放错的金属钠:“这瓶钠不应该是单质区的吗?”
好奇之下,他用水稀释了一下黄色液体,然后滴了一滴在pH试纸上。
然后,他看着变红的pH试纸,沉默了……
“查了下资料,这个黄色液体的颜色看着和煤油在空气中变质的样子一样……”你上前戳了戳白风,说道。
白风皱着眉头,在那里思考了半天,忽然一拍脑袋:“我好像知道怎么回事了! ”
Ⅰ.据此推测实验室存放药品采用的分类方法是___________ 。
Ⅱ.试猜测产生这一现象的原因:______________________ 。
此时你正趴在床上无所事事,听到这话你迫不及待地爬了起来:“好耶,终于可以出去玩啦~”
“不过,咱们上哪里玩呢?”
“要不……去学校的实验室?”
“好呀~刚好我想折腾药品惹~”
“对了,我们学校的实验室管理有个传统,进去之前要先证明自己的实力。”白风还没说完,他们就被负责的老师给拦在了门口。
“如果你们要进有机实验室,至少先把这个做了。”
(1)完成下列物质的系统命名:


(2)“这瓶钠经历了什么……”看着瓶中已经变质的金属钠,白风皱了皱眉头:“怎么变黄色液体了……?”
实验室的药品摆放都是按照一定分类摆放的,白风在检查“酸”区的时候却意外发现了这样一瓶放错的金属钠:“这瓶钠不应该是单质区的吗?”
好奇之下,他用水稀释了一下黄色液体,然后滴了一滴在pH试纸上。
然后,他看着变红的pH试纸,沉默了……
“查了下资料,这个黄色液体的颜色看着和煤油在空气中变质的样子一样……”你上前戳了戳白风,说道。
白风皱着眉头,在那里思考了半天,忽然一拍脑袋:“我好像知道怎么回事了! ”
Ⅰ.据此推测实验室存放药品采用的分类方法是
Ⅱ.试猜测产生这一现象的原因:
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐1】氧化还原反应在生产、生活中应用广泛,酸性KMnO4、H2O2、Fe(NO3)3是重要的氧化剂。用所学知识回答问题( )
(1)在稀硫酸中,KMnO4能将H2C2O4氧化为CO2。该反应的化学方程式为_________ ,反应中消耗1mol的MnO4—时转移电子数为______ 。
(2)取300mL 0.2mol/L的KI溶液与一定量的酸性KMnO4溶液恰好反应,生成等物质的量的I2和KIO3,则消耗KMnO4的物质的量的是____ mol。
(3)在Fe(NO3)3溶液中加入Na2SO3溶液,溶液先由棕黄色变为浅绿色,过一会又变为棕黄色,溶液先变为浅绿色的离子方程式是_______________ ,又变为棕黄色的原因是________ 。
(1)在稀硫酸中,KMnO4能将H2C2O4氧化为CO2。该反应的化学方程式为
(2)取300mL 0.2mol/L的KI溶液与一定量的酸性KMnO4溶液恰好反应,生成等物质的量的I2和KIO3,则消耗KMnO4的物质的量的是
(3)在Fe(NO3)3溶液中加入Na2SO3溶液,溶液先由棕黄色变为浅绿色,过一会又变为棕黄色,溶液先变为浅绿色的离子方程式是
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】I.写出下列反应的化学方程式
(1)铁与水蒸气高温反应:_______ ;
(2)用氯化铁溶液刻蚀铜:_______ ;
(3)铜与浓硫酸制 :
:_______ ;
(4) 悬浊液置于空气中:
悬浊液置于空气中:_______ 。
II.写出下列反应的离子方程式
(5)铝与氢氧化钠溶液:_______ ;
(6) 溶于稀硫酸:
溶于稀硫酸:_______ ;
(7)氯化亚铁溶液中通氯气:_______ ;
(8)铜与稀硝酸制NO:_______ 。
(1)铁与水蒸气高温反应:
(2)用氯化铁溶液刻蚀铜:
(3)铜与浓硫酸制
 :
:(4)
 悬浊液置于空气中:
悬浊液置于空气中:II.写出下列反应的
(5)铝与氢氧化钠溶液:
(6)
 溶于稀硫酸:
溶于稀硫酸:(7)氯化亚铁溶液中通氯气:
(8)铜与稀硝酸制NO:
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,比C12、O2、C1O2、KMnO4氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
(1)干法制备高铁酸钠的主要反应为:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑
①该反应中的氧化剂是_______ ,还原剂是_____ ,每生成1mol Na2FeO4转移___ mol电子。
②简要说明K2FeO4作为水处理剂时,在水处理过程中所起的作用_______________________ 。
(2)湿法制备高铁酸钾(K2FeO4)的反应体系中有六种数粒:Fe(OH)3、C1O-、OH-、FeO42-、C1-、H2O。
①写出并配平湿法制高铁酸钾的离子反应方程式:___________________ 。
②每生成1mol FeO42-转移__ mol电子,若反应过程中转移了0.3mol电子,则还原产物的物质的量为_____ mol。
③低温下,在高铁酸钠溶液中加入KOH至饱和可析出高铁酸钾(K2FeO4),说明什么问题_____________ 。
(1)干法制备高铁酸钠的主要反应为:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑
①该反应中的氧化剂是
②简要说明K2FeO4作为水处理剂时,在水处理过程中所起的作用
(2)湿法制备高铁酸钾(K2FeO4)的反应体系中有六种数粒:Fe(OH)3、C1O-、OH-、FeO42-、C1-、H2O。
①写出并配平湿法制高铁酸钾的离子反应方程式:
②每生成1mol FeO42-转移
③低温下,在高铁酸钠溶液中加入KOH至饱和可析出高铁酸钾(K2FeO4),说明什么问题
您最近半年使用:0次



