请根据化学方程式计算:
(1)完全中和0.3 mol氢氧化钠,需要硫酸的物质的量是多少?需要物质的量浓度为3 mol·L-1 稀硫酸多少升?(要求写出计算过程)
(2)质量分数为98%、密度为1.84 g·mL-1的浓硫酸的物质的量浓度是多少?若有此浓硫酸来稀释成3 mol·L-1稀硫酸,需要该浓硫酸多少毫升?(要求写出计算过程)
(1)完全中和0.3 mol氢氧化钠,需要硫酸的物质的量是多少?需要物质的量浓度为3 mol·L-1 稀硫酸多少升?(要求写出计算过程)
(2)质量分数为98%、密度为1.84 g·mL-1的浓硫酸的物质的量浓度是多少?若有此浓硫酸来稀释成3 mol·L-1稀硫酸,需要该浓硫酸多少毫升?(要求写出计算过程)
更新时间:2016-01-04 16:25:31
|
【知识点】 化学计量
相似题推荐
计算题
|
适中
(0.65)
【推荐1】现有Fe和Fe2O3组成的混合物27.2g,与100mL一定浓度稀硫酸恰好完全反应,放出标准状况下2.24L H2,向反应后的溶液中滴入KSCN溶液,未见红色。求混合物中Fe的质量____ 。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】(1)3.01×1024个氢氧根离子的物质的量是___________ mol,其摩尔质量为___________ 。
(2)在标准状况下,0.01 mol某气体的质量为0.44 g,则该气体的密度为___________ g·L−1(保留小数点后两位),该气体的相对分子质量为___________ 。
(3)在标准状况下,由CO和CO2组成的混合气体为6.72 L,质量为12 g,此混合物中CO和CO2物质的量之比是___________ ,CO的体积分数是___________ ,CO的质量分数是___________ ,C和O原子个数比是___________ 。
(2)在标准状况下,0.01 mol某气体的质量为0.44 g,则该气体的密度为
(3)在标准状况下,由CO和CO2组成的混合气体为6.72 L,质量为12 g,此混合物中CO和CO2物质的量之比是
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】回答下列问题:
(1)质量相同的①H2、②SO2、③O3三种气体中,含有分子数目由多到少的顺序为_______ (填序号,下同);在同温同压下,密度由大到小的顺序为_______ 。
(2)固体A在一定温度下分解生成气体B、C、D,反应方程式为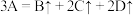 。若测得生成物气体对氢气的密度是15,则固体A的摩尔质量是
。若测得生成物气体对氢气的密度是15,则固体A的摩尔质量是_______ 。
(3)将8g铁片放入100mL硫酸铜溶液中,溶液中的Cu2+全部被还原时,铁片变为8.6g,则原c(CuSO4)为_______ mol/L。
(4)将部分在空气中被氧化的金属钠5.08g投入到水中充分反应得到100mL溶液,在该溶液中加入足量的金属铝,收集到标准状况下的气体6720mL(溶液体积变化忽略不计)。计算:
①最后所得的溶液的物质的量浓度为_______ mol/L。
②被氧化的金属钠的质量为_______ g。
(1)质量相同的①H2、②SO2、③O3三种气体中,含有分子数目由多到少的顺序为
(2)固体A在一定温度下分解生成气体B、C、D,反应方程式为
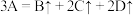 。若测得生成物气体对氢气的密度是15,则固体A的摩尔质量是
。若测得生成物气体对氢气的密度是15,则固体A的摩尔质量是(3)将8g铁片放入100mL硫酸铜溶液中,溶液中的Cu2+全部被还原时,铁片变为8.6g,则原c(CuSO4)为
(4)将部分在空气中被氧化的金属钠5.08g投入到水中充分反应得到100mL溶液,在该溶液中加入足量的金属铝,收集到标准状况下的气体6720mL(溶液体积变化忽略不计)。计算:
①最后所得的溶液的物质的量浓度为
②被氧化的金属钠的质量为
您最近一年使用:0次



