化学是一门以实验为基础的学科,化学所取得的丰硕成果,是与实验的重要作用分不开的.结合下来实验常用到的仪器回答问题:
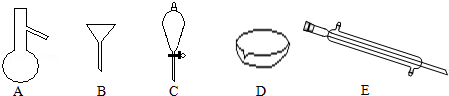
(1)填写以下仪器的名称:A_________ E________ .
(2)用四氯化碳提取出溴水中的溴的方法叫做:_________ ,将溴的四氯化碳溶液和水分离开的操作叫做:_______ ,下列是进行该操作的步骤,正确的顺序是:_________ .
①将混合物倒入分液漏斗中,并放在铁架台的铁圈上静置,分层;
②从分液漏斗上口倒出上层溶液
③将分液漏斗的玻璃塞打开或使玻璃塞上的凹槽对准漏斗颈部的小孔
④分液漏斗下面导管紧贴烧杯内壁,旋开活塞,用烧杯接受溶液
⑤检查分液漏斗活塞和颈部的玻璃塞是否漏水.
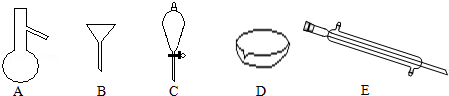
(1)填写以下仪器的名称:A
(2)用四氯化碳提取出溴水中的溴的方法叫做:
①将混合物倒入分液漏斗中,并放在铁架台的铁圈上静置,分层;
②从分液漏斗上口倒出上层溶液
③将分液漏斗的玻璃塞打开或使玻璃塞上的凹槽对准漏斗颈部的小孔
④分液漏斗下面导管紧贴烧杯内壁,旋开活塞,用烧杯接受溶液
⑤检查分液漏斗活塞和颈部的玻璃塞是否漏水.
更新时间:2016-12-09 11:05:35
|
相似题推荐
填空题
|
适中
(0.64)
【推荐1】如何除去下列物质中混有的少量杂质(括号内为杂质)。写出最佳的化学方程式,是离子反应的只写离子方程式。
(1)Na2CO3固体(NaHCO3):_______________________ 。
(2)NaHCO3溶液(Na2CO3):________________________ 。
(3)FeCl3溶液(FeCl2):___________________________ 。
(4)FeCl2溶液(FeCl3):___________________________ 。
(5)SO2气体中( HCl):__________________________ 。
(6)单质Mg粉(Al):______________________________ 。
(1)Na2CO3固体(NaHCO3):
(2)NaHCO3溶液(Na2CO3):
(3)FeCl3溶液(FeCl2):
(4)FeCl2溶液(FeCl3):
(5)SO2气体中( HCl):
(6)单质Mg粉(Al):
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】苯乙酸铜是合成优良催化剂、传感材料纳米氧化铜的重要前驱体之一。下面是它的一种实验室合成路线:
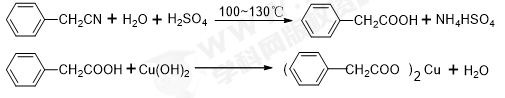

制备苯乙酸的装置如右图所示(加热和夹持装置等略),已知:苯乙酸的熔点为76.5 ℃,微溶于冷水,溶于乙醇。回答下列问题:(1)在250 mL三口瓶a中加入70 mL70%硫酸。配制此硫酸时,加入蒸馏水与浓硫酸的先后顺序是_____________________ 。
(2)将a中的溶液加热至100 ℃,缓缓滴加40 g苯乙腈到硫酸溶液中,然后升温至130 ℃继续反应。在装置中,仪器b的作用是______________ ;仪器c的名称是__________ ,其作用是__________________ 。反应结束后加适量冷水,再分离出苯乙酸粗品。加入冷水的目的是_______ 。下列仪器中可用于分离苯乙酸粗品的是___________ (填标号)。
A.分液漏斗B.漏斗C.烧杯D.直形冷凝管E.玻璃棒


制备苯乙酸的装置如右图所示(加热和夹持装置等略),已知:苯乙酸的熔点为76.5 ℃,微溶于冷水,溶于乙醇。回答下列问题:(1)在250 mL三口瓶a中加入70 mL70%硫酸。配制此硫酸时,加入蒸馏水与浓硫酸的先后顺序是
(2)将a中的溶液加热至100 ℃,缓缓滴加40 g苯乙腈到硫酸溶液中,然后升温至130 ℃继续反应。在装置中,仪器b的作用是
A.分液漏斗B.漏斗C.烧杯D.直形冷凝管E.玻璃棒
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】在纯碱工业的发展史上,法国的路布兰、比利时的索尔维和我国的侯德榜等科学家都取得了卓越的成就。
【方法一】路布兰以食盐、浓硫酸、焦炭和石灰石为原料,制得了纯碱。其反应原理为
①2NaCl+H2SO4(浓) Na2SO4+2HCl
Na2SO4+2HCl
②2Na2SO4+4C Na2S+4CO↑
Na2S+4CO↑
③Na2S+CaCO3 Na2CO3+CaS
Na2CO3+CaS
(1)写出反应③的基本反应类型___________
(2)用单线桥法表示反应②的电子转移方向和数目___________
【方法二】索尔维和侯德榜又发明了新的制碱方法,其模拟流程如下:

【资料查阅】
I.通常情况下,1体积水中大约能溶解700体积氨气,1体积水中大约能溶解1体积二氧化碳。
Ⅱ.饱和食盐水中发生的主要反应为NH3+CO2+H2O+NaCl=NaHCO3↓+NH4Cl。
(3)上述流程中过程②的主要操作的名称是___________ ,可以循环利用的物质是___________ (填化学式)。
(4)写出饱和食盐水中主要反应的离子方程式___________
(5)为了提高产率,往饱和食盐水中通入气体时,你认为应该先通入___________ (填“NH3”或“CO2”),你的理由是___________ 。
(6)母液的主要成分为NH4Cl和NaCl,写出在加热条件下母液与石灰乳反应的化学方程式___________ 。
【方法一】路布兰以食盐、浓硫酸、焦炭和石灰石为原料,制得了纯碱。其反应原理为
①2NaCl+H2SO4(浓)
 Na2SO4+2HCl
Na2SO4+2HCl②2Na2SO4+4C
 Na2S+4CO↑
Na2S+4CO↑③Na2S+CaCO3
 Na2CO3+CaS
Na2CO3+CaS(1)写出反应③的基本反应类型
(2)用单线桥法表示反应②的电子转移方向和数目
【方法二】索尔维和侯德榜又发明了新的制碱方法,其模拟流程如下:

【资料查阅】
I.通常情况下,1体积水中大约能溶解700体积氨气,1体积水中大约能溶解1体积二氧化碳。
Ⅱ.饱和食盐水中发生的主要反应为NH3+CO2+H2O+NaCl=NaHCO3↓+NH4Cl。
(3)上述流程中过程②的主要操作的名称是
(4)写出饱和食盐水中主要反应的离子方程式
(5)为了提高产率,往饱和食盐水中通入气体时,你认为应该先通入
(6)母液的主要成分为NH4Cl和NaCl,写出在加热条件下母液与石灰乳反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.64)
【推荐1】有下列化学仪器:①量筒 ②烧杯 ③容量瓶 ④胶头滴管 ⑤细口试剂瓶 ⑥标签纸
(1)现需要配制500 mL 1 mol·L-1的硫酸溶液,需用质量分数为98%、密度为1.84 g·cm-3的浓硫酸______ mL。
(2)从上述仪器中,按实验使用的先后顺序,其编号排列是_______________
(3)容量瓶使用前应进行的操作是_______________
(4)若实验遇到下列情况,对硫酸溶液的物质的量浓度的影响,下列判断正确的是___________
①用量筒量取硫酸时俯视读数 ②稀释浓硫酸的烧杯中原有少量蒸馏水;
(1)现需要配制500 mL 1 mol·L-1的硫酸溶液,需用质量分数为98%、密度为1.84 g·cm-3的浓硫酸
(2)从上述仪器中,按实验使用的先后顺序,其编号排列是
(3)容量瓶使用前应进行的操作是
(4)若实验遇到下列情况,对硫酸溶液的物质的量浓度的影响,下列判断正确的是
①用量筒量取硫酸时俯视读数 ②稀释浓硫酸的烧杯中原有少量蒸馏水;
| A.①偏低②不变 | B.①偏低②偏低 | C.①偏高②偏低 | D.①偏高②不变 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】在已经提取氯化钠、溴、镁等化学物质的富碘卤水中,采用所给的工艺流程生产单质碘:
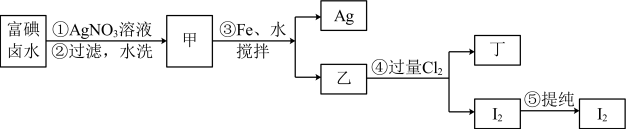
(1)碘位于元素周期表中的第___________ 周期第___________ 族。
(2)步骤③加Fe的目的是___________
(3)写出步骤④的化学方程式:___________ 。
(4)上述生产流程中,可以循环利用的副产物是,已知上述流程得到的该副产物含杂质,现需将其制成生产所需的试剂,先后还需加入___________ 、___________ 来进行处理。
(5)甲物质见光易变黑,其原因是(用化学方程式表示)___________ 。
(6)第⑤步操作可供提纯I2的两种方法是和___________ 、___________ 。

(1)碘位于元素周期表中的第
(2)步骤③加Fe的目的是
(3)写出步骤④的化学方程式:
(4)上述生产流程中,可以循环利用的副产物是,已知上述流程得到的该副产物含杂质,现需将其制成生产所需的试剂,先后还需加入
(5)甲物质见光易变黑,其原因是(用化学方程式表示)
(6)第⑤步操作可供提纯I2的两种方法是和
您最近一年使用:0次
填空题
|
适中
(0.64)
【推荐3】化学实验是化学学科学习、探究的基础。
(1)下列描述错误的是_______ .
a.为了防止试剂瓶内的试剂被污染,取用后多余的试剂一定都不能放回原试剂瓶
b.滴定管、容量瓶、分液漏斗在使用时都需要检漏
c.海带中碘的提取时需要对干海带进行灼烧,此时需要用到的仪器有玻璃棒、燃烧匙、 泥三角、三脚架、酒精灯
d.检验Na2SO3固体是否被氧化:取少量固体溶于水,加入Ba(NO3)2溶液,产生白色沉淀,滴加稀盐酸,观察白色沉淀是否溶解
e.海带中碘的提取时,对碘水中的碘进行萃取可采用裂化汽油、苯、四氯化碳、无水酒精等有机溶剂
(2)某溶液中可能存在Br-、CO32-、SO32-、I-、A13+、Mg2+、Na+等7种离子中的某几种。现取该溶液进行实验,得到如下现象:
①向溶液中滴加足量氯水后,溶液变橙色,且有无色气泡冒出;
②向所得橙色溶液中加入足量BaCl2溶液,有白色沉淀生成,加入稀盐酸沉淀不溶解。
③向所得溶液中继续滴加淀粉溶液,溶液不变蓝色。
据此可以推断:该溶液肯定存在的离子是:_______________
在②中产生的自色沉淀是:_________________
(1)下列描述错误的是
a.为了防止试剂瓶内的试剂被污染,取用后多余的试剂一定都不能放回原试剂瓶
b.滴定管、容量瓶、分液漏斗在使用时都需要检漏
c.海带中碘的提取时需要对干海带进行灼烧,此时需要用到的仪器有玻璃棒、燃烧匙、 泥三角、三脚架、酒精灯
d.检验Na2SO3固体是否被氧化:取少量固体溶于水,加入Ba(NO3)2溶液,产生白色沉淀,滴加稀盐酸,观察白色沉淀是否溶解
e.海带中碘的提取时,对碘水中的碘进行萃取可采用裂化汽油、苯、四氯化碳、无水酒精等有机溶剂
(2)某溶液中可能存在Br-、CO32-、SO32-、I-、A13+、Mg2+、Na+等7种离子中的某几种。现取该溶液进行实验,得到如下现象:
①向溶液中滴加足量氯水后,溶液变橙色,且有无色气泡冒出;
②向所得橙色溶液中加入足量BaCl2溶液,有白色沉淀生成,加入稀盐酸沉淀不溶解。
③向所得溶液中继续滴加淀粉溶液,溶液不变蓝色。
据此可以推断:该溶液肯定存在的离子是:
在②中产生的自色沉淀是:
您最近一年使用:0次



