中国有广阔的海岸线,海水的综合利用大有可为,海水中溴含量约为65mg/L,从海水中提取Br2的工艺流程如下:
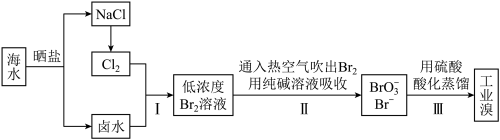
(1)①从海水中获得淡水的方法主要有_________ (填一种)
②我国政府规定食用盐中必须加入一定量的KIO3(碘酸钾),其中碘元素的化合价为_________ 价。
(2)经过化学变化才能从海水中获得的物质是__________(选填字母序号)
(3)步骤Ⅱ通入热空气或水蒸气吹出Br2,利用了溴的___________;
(4)请写出步骤Ⅱ中反应的离子反应方程式__________ 。

(1)①从海水中获得淡水的方法主要有
②我国政府规定食用盐中必须加入一定量的KIO3(碘酸钾),其中碘元素的化合价为
(2)经过化学变化才能从海水中获得的物质是__________(选填字母序号)
| A.氯、溴、碘 | B.钠、镁 | C.烧碱、氢气 | D.食盐、淡水 |
| A.氧化性 | B.还原性 | C.挥发性 | D.腐蚀性 |
更新时间:2016-12-09 11:05:35
|
相似题推荐
解答题-工业流程题
|
较难
(0.4)
名校
【推荐1】海水的综合利用可以制备金属镁,其流程如图所示:

(1)海水提取镁要用到海滩上的贝壳,贝壳煅烧过程中发生反应的化学方程式为___________________________________________ 。
(2)母液中加入石灰乳反应的离子方程式为______ 。
(3)实验室里将粗盐制成精盐的过程中,在溶解、过滤、蒸发三个步骤的操作中都要用到玻璃棒,分别说明在这三种情况下使用玻璃棒的目的。
溶解时:_____________________________ ,
过滤时:_____________________________ ,
蒸发时:_____________________________ 。
(4)除去粗盐溶液中含有的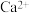 、
、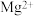 、
、 ,可依次加入
,可依次加入 溶液、NaOH溶液、
溶液、NaOH溶液、________ ,最后加入_________ 调节pH至中性。
(5)写出金属镁在空气中燃烧的化学方程式____________________________ 。

(1)海水提取镁要用到海滩上的贝壳,贝壳煅烧过程中发生反应的化学方程式为
(2)母液中加入石灰乳反应的离子方程式为
(3)实验室里将粗盐制成精盐的过程中,在溶解、过滤、蒸发三个步骤的操作中都要用到玻璃棒,分别说明在这三种情况下使用玻璃棒的目的。
溶解时:
过滤时:
蒸发时:
(4)除去粗盐溶液中含有的
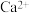 、
、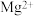 、
、 ,可依次加入
,可依次加入 溶液、NaOH溶液、
溶液、NaOH溶液、(5)写出金属镁在空气中燃烧的化学方程式
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐2】海水中有丰富的资源,多种多样的海洋动物、植物、矿藏等。如图是从海水中提取某些物质的示意图。已知:海水中含量最高的几种离子的浓度依次为

请根据以上信息回答下列问题:
(1)写出步骤②的操作名称_______ ;实验室中步骤⑤所需的玻璃仪器除烧杯外,还需要的仪器是___________ 。
(2)D具有杀菌消毒的作用,请写出反应④的离子方程式___________ 。
(3)初步提纯后的粗盐中含有等Ca2+、Mg2+、 等杂质,精制得到精盐的步骤顺序为
等杂质,精制得到精盐的步骤顺序为________ 。(用字母序号填空)
a.加适量盐酸;b.加稍过量的氯化钡溶液,再加稍过量的NaOH溶液;c.过滤;d.蒸发结晶;e.加稍过量碳酸钠溶液
(4)____________ (填“能”或“不能”)用 一种试剂替代步骤②中两种试剂,理由是
一种试剂替代步骤②中两种试剂,理由是________ 。
| 微粒种类 | Cl- | Na+ | Mg2+ |  | Ca2+ |
| 微粒浓度 | 0.55mol·L-1 | 0.47mol·L-1 | 0.054mol·L-1 | 0.027mol·L-1 | 0.01mol·L-1 |

请根据以上信息回答下列问题:
(1)写出步骤②的操作名称
(2)D具有杀菌消毒的作用,请写出反应④的离子方程式
(3)初步提纯后的粗盐中含有等Ca2+、Mg2+、
 等杂质,精制得到精盐的步骤顺序为
等杂质,精制得到精盐的步骤顺序为a.加适量盐酸;b.加稍过量的氯化钡溶液,再加稍过量的NaOH溶液;c.过滤;d.蒸发结晶;e.加稍过量碳酸钠溶液
(4)
 一种试剂替代步骤②中两种试剂,理由是
一种试剂替代步骤②中两种试剂,理由是
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐3】海洋约占地球表面积的71%,海水化学资源的利用具有非常广阔的前景.
(1)海水晒盐可获得粗盐,在实验室中粗盐经过溶解、________ 、________ 可制得精盐。(填具体操作名称)
(2)镁及其合金是一种用途很广的金属材料,目前世界上60%的镁是从海水中提取的,其主要步骤如下:
①为了使MgSO4转化为Mg(OH)2 , 试剂①可以选用________ 。
②试从节约能源、提高金属镁的纯度分析,以下适宜的冶镁方法是________ 。
A.Mg(OH)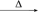 MgO
MgO Mg B.Mg(OH)
Mg B.Mg(OH)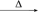 MgO
MgO Mg
Mg
C.Mg(OH)2 MgCl2
MgCl2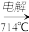 Mg D.Mg(OH)2
Mg D.Mg(OH)2 MgCl2
MgCl2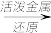 Mg
Mg
(3)溴及其化合物用途十分广泛,我国正在大力开展海水提溴的研究和开发工作。工业以浓缩海水为原料提取溴的部分过程如下:
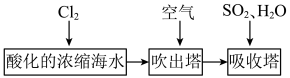
某课外小组在实验室模拟上述过程设计以下装置进行实验(所有橡胶制品均已被保护,夹持装置已略去):

①A装置中通入a气体的目的是(用离子方程式表示)______________________________ ;
②A装置中通入a气体一段时间后,停止通入,改通热空气.通入热空气的目的是___________ ;
③反应过程中,B装置中有SO42﹣生成,检验SO42﹣的方法是____________________________ ;
④C装置的作用是______________________________________________ 。
(1)海水晒盐可获得粗盐,在实验室中粗盐经过溶解、
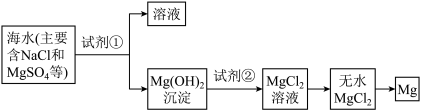
(2)镁及其合金是一种用途很广的金属材料,目前世界上60%的镁是从海水中提取的,其主要步骤如下:

①为了使MgSO4转化为Mg(OH)2 , 试剂①可以选用
②试从节约能源、提高金属镁的纯度分析,以下适宜的冶镁方法是
A.Mg(OH)
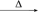 MgO
MgO Mg B.Mg(OH)
Mg B.Mg(OH)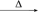 MgO
MgO Mg
MgC.Mg(OH)2
 MgCl2
MgCl2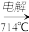 Mg D.Mg(OH)2
Mg D.Mg(OH)2 MgCl2
MgCl2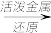 Mg
Mg(3)溴及其化合物用途十分广泛,我国正在大力开展海水提溴的研究和开发工作。工业以浓缩海水为原料提取溴的部分过程如下:

某课外小组在实验室模拟上述过程设计以下装置进行实验(所有橡胶制品均已被保护,夹持装置已略去):

①A装置中通入a气体的目的是(用离子方程式表示)
②A装置中通入a气体一段时间后,停止通入,改通热空气.通入热空气的目的是
③反应过程中,B装置中有SO42﹣生成,检验SO42﹣的方法是
④C装置的作用是
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐1】查阅资料知:Br2的沸点为58.8 ℃,密度为3.119 g·cm-3,微溶于水,有毒。
Ⅰ.(1)常温下,单质溴通常呈________ 态,保存时通常在盛溴的试剂瓶中加入少量________ 。
Ⅱ.工业生产中,海水提取溴常用热空气吹出法。其生产流程如下:

某化学实验小组模拟该法设计了如下实验装置(夹持装置略去)从浓缩的海水中提取液溴。实验步骤如下:
①关闭活塞b、d,打开活塞a、c,向A中缓慢通入Cl2至反应结束;
②关闭a、c,打开b、d,向A中鼓入足量热空气;
③关闭b,打开a,再通过A向B中通入足量的Cl2;
④将B中所得液体进行蒸馏,收集液溴。

(2)当观察到A中液面上方出现________ (实验现象)时即可判断步骤①中反应已经结束。
(3)X试剂可以是________ (填字母,下同),尾气处理选用________ 。
a.H2O b.饱和食盐水 c.氢氧化钠溶液 d.饱和Na2SO3溶液
B中X试剂发生反应的离子方程式为________________________________ 。
(4)蒸馏时应该选择______ (填序号),操作中应控制的关键实验条件为____________ 。
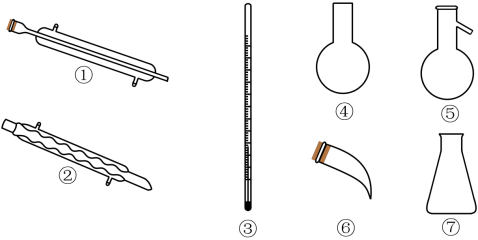
Ⅲ.该实验小组利用制得的单质溴研究H2与Br2生成HBr的反应,实验装置如下:

(5)E装置可用来检验反应产物HBr,则D装置的作用是_______ 。若要检验E中收集的HBr,图示装置检验HBr还不够完善,请结合原有实验装置予以改进:__________ 。
Ⅰ.(1)常温下,单质溴通常呈
Ⅱ.工业生产中,海水提取溴常用热空气吹出法。其生产流程如下:

某化学实验小组模拟该法设计了如下实验装置(夹持装置略去)从浓缩的海水中提取液溴。实验步骤如下:
①关闭活塞b、d,打开活塞a、c,向A中缓慢通入Cl2至反应结束;
②关闭a、c,打开b、d,向A中鼓入足量热空气;
③关闭b,打开a,再通过A向B中通入足量的Cl2;
④将B中所得液体进行蒸馏,收集液溴。

(2)当观察到A中液面上方出现
(3)X试剂可以是
a.H2O b.饱和食盐水 c.氢氧化钠溶液 d.饱和Na2SO3溶液
B中X试剂发生反应的离子方程式为
(4)蒸馏时应该选择

Ⅲ.该实验小组利用制得的单质溴研究H2与Br2生成HBr的反应,实验装置如下:

(5)E装置可用来检验反应产物HBr,则D装置的作用是
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐2】溴主要以Br- 形式存在于海水(呈弱碱性)中,利用空气吹出法从海水中提溴,工艺流程示意如下。

资料:常温下溴呈液态,深红棕色,易挥发。
(1)酸化:将海水酸化的主要目的是避免___ (写离子反应方程式)。
(2)脱氯:除去含溴蒸气中残留的Cl2
①具有脱氯作用的离子是____ 。
②溶液失去脱氯作用后,补加FeBr2或加入____ ,脱氯作用恢复。
(3)富集、制取Br2:
用Na2CO3溶液吸收溴,Br2歧化为BrO3- 和Br-。再用H2SO4酸化歧化后的溶液得到Br2,其离子反应方程式为____ 。
(4)探究(3)中所用H2SO4浓度对Br2生成的影响,实验如下:
①B中溶液呈棕红色说明产生了____ 。
②分析C中溶液颜色变浅的原因,甲同学认为是发生了化学反应所致;乙同学认为是用水稀释所致。若认为甲同学的分析合理,请用具体的反应说明理由;若认为乙同学的分析合理,进一步设计实验方案说明。理由或方案:____ 。
③酸化歧化后的溶液宜选用的酸是____ (填“稀硫酸”或“浓硫酸”)。

资料:常温下溴呈液态,深红棕色,易挥发。
(1)酸化:将海水酸化的主要目的是避免
(2)脱氯:除去含溴蒸气中残留的Cl2
①具有脱氯作用的离子是
②溶液失去脱氯作用后,补加FeBr2或加入
(3)富集、制取Br2:
用Na2CO3溶液吸收溴,Br2歧化为BrO3- 和Br-。再用H2SO4酸化歧化后的溶液得到Br2,其离子反应方程式为
(4)探究(3)中所用H2SO4浓度对Br2生成的影响,实验如下:
| 序号 | A | B | C |
| 试剂组成 | 1 mol/L NaBr 20% H2SO4 | 1 mol/L NaBr 98% H2SO4 | 将B中反应后溶液用水稀释 |
| 实验现象 | 无明显现象 | 溶液呈棕红色,放热 | 溶液颜色变得很浅 |
①B中溶液呈棕红色说明产生了
②分析C中溶液颜色变浅的原因,甲同学认为是发生了化学反应所致;乙同学认为是用水稀释所致。若认为甲同学的分析合理,请用具体的反应说明理由;若认为乙同学的分析合理,进一步设计实验方案说明。理由或方案:
③酸化歧化后的溶液宜选用的酸是
您最近一年使用:0次
【推荐3】地球的表面积为 5.1 亿平方公里,其中海洋的面积为 3.67 亿平方公里,占整个地球表面积的 70.8 %。海洋是一个巨大的化学资源宝库,请回答下列问题:
Ⅰ 请列举海水淡化的一种方法____________________________ 。
II 下面是海水资源综合利用的部分流程图:

(1)步骤①中,粗盐中含有 Ca2+、Mg2+、 等杂质离子,精制时常用的试剂有:a 稀盐酸;b 氯化钡溶液;c 氢氧化钠溶液;d 碳酸钠溶液。加入试剂的顺序正确的是
等杂质离子,精制时常用的试剂有:a 稀盐酸;b 氯化钡溶液;c 氢氧化钠溶液;d 碳酸钠溶液。加入试剂的顺序正确的是_____ (填字母)。
(2)反应④由无水 MgCl2制取金属镁的常用工业方法是________________ (用化学方程式表示)。
(3)步骤⑤已经获得 Br2,步骤⑥又将 Br2还原为 Br-,其目的是________ 。写出步骤⑥反应的离子方程式 ______________________________ 。由海水提溴过程中的反应可得出 Cl-、SO2、Br-还原性由强到弱的顺序是____________________ 。
(4)工业上也可以用 Na2CO3溶液吸收吹出的 Br2,生成溴化钠和溴酸钠,同时放出 CO2。写出反应的离子方程式__________________________ 。最后再用H2SO4处理所得溶液重新得到Br2,其反应的离子方程式为 ______________________________ 。
Ⅲ 海带灰中富含以 I- 形式存在的碘元素。实验室提取 I2的途径如图所示:

(1)灼烧海带至灰烬时所用的主要仪器名称是_______________ 。
(2)向酸化的滤液中加过氧化氢溶液,写出该反应的离子方程式_________ 。反应结束后,再加入 CCl4作萃取剂,振荡、静置,可以观察到 CCl4层呈 ______ 色。
Ⅰ 请列举海水淡化的一种方法
II 下面是海水资源综合利用的部分流程图:

(1)步骤①中,粗盐中含有 Ca2+、Mg2+、
 等杂质离子,精制时常用的试剂有:a 稀盐酸;b 氯化钡溶液;c 氢氧化钠溶液;d 碳酸钠溶液。加入试剂的顺序正确的是
等杂质离子,精制时常用的试剂有:a 稀盐酸;b 氯化钡溶液;c 氢氧化钠溶液;d 碳酸钠溶液。加入试剂的顺序正确的是(2)反应④由无水 MgCl2制取金属镁的常用工业方法是
(3)步骤⑤已经获得 Br2,步骤⑥又将 Br2还原为 Br-,其目的是
(4)工业上也可以用 Na2CO3溶液吸收吹出的 Br2,生成溴化钠和溴酸钠,同时放出 CO2。写出反应的离子方程式
Ⅲ 海带灰中富含以 I- 形式存在的碘元素。实验室提取 I2的途径如图所示:

(1)灼烧海带至灰烬时所用的主要仪器名称是
(2)向酸化的滤液中加过氧化氢溶液,写出该反应的离子方程式
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐1】浩瀚的大海蕴藏着丰富的化学资源,从海水中提取物质,已日益受到人们的重视。
(1)从海水提取溴,一般要经过______ 、氧化和_______ 三个步骤。常用的氧化剂是氯气,反应的离子方程式为___________________________ 。
(2)从海带中提取碘,除试管、烧杯、漏斗、玻璃棒、带铁圈的铁架台、酒精灯、坩埚、泥三角、坩埚钳、托盘天平,还缺少的玻璃仪器有_______________________________________ 。
(3)将灼烧后的海带灰溶解、过滤,为检验滤液中有I-,取1mL滤液,先加_______ ,再滴加_____________ ,并不断振荡,观察到溶液变蓝。提取碘水中的碘,可选用的萃取剂有________________ 。(选填编号)
a. 裂化汽油 b. 甲苯 c. 酒精 d. 四氯化碳
(4)为了预防碘缺乏病,国家规定食盐中应含有一定量的碘酸钾。利用下列原理可测定食盐中的含碘量(质量分数):IO3-+5I-+6H+→3I2+3H2O,I2+2S2O32-→2I-+S4O62-。称ag食盐样品,配成250mL溶液,取出25.00mL。加入过量的硫酸酸化KI,若滴定消耗bmol/L的硫代硫酸钠溶液vmL,则该食盐中的含碘量为______ (写出表达式)。
(1)从海水提取溴,一般要经过
(2)从海带中提取碘,除试管、烧杯、漏斗、玻璃棒、带铁圈的铁架台、酒精灯、坩埚、泥三角、坩埚钳、托盘天平,还缺少的玻璃仪器有
(3)将灼烧后的海带灰溶解、过滤,为检验滤液中有I-,取1mL滤液,先加
a. 裂化汽油 b. 甲苯 c. 酒精 d. 四氯化碳
(4)为了预防碘缺乏病,国家规定食盐中应含有一定量的碘酸钾。利用下列原理可测定食盐中的含碘量(质量分数):IO3-+5I-+6H+→3I2+3H2O,I2+2S2O32-→2I-+S4O62-。称ag食盐样品,配成250mL溶液,取出25.00mL。加入过量的硫酸酸化KI,若滴定消耗bmol/L的硫代硫酸钠溶液vmL,则该食盐中的含碘量为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐2】中国有广阔的海岸线,建设发展海洋经济、海水的综合利用大有可为。
Ⅰ.海洋植物中富含一种人体必需的微量元素——碘。实验室模拟从海带中提取碘单质的流程图如下:_______ 中进行。
(2)操作Ⅰ中具体实验步骤:_______
(3)为寻找氯水的替代品,某同学设计了用 代替氯水。请写出此反应的离子方程式:
代替氯水。请写出此反应的离子方程式:_______ 。
Ⅱ.空气吹出法工艺,是目前“海水提溴”的最主要方法之一,其流程如图所示,试回答下列问题:_______ 。
(5)步骤Ⅱ中涉及的离子方程式如下,请在下面横线上填入适当的化学计量数_______ 。
_______ _______
_______ _______
_______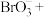 _______
_______ _______
_______
(6)上述流程中吹出的溴蒸气,也可先用二氧化硫水溶液吸收,再用氯气氧化后蒸馏。写出溴与二氧化硫水溶液反应的离子方程式:_______ 。
Ⅲ.镁及其合金是一种用途很广的金属材料,目前60%的镁是从海水中提取的。主要步骤如下: 转化为
转化为 ,试剂①工业上选用
,试剂①工业上选用_______ (填化学式)。
(8)熔融状态的无水 通电后会产生Mg和
通电后会产生Mg和 ,试写出该反应的化学方程式:
,试写出该反应的化学方程式:_______ 。
Ⅰ.海洋植物中富含一种人体必需的微量元素——碘。实验室模拟从海带中提取碘单质的流程图如下:

(2)操作Ⅰ中具体实验步骤:
(3)为寻找氯水的替代品,某同学设计了用
 代替氯水。请写出此反应的离子方程式:
代替氯水。请写出此反应的离子方程式:Ⅱ.空气吹出法工艺,是目前“海水提溴”的最主要方法之一,其流程如图所示,试回答下列问题:

(5)步骤Ⅱ中涉及的离子方程式如下,请在下面横线上填入适当的化学计量数
_______
 _______
_______ _______
_______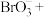 _______
_______ _______
_______
(6)上述流程中吹出的溴蒸气,也可先用二氧化硫水溶液吸收,再用氯气氧化后蒸馏。写出溴与二氧化硫水溶液反应的离子方程式:
Ⅲ.镁及其合金是一种用途很广的金属材料,目前60%的镁是从海水中提取的。主要步骤如下:
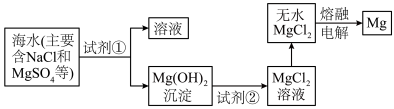
 转化为
转化为 ,试剂①工业上选用
,试剂①工业上选用(8)熔融状态的无水
 通电后会产生Mg和
通电后会产生Mg和 ,试写出该反应的化学方程式:
,试写出该反应的化学方程式:
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐3】全球海水中溴的储藏量丰富,约占地球溴总储藏量的99%,故溴有“海洋元素”之称,海水中溴含量为65mg/L。空气吹出法工艺是目前“海水提溴”的最主要方法之一、其工艺流程如图:
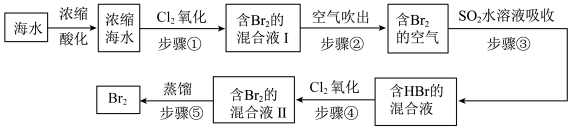
(1)步骤①中获得Br2的离子方程式为____ 。
(2)根据上述反应可判断SO2、Cl2、Br2三种物质氧化性由强到弱的顺序是____ 。
(3)步骤③中若吸收剂为饱和Na2SO3溶液(足量),则完全吸收1molBr2共有___ 个电子转移(用NA的代数式表示)。
碘是人体必需的一种微量元素。海洋植物中富含碘元素。实验室模拟从海带中提取碘单质的流程图如图:

(4)设计“操作Ⅰ”的主要步骤溶解和____ 。
(5)“试剂a”通常应具有一定的____ 性。利用H2O2完成“溶液A”向“溶液B”的转变。写出该反应的化学方程式:________________ 。
(6)由于“溶液B”中I2的含量较低,“操作II”能将I2“富集、浓缩”到“有机溶液X”中。
已知:I2在以下试剂中的溶解度都大于水,则“试剂b”可以是___ 。(选填编号)
(7)“操作II”宜选用的装置是 。(选填编号)
(8)在操作II后,检验提取碘后的水层是否仍含有碘单质的方法是:____ 。
(9)已知:KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O,I2+2S2O =2I-+S4O
=2I-+S4O ,学生测定某碘盐(含KIO3)中碘元素的含量,其步骤为:
,学生测定某碘盐(含KIO3)中碘元素的含量,其步骤为:
a.准确称取120g食盐,加适量蒸馏水使其完全溶解
b.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全
c.以淀粉为指示剂,逐滴加入物质的量浓度为2.0×10-3mol·L-1的Na2S2O3溶液50.0mL,恰好反应完全。则所测盐中碘的含量是____ mg•g-1(保留四位小数)。

(1)步骤①中获得Br2的离子方程式为
(2)根据上述反应可判断SO2、Cl2、Br2三种物质氧化性由强到弱的顺序是
(3)步骤③中若吸收剂为饱和Na2SO3溶液(足量),则完全吸收1molBr2共有
碘是人体必需的一种微量元素。海洋植物中富含碘元素。实验室模拟从海带中提取碘单质的流程图如图:

(4)设计“操作Ⅰ”的主要步骤溶解和
(5)“试剂a”通常应具有一定的
(6)由于“溶液B”中I2的含量较低,“操作II”能将I2“富集、浓缩”到“有机溶液X”中。
已知:I2在以下试剂中的溶解度都大于水,则“试剂b”可以是
| 试剂 | A.乙醇 | B.溴水 | C.四氯化碳 | D.裂化汽油 |
| 相关性质 | 与水互溶不与反应 | 与水互溶与I2反应 | 与水不互溶不与I2反应 | 与水不互溶与I2反应 |
(7)“操作II”宜选用的装置是 。(选填编号)
A.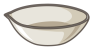 | B. | C.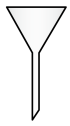 | D.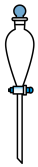 |
(8)在操作II后,检验提取碘后的水层是否仍含有碘单质的方法是:
(9)已知:KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O,I2+2S2O
 =2I-+S4O
=2I-+S4O ,学生测定某碘盐(含KIO3)中碘元素的含量,其步骤为:
,学生测定某碘盐(含KIO3)中碘元素的含量,其步骤为:a.准确称取120g食盐,加适量蒸馏水使其完全溶解
b.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全
c.以淀粉为指示剂,逐滴加入物质的量浓度为2.0×10-3mol·L-1的Na2S2O3溶液50.0mL,恰好反应完全。则所测盐中碘的含量是
您最近一年使用:0次



