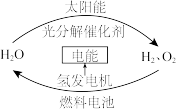
美国圣路易斯大学研制了一种新型的乙醇电池,其反应为:C2H5OH+3O2→ 2CO2+3H2O,电池示意如右图,下列说法正确的是
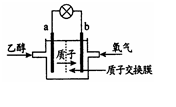

| A.a极为电池的正极 |
| B.b极发生氧化反应 |
| C.负极的反应为:4H++O2+4e-=2H2O |
| D.电池工作时,1mol乙醇被氧化时有12mol电子转移 |
9-10高二下·河北石家庄·期中 查看更多[4]
(已下线)2010年石家庄市第一中学第二学期高二年级期中考试化学试题山西省原平市范亭中学2018-2019学年高二下学期期末考试化学试题山西省吕梁市岚县中学2019—2020学年高二上学期期末考试化学试题(实验班、重点班)吉林省吉化第一高级中学校2020-2021学年高二上学期11月月考化学试题
更新时间:2016-12-09 00:27:23
|
相似题推荐
单选题
|
较易
(0.85)
名校
解题方法
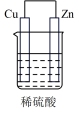
【推荐1】现有如右图所示的甲、乙两装置,下列说法中,正确的是
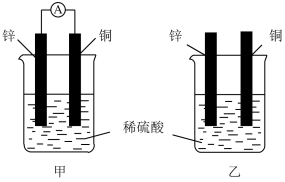
| A.两装置中,锌片的质量均是逐渐减小 |
| B.两装置中,铜片表面均无气泡产生 |
| C.甲装置中,电子从铜片经导线流向锌片 |
| D.装置乙中,氢离子在铜表面被还原,产生气泡 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】如果用铁片和铜片构成柠檬电池,会发生的是

柠檬电池
| A.铜片上发生反应:Cu - 2e- ═ Cu2+ | B.铁片是负极,其质量逐渐减小 |
| C.电流由铁片经导线流向铜片 | D.柠檬中蕴含的电能转化为化学能 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】关于下图所示的原电池,下列说法正确的是
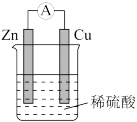

| A.Zn作负极 |
B.锌片上发生的反应: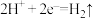 |
| C.电子由铜片通过导线流向锌片 |
| D.该装置是将电能转化为化学能 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】一种镁氧电池如图所示,电极材料为金属镁和吸附氧气的活性炭,电解液为KOH浓溶液。下列说法正确的是( )


| A.电池总反应式为2Mg+O2+2H2O=2Mg(OH)2 |
| B.正极反应式为Mg-2e-=Mg2+ |
| C.活性炭可以加快O2在负极上的反应速率 |
| D.电子的移动方向由b经外电路到a |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】燃料电池是燃料(如CO、H2、CH4等)跟氧气(或空气)起反应将化学能转变为电能的装置,若电解质溶液是强碱溶液,下面关于甲烷燃料电池的说法正确的是( )
A.负极反应式:O2+2H2O+4e-=4OH- |
| B.负极反应式:CH4+8OH--8e-=CO2+6H2O |
| C.随着放电的进行,溶液的氢氧根浓度不变 |
| D.放电时溶液中的阴离子向负极移动 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】某种熔融碳酸盐燃料电池以Li2CO3、K2CO3为电解质、以CH4为燃料时,该电池工作原理见如图。下列说法正确的是
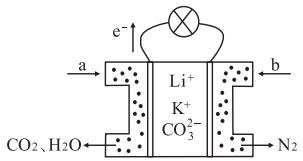

| A.此电池在常温时也能工作 |
B.正极电极反应式为:O2+2CO2+4e-=2 |
C. 向正极移动 向正极移动 |
| D.a为CH4,b为CO |
您最近一年使用:0次
单选题
|
较易
(0.85)
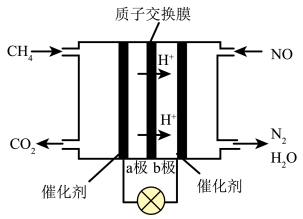
【推荐1】天然气( )既是清洁能源,又是重要的化工原料,在工业生产中应用广泛。某科研小组设计如图电池,利用
)既是清洁能源,又是重要的化工原料,在工业生产中应用广泛。某科研小组设计如图电池,利用 既除去了污染物NO,又提供了电能。下列说法正确的是
既除去了污染物NO,又提供了电能。下列说法正确的是
 )既是清洁能源,又是重要的化工原料,在工业生产中应用广泛。某科研小组设计如图电池,利用
)既是清洁能源,又是重要的化工原料,在工业生产中应用广泛。某科研小组设计如图电池,利用 既除去了污染物NO,又提供了电能。下列说法正确的是
既除去了污染物NO,又提供了电能。下列说法正确的是
| A.电池工作时正极区溶液pH减小 |
B.每耗掉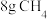 ,理论上电路中流过4mol电子 ,理论上电路中流过4mol电子 |
| C.a极与用电器的正极相连 |
D.正极反应式为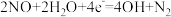 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】“碳呼吸电池”是一种新型能源装置,其工作原理如图所示。下列有关说法错误的是
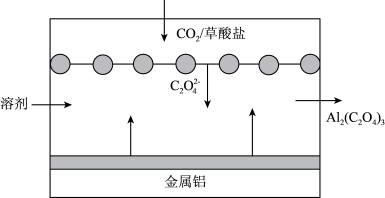

A.通入 的一极电极反应式为: 的一极电极反应式为: |
B.以该装置为电源为铅蓄电池充电,金属铝质量减少 时,理论上阴极质量减少144克 时,理论上阴极质量减少144克 |
C.每得到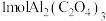 ,负极质量减少54克 ,负极质量减少54克 |
D. 向正极移动 向正极移动 |
您最近一年使用:0次

 )始终保持不变
)始终保持不变