在75℃左右,实验室用HgSO4做催化剂,可使乙炔与水反应制取乙醛。装置图如下:(夹持装置均已略去)
供选用试剂:电石(混有CaS等杂质)、HgO粉末、浓H2SO4、NaOH溶液、蒸馏水
资料提示:CaS遇水会产生H2S气体;HgSO4遇到H2S会发生催化剂中毒而失去活性。

回答下列问题:
(1)加入药品前,必须对装置进行的操作是:_________________________________ 。
(2)装置B中盛放的试剂为__________ ,作用是____________________
(3)写出A中发生的主要反应的化学方程式___________________________________
(4)反应温度应控制在75℃左右,采用E装置的优点是_________________________
供选用试剂:电石(混有CaS等杂质)、HgO粉末、浓H2SO4、NaOH溶液、蒸馏水
资料提示:CaS遇水会产生H2S气体;HgSO4遇到H2S会发生催化剂中毒而失去活性。

回答下列问题:
(1)加入药品前,必须对装置进行的操作是:
(2)装置B中盛放的试剂为
(3)写出A中发生的主要反应的化学方程式
(4)反应温度应控制在75℃左右,采用E装置的优点是
9-10高二下·湖北十堰·期中 查看更多[1]
(已下线)2009―2010学年十堰市东风高中高二下学期期中考试化学试题
更新时间:2016-12-09 00:37:27
|
相似题推荐
解答题-实验探究题
|
容易
(0.94)
名校
解题方法
【推荐1】Ⅰ.在实验室利用下列装置,可制备某些气体并验证其化学性质。
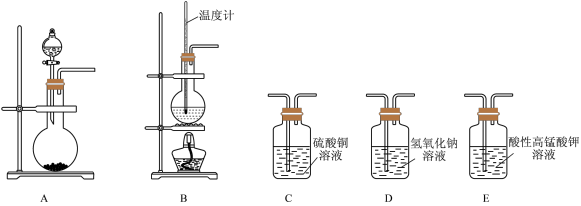
完成下列表格:
(3)D装置中氢氧化钠溶液的作用___ 。
Ⅱ.工业上用乙烯和氯气为原料,经下列各步合成聚氯乙烯(PVC):
乙烯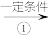 甲
甲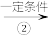 乙
乙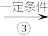 PVC
PVC
(4)甲的结构简式是___ ;
(5)反应③的化学方程式是__ 。
(6)下列说法正确的是___ 。
A.乙烯可以作为植物生长调节剂
B.PVC不能使酸性高锰酸钾溶液褪色
C.PVC中的官能团是碳碳双键和氯原子

完成下列表格:
| 序号 | 气体 | 装置连接顺序(填字母) | 制备反应的化学方程式 |
| (1) | 乙烯 | B→D→E | |
| (2) | 乙炔 |
Ⅱ.工业上用乙烯和氯气为原料,经下列各步合成聚氯乙烯(PVC):
乙烯
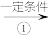 甲
甲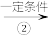 乙
乙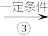 PVC
PVC (4)甲的结构简式是
(5)反应③的化学方程式是
(6)下列说法正确的是
A.乙烯可以作为植物生长调节剂
B.PVC不能使酸性高锰酸钾溶液褪色
C.PVC中的官能团是碳碳双键和氯原子
您最近一年使用:0次
解答题-实验探究题
|
容易
(0.94)
名校
【推荐1】FeCl3为黑棕色固体,无水氯化铁在300℃以上升华,遇潮湿空气极易潮解。
(1)甲组同学拟用下列装置制取纯净干燥的氯气。
①装置B的作用是_________
②装置A中发生反应时消耗的氧化剂和还原剂的物质的量之比为__________
(2)乙组同学选用甲组实验中的装置ABC和下列装置制取FeCl3

①乙组同学的实验装置中,依次连接的合理顺序为:a→_____ →_____ →_____ →_____ →_____ →_____
②连好装置,检查装置的气密性,先打开装置A中___________ (填仪器的名称)的活塞,直到______ 再点燃装置F处的酒精灯,目的是_______
③装置D的作用有_______
(3)实验结束后,取少量F中的固体加水溶解,欲对所得产物FeCl3中是否含有FeCl2进行检测,所需试剂是_______
a.KSCN b.H2O2 c.K3[Fe(CN)6] d. .K4[Fe(CN)6]
经检测发现溶液中含有Fe2+,丙同学认为所得产物FeCl3中一定含有FeCl2,丁同学认为不一定,理由是_____
(1)甲组同学拟用下列装置制取纯净干燥的氯气。
①装置B的作用是
②装置A中发生反应时消耗的氧化剂和还原剂的物质的量之比为
(2)乙组同学选用甲组实验中的装置ABC和下列装置制取FeCl3

①乙组同学的实验装置中,依次连接的合理顺序为:a→
②连好装置,检查装置的气密性,先打开装置A中
③装置D的作用有
(3)实验结束后,取少量F中的固体加水溶解,欲对所得产物FeCl3中是否含有FeCl2进行检测,所需试剂是
a.KSCN b.H2O2 c.K3[Fe(CN)6] d. .K4[Fe(CN)6]
经检测发现溶液中含有Fe2+,丙同学认为所得产物FeCl3中一定含有FeCl2,丁同学认为不一定,理由是
您最近一年使用:0次
解答题-实验探究题
|
容易
(0.94)
【推荐2】已知合金A由两种常见金属组成。为测定其组成,某同学的实验流程如图所示:

请回答:
(1)过程②中分离C和E的化学实验基本操作是________________________ ;
(2)溶液H中所含的阳离子有________________ (用离子符号表示);
(3)合金A与D在高温下反应的化学方程式_____________________________ 。

请回答:
(1)过程②中分离C和E的化学实验基本操作是
(2)溶液H中所含的阳离子有
(3)合金A与D在高温下反应的化学方程式
您最近一年使用:0次
解答题-工业流程题
|
容易
(0.94)
名校
【推荐3】“以废治废”是基于“绿色化学”观念治理污染的思路。用工业废碱渣(主要成分为Na2CO3)吸收烟气中的 SO2,得到亚硫酸钠(Na2SO3)粗品。其流程如下:
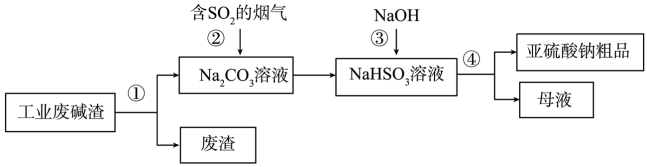
(1)为加快工业废碱渣中 Na2CO3的溶解,可采取的措施是_____ (写出一种即可)。
(2)上述流程中,加入NaOH 后,发生反应的化学方程式为_____ 。
(3)亚硫酸钠粗品中含有少量Na2SO4,原因是_____ 。
(4)设计实验证明亚硫酸钠粗品含有少量 Na2SO4的方案是:在一支试管中,加入少量 亚硫酸钠粗品,用适量蒸馏水溶解,_____ ,出现白色沉淀,则证明含有 Na2SO4。

(1)为加快工业废碱渣中 Na2CO3的溶解,可采取的措施是
(2)上述流程中,加入NaOH 后,发生反应的化学方程式为
(3)亚硫酸钠粗品中含有少量Na2SO4,原因是
(4)设计实验证明亚硫酸钠粗品含有少量 Na2SO4的方案是:在一支试管中,加入少量 亚硫酸钠粗品,用适量蒸馏水溶解,
您最近一年使用:0次



