如下图所示,某同学设计一个燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。
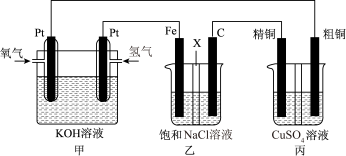
根据要求回答相关问题:
(1)通入氧气的电极为________ (填“正极”或“负极”),负极的电极反应式为______________ 。
(2)铁电极为________ (填“阳极”或“阴极”),石墨电极(C)的电极反应式为_______________ 。
(3)反应一段时间后,乙装置中生成氢氧化钠主要在________ 区。(填“铁极”或“石墨极”)
(4)如果粗铜中含有锌、银等杂质,则丙装置中反应一段时间后,硫酸铜溶液浓度将________ (填“增大”“减小”或“不变”)。
(5)若在标准状况下,有2.24 L氧气参加反应,则乙装置中铁电极上生成的气体的分子数为________ ;丙装置中阴极析出铜的质量为_______ 。

根据要求回答相关问题:
(1)通入氧气的电极为
(2)铁电极为
(3)反应一段时间后,乙装置中生成氢氧化钠主要在
(4)如果粗铜中含有锌、银等杂质,则丙装置中反应一段时间后,硫酸铜溶液浓度将
(5)若在标准状况下,有2.24 L氧气参加反应,则乙装置中铁电极上生成的气体的分子数为
11-12高二上·辽宁·期中 查看更多[5]
(已下线)2011-2012学年辽南协作体高二上学期期中考试化学试卷2015-2016学年山东省淄博六中高二上学期期末化学试卷河北省鸡泽县第一中学2016-2017学年高一下学期期中考试化学试题河南省郑州市中牟县二中2017-2018学年高二第一次月考化学试题黑龙江省嫩江市第一中学2021-2022学年高二下学期开学考试化学试题
更新时间:2016-12-09 14:47:37
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】某校课题组的同学设计“甲烷一碳酸盐一空气”熔盐燃料电池处理污水,其结构示意图如下:

污水处理原理:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3沉淀。Fe(OH)3有吸附性,可吸附污物而沉积下来,具有净化水的作用。阴极产生的气泡把污水中的悬浮物带到水面形成浮渣,刮去(或撤掉)浮渣,即起到了浮选净化的作用。
回答下列问题:
(1)图中A的化学式为_______ 。
(2)燃料电池正极反应为O2+2CO2+4e-=2CO ,负极反应式为
,负极反应式为_______ ;
(3)用电极反应式和离子或化学方程式说明电解池中生成Fe(OH)3的过程:_______
(4)若在阴极产生了2mol气体,则理论上熔融盐燃料电池消耗CH4(标准状况下)_______ 。

污水处理原理:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3沉淀。Fe(OH)3有吸附性,可吸附污物而沉积下来,具有净化水的作用。阴极产生的气泡把污水中的悬浮物带到水面形成浮渣,刮去(或撤掉)浮渣,即起到了浮选净化的作用。
回答下列问题:
(1)图中A的化学式为
(2)燃料电池正极反应为O2+2CO2+4e-=2CO
 ,负极反应式为
,负极反应式为(3)用电极反应式和离子或化学方程式说明电解池中生成Fe(OH)3的过程:
(4)若在阴极产生了2mol气体,则理论上熔融盐燃料电池消耗CH4(标准状况下)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】如图所示3套实验装置,分别回答下列问题。
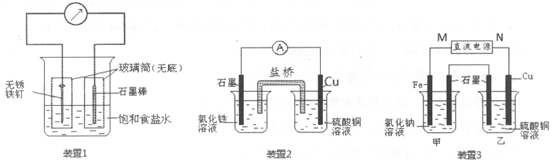
(1)装置1为铁的吸氧腐蚀实验,一段时间后,玻璃筒内的石墨电极上的电极反应式为_________ 。
(2)装置2中的石墨是_______ 极,该电极反应式为___________ 。
(3)装置3中甲烧杯盛放100mL0.2mol/L的NaCl溶液,乙烧杯盛放100mL0.5mol/L的CuSO4溶液。反应一段时间后,停止通电。向甲烧杯中滴入几滴酚酞,观察到石墨电极附近首先变红。
①电源的M端为________ 极;甲烧杯中铁电极的电极反应为_________________ 。
②乙烧杯中电解的总方程式为_______________ 。
③停止电解,取出Cu电极,洗涤、干燥、称量、电极增重0.64 g,甲烧杯中产生的气体标准状况下体积为________ mL。

(1)装置1为铁的吸氧腐蚀实验,一段时间后,玻璃筒内的石墨电极上的电极反应式为
(2)装置2中的石墨是
(3)装置3中甲烧杯盛放100mL0.2mol/L的NaCl溶液,乙烧杯盛放100mL0.5mol/L的CuSO4溶液。反应一段时间后,停止通电。向甲烧杯中滴入几滴酚酞,观察到石墨电极附近首先变红。
①电源的M端为
②乙烧杯中电解的总方程式为
③停止电解,取出Cu电极,洗涤、干燥、称量、电极增重0.64 g,甲烧杯中产生的气体标准状况下体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】观察下图A、B、C三个装置,回答下列问题:

(1)把一块纯净的锌片插入装有稀硫酸的烧杯中,可观察到锌片上有气泡,再平行插入一碳棒,可观察到碳棒上________ (填“有”或“没有”)气泡产生。用导线把锌片和碳棒连接起来组成一个原电池(图A),正极的反应式为_______________ 。
(2)如果烧杯中最初装入的是500 mL 2 mol/L硫酸溶液,构成铜锌原电池(图B,假设产生的气体没有损失),当收集到11.2 L(标准状况下)H2时,溶液体积变化忽略不计,则烧杯内硫酸的物质的量浓度为________ 。
(3)如果电极材料分别是铁片和石墨并进行连接,插入氯化钠溶液中(图C),放置数天后,铁片生锈;负极的反应式为_______________ 。

(1)把一块纯净的锌片插入装有稀硫酸的烧杯中,可观察到锌片上有气泡,再平行插入一碳棒,可观察到碳棒上
(2)如果烧杯中最初装入的是500 mL 2 mol/L硫酸溶液,构成铜锌原电池(图B,假设产生的气体没有损失),当收集到11.2 L(标准状况下)H2时,溶液体积变化忽略不计,则烧杯内硫酸的物质的量浓度为
(3)如果电极材料分别是铁片和石墨并进行连接,插入氯化钠溶液中(图C),放置数天后,铁片生锈;负极的反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】铜与稀硫酸不反应,某校实验小组的同学在老师的指导下设计了下列装置,实现了铜与稀硫酸的反应。请回答下列问题:

(1)甲同学认为在通入空气的同时,将开关K与_______ (填“a”或“b”)连接,即可实现。则此时石墨电极的反应式为_______ ,电池工作时,H+向_______ (填“C”或“Cu”)极移动。
(2)乙同学认为,不通入空气,将K与_______ (填“a”或“b”连接,也可以实现,总反应的离子方程式为_______ 。
(3)丙同学认为还可以用如图所示装置模拟工业上电镀铜。他认为只要将C换成Fe(Cu足量),并将乙同学的实验持续足够长时间,即可实现在Fe上镀Cu。这种方法得到的铜镀层不牢固,理由是_______ 。

(1)甲同学认为在通入空气的同时,将开关K与
(2)乙同学认为,不通入空气,将K与
(3)丙同学认为还可以用如图所示装置模拟工业上电镀铜。他认为只要将C换成Fe(Cu足量),并将乙同学的实验持续足够长时间,即可实现在Fe上镀Cu。这种方法得到的铜镀层不牢固,理由是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】氢氧燃料电池是符合绿色化学理念的新型发电装置。下图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定。

(1)氢氧燃料电池的能量转化形式主要是___________ ,在导线中电子流动方向为_____ (用a、b 和箭头表示)。
(2)负极反应式为______________________________________ 。
(3)电极表面镀铂粉的原因为____________________________________________________ 。
(4)氢气的制备和存储是氢氧燃料电池能否有效推广的关键技术。有人提出利用光伏发电装置电解尿素的碱性溶液来制备氢气。光伏发电是当今世界利用太阳能最主要方式之一。图1为光伏并网发电装置,图2为电解尿素[CO(NH2)2](C为+4价)的碱性溶液制氢的装置示意图(电解池中隔膜仅阻止气体通过,阴、阳极均为惰性电极)。


① 图1中N型半导体为________ (填“正极”或“负极”)
② 该系统工作时,A极的电极反应式为____________________ 。
③ 若A极产生7.00g N2,则此时B极产生________ L H2(标准状况下)。

(1)氢氧燃料电池的能量转化形式主要是
(2)负极反应式为
(3)电极表面镀铂粉的原因为
(4)氢气的制备和存储是氢氧燃料电池能否有效推广的关键技术。有人提出利用光伏发电装置电解尿素的碱性溶液来制备氢气。光伏发电是当今世界利用太阳能最主要方式之一。图1为光伏并网发电装置,图2为电解尿素[CO(NH2)2](C为+4价)的碱性溶液制氢的装置示意图(电解池中隔膜仅阻止气体通过,阴、阳极均为惰性电极)。


① 图1中N型半导体为
② 该系统工作时,A极的电极反应式为
③ 若A极产生7.00g N2,则此时B极产生
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】Ⅰ.如图所示,某同学设计了一个燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。请按要求回答相关问题:

(1)甲是燃料电池,通入甲烷的电极作___________ 极(填入“正”或“负”),其电极反应式为___________ 。
(2)乙是___________ 池(填“原电池”或“电解池”),乙装置发生电解的总反应离子方程式为:___________ 。
(3)丙中粗铜作___________ 极(填入“阴”或“阳”),若在标准状况下,有2.24L氧气参加反应,丙装置中析出精铜的质量为___________ g。
(4)若将乙装置中铁电极与石墨电极位置互换,其他装置不变,此时乙装置中发生的总反应化学方程式为___________ 。
Ⅱ.工业处理的酸性工业废水常用以下方法:
(5)将含 的废水通入电解池内,用铁作电极,电解时的电极反应,阳极反应为:
的废水通入电解池内,用铁作电极,电解时的电极反应,阳极反应为:___________ ;在酸性环境中,加入适量的NaCl进行电解, 转变为
转变为 的离子方程式为
的离子方程式为___________ 。

(1)甲是燃料电池,通入甲烷的电极作
(2)乙是
(3)丙中粗铜作
(4)若将乙装置中铁电极与石墨电极位置互换,其他装置不变,此时乙装置中发生的总反应化学方程式为
Ⅱ.工业处理的酸性工业废水常用以下方法:
(5)将含
 的废水通入电解池内,用铁作电极,电解时的电极反应,阳极反应为:
的废水通入电解池内,用铁作电极,电解时的电极反应,阳极反应为: 转变为
转变为 的离子方程式为
的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】下图是一个化学过程的示意图。已知甲池的总反应式为:2CH3OH+3O2+4KOH= 2K2CO3+6H2O
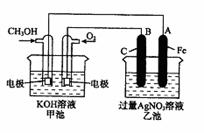
(1)乙池是__________ 装置。
(2)通入CH3OH的电极名称是______________________
(3)通入O2的电极的电极反应式是__________________________ 。若甲池用熔融碳酸盐为电解质,则通入O2的电极的电极反应式为___________________ 。
(4)乙池中反应的化学方程式为_______________________________ 。
(5)当乙池中A(Fe)极的质量增加5.40g时,甲池中理论上消耗O2_________ mL(标准状况下)

(1)乙池是
(2)通入CH3OH的电极名称是
(3)通入O2的电极的电极反应式是
(4)乙池中反应的化学方程式为
(5)当乙池中A(Fe)极的质量增加5.40g时,甲池中理论上消耗O2
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】CuSO4溶液是中学化学及工农业生产中常见的一种试剂。
(1)某同学配制CuSO4溶液时,向盛有一定量硫酸铜晶体的烧杯中加入适量的蒸馏水,并不断搅拌,结果得到悬浊液。他认为是固体没有完全溶解,于是对悬浊液加热,结果发现浑浊更明显了。原因是(用离子方程式和简要文字说明表示)___________________________ ,最后,他向烧杯中加入了一定量的_________________ 溶液,得到了澄清的CuSO4溶液。
(2)该同学利用制得的CuSO4溶液,进行了以下实验探究。
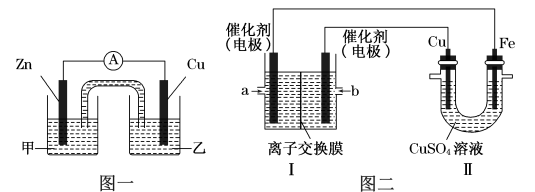
①图一是根据反应Zn+CuSO4═Cu+ZnSO4设计成的锌铜原电池。电解质溶液乙是______ 溶液,Cu极的电极反应式是____________________ 。
②图二中,Ⅰ是甲烷燃料电池(电解质溶液为NaOH溶液)的结构示意图,该同学想在Ⅱ中实现铁上镀铜,则Fe电极为__________ (填“阳极”或“阴极”)。若铜电极的质量减轻3.2 g,则消耗的CH4在标准状况下的体积为___________ L。

(1)某同学配制CuSO4溶液时,向盛有一定量硫酸铜晶体的烧杯中加入适量的蒸馏水,并不断搅拌,结果得到悬浊液。他认为是固体没有完全溶解,于是对悬浊液加热,结果发现浑浊更明显了。原因是(用离子方程式和简要文字说明表示)
(2)该同学利用制得的CuSO4溶液,进行了以下实验探究。
①图一是根据反应Zn+CuSO4═Cu+ZnSO4设计成的锌铜原电池。电解质溶液乙是
②图二中,Ⅰ是甲烷燃料电池(电解质溶液为NaOH溶液)的结构示意图,该同学想在Ⅱ中实现铁上镀铜,则Fe电极为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】回答下列问题:
(1)磷酸铁锂(LiFePO4)电极材料主要用于各种锂离子电池,回答下列问题。
①Fe位于元素周期表中第____ 周期____ 族,其价电子排布式为____ 。
②用“>”“<”成“=”填空:离子半径:Li+____ H-;第一电离能:Li____ Be;电负性:O____ P。
(2)铝灰是炼铝厂的废渣,主要含有Al2O3、Al、AlN等物质,工业上常用酸溶铝灰来制取氯化铝及聚合氯化铝,从而变废为宝、保护环境。实验室取适量铝灰于反应容器中,恒温水浴预热,加入盐酸,磁力搅拌并控制搅拌速度,用氨气吸收装置吸收氨气。
①AlN与盐酸充分反应的化学方程式为____ 。
②铝灰中铝含量测定:取10.0g铝灰样品,置于反应容器中,恒温水浴预热,加入盐酸充分反应,冷却过滤,取滤液配成100mL溶液,取出20.00mL溶液,加入0.2000mol·L-1EDTA—(Na2H2Y)溶液30.00mL,调节溶液pH为3~4,煮沸,冷却后用0.1000mol·L-1ZnSO4标准溶液滴定过量的EDTA至终点,平行滴定3次,平均消耗ZnSO4标准溶液20.00mL(已知Al3+、Zn2+与EDTA反应的化学计量比均为1∶1)。计算铝灰样品中铝的质量____ 。
③无水氯化铝常用熔融盐电镀铝工艺中,在熔融的AlCl3、NaCl、KCl盐中存在着AlCl 、Al2O
、Al2O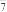 、Na+、K+和Cl-离子。
、Na+、K+和Cl-离子。
a.电镀时阴极的电极反应式为____ 。
b.已知Al2Cl6的结构式为 ,写出Al2O
,写出Al2O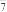 的结构式:
的结构式:____ 。
(1)磷酸铁锂(LiFePO4)电极材料主要用于各种锂离子电池,回答下列问题。
①Fe位于元素周期表中第
②用“>”“<”成“=”填空:离子半径:Li+
(2)铝灰是炼铝厂的废渣,主要含有Al2O3、Al、AlN等物质,工业上常用酸溶铝灰来制取氯化铝及聚合氯化铝,从而变废为宝、保护环境。实验室取适量铝灰于反应容器中,恒温水浴预热,加入盐酸,磁力搅拌并控制搅拌速度,用氨气吸收装置吸收氨气。
①AlN与盐酸充分反应的化学方程式为
②铝灰中铝含量测定:取10.0g铝灰样品,置于反应容器中,恒温水浴预热,加入盐酸充分反应,冷却过滤,取滤液配成100mL溶液,取出20.00mL溶液,加入0.2000mol·L-1EDTA—(Na2H2Y)溶液30.00mL,调节溶液pH为3~4,煮沸,冷却后用0.1000mol·L-1ZnSO4标准溶液滴定过量的EDTA至终点,平行滴定3次,平均消耗ZnSO4标准溶液20.00mL(已知Al3+、Zn2+与EDTA反应的化学计量比均为1∶1)。计算铝灰样品中铝的质量
③无水氯化铝常用熔融盐电镀铝工艺中,在熔融的AlCl3、NaCl、KCl盐中存在着AlCl
 、Al2O
、Al2O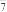 、Na+、K+和Cl-离子。
、Na+、K+和Cl-离子。a.电镀时阴极的电极反应式为
b.已知Al2Cl6的结构式为
 ,写出Al2O
,写出Al2O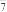 的结构式:
的结构式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】回答下列问题:
(1)目前科学家利用生物燃料电池原理(电池工作时MV2+/MV+在电极与酶之间传递电子),研究室温下合成氨并取得初步成果,示意图如图:
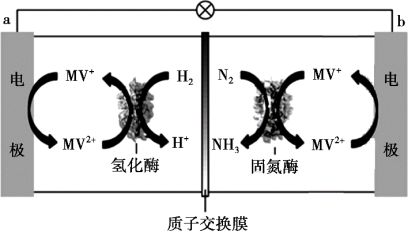
①氢化酶区域所发生反应的离子方程式为____ 。
②整个b电极区域所发生的总反应的离子方程式为____ 。
③相比传统工业合成氨,该方法的优点有____ 。
(2)若用如图所示生物燃料电池作甲装置的电源,并将甲装置中产生的CH4气体通入乙装置中,发生转化的过程如图:
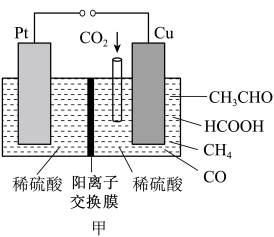
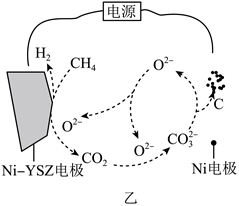
①甲装置中Pt电极应连接生物燃料电池的___ 电极(填“a”或“b”)。电解一段时间后,甲装置阳极区c(H+)____ (填“增大”“减小”或“不变”)。
②乙装置中Ni—YSZ电极上的反应为:CH4-4e-+2O2-=CO2+2H2,且整个过程中消耗的O2-和产生的O2-总数目相等。则在Ni—YSZ电极上消耗的O2-与CO2消耗的O2-数目之比为____ 。
③若开始电解一段时间后,甲装置中铜电极上只生成6.4gCH4,则甲装置铜极区溶液质量变化了____ g,乙装置中理论上生成碳的质量为___ g,生物燃料电池中理论上合成氨的质量为___ g(保留到小数点后两位)。
(1)目前科学家利用生物燃料电池原理(电池工作时MV2+/MV+在电极与酶之间传递电子),研究室温下合成氨并取得初步成果,示意图如图:

①氢化酶区域所发生反应的离子方程式为
②整个b电极区域所发生的总反应的离子方程式为
③相比传统工业合成氨,该方法的优点有
(2)若用如图所示生物燃料电池作甲装置的电源,并将甲装置中产生的CH4气体通入乙装置中,发生转化的过程如图:


①甲装置中Pt电极应连接生物燃料电池的
②乙装置中Ni—YSZ电极上的反应为:CH4-4e-+2O2-=CO2+2H2,且整个过程中消耗的O2-和产生的O2-总数目相等。则在Ni—YSZ电极上消耗的O2-与CO2消耗的O2-数目之比为
③若开始电解一段时间后,甲装置中铜电极上只生成6.4gCH4,则甲装置铜极区溶液质量变化了
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】有下图所示装置:
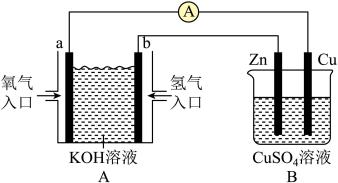
(1)装置A中b的电极名称为________ 极,a电极反应式为___________________________________ ;
(2)B装置中Cu为________ 极,电极反应式为___________________________________ ;
(3)当铜片的质量变化为12.8g时,a极上消耗的O2在标准状况下的体积为______________ L。

(1)装置A中b的电极名称为
(2)B装置中Cu为
(3)当铜片的质量变化为12.8g时,a极上消耗的O2在标准状况下的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】认真观察下列装置,回答下列问题:

(1)装置B中PbO2上发生的电极反应方程式为__________________ 。
(2)装置A中总反应的离子方程式为____________________________ 。
(3)装置D中总反应的离子方程式为_____________________________ 。
(4)若装置E的目的是在Cu材料上镀银,则X为________ ,极板N的材料为__________ 。
(5)当装置A中Cu电极质量改变6.4 g时,装置D中产生的气体体积为____ L(标准状况下)。

(1)装置B中PbO2上发生的电极反应方程式为
(2)装置A中总反应的离子方程式为
(3)装置D中总反应的离子方程式为
(4)若装置E的目的是在Cu材料上镀银,则X为
(5)当装置A中Cu电极质量改变6.4 g时,装置D中产生的气体体积为
您最近一年使用:0次



