镁燃料电池以镁合金作为电池的一极,另一极充入过氧化氢,电解质溶液是酸化的氯化钠溶液,放电时总反应为Mg+2H++H2O2=Mg2++2H2O。关于该电池说法正确的是
| A.镁合金作为电池的负极,发生还原反应 |
| B.放电时H2O2在正极得电子,被还原 |
| C.负极反应式为:Mg-2e-=Mg2+ |
| D.放电时正极附近溶液酸性增强 |
9-10高一下·广东·期末 查看更多[2]
更新时间:2016-12-09 00:46:02
|
相似题推荐
多选题
|
容易
(0.94)
【推荐1】由Cu、Zn和稀硫酸构成的原电池装置如图所示。下列叙述错误的是
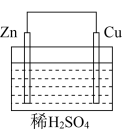

| A.Zn电极为负极 | B.Cu电极发生还原反应 |
C.电子流向:Zn电极→稀 →Cu电极 →Cu电极 | D.工作一段时间后,电解质溶液的pH减小 |
您最近一年使用:0次
多选题
|
容易
(0.94)
名校
解题方法
【推荐2】铜锌原电池装置如图,下列说法正确的是
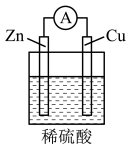

| A.锌片逐渐溶解 | B.氢离子在铜片表面被氧化 |
| C.电流从锌片经导线流向铜片 | D.该装置将化学能转化为电能 |
您最近一年使用:0次
多选题
|
容易
(0.94)
名校
解题方法
【推荐1】某原电池装置如图所示,下列说法正确的是


A.外电流的方向是从Zn→外电路→Cu |
| B.Cu棒的质量逐渐增大 |
| C.Zn棒处的电极反应式:Zn—2e-=Zn2+ |
| D.溶液中的Cu2+向负极移动 |
您最近一年使用:0次




