今有下列两组单质,试将每组单质从不同角度进行“分类”,每种“分类”都可分别挑出一种单质,它跟其他三种单质属于不同的“类”,将挑出的单质(写化学符号)和挑选依据(写编码)列在下面相应的表格内:
两组单质为:Ⅰ.O2、F2、S、N2 Ⅱ.Fe、Na、Al、Si
“挑选依据”仅限于下述六种。该被挑出的单质跟其他三种单质不同,是由于:
A.其组成元素不属于金属(或非金属); B.其组成元素不属于周期表中的同一族;C.其组成元素不属于周期表中的同一周期; D.其组成元素不属于主族(或副族)元素;(E)在常温常压下呈不同物态;(F)在常温下遇水能(或不能)迅速产生气体。
两组单质为:Ⅰ.O2、F2、S、N2 Ⅱ.Fe、Na、Al、Si
“挑选依据”仅限于下述六种。该被挑出的单质跟其他三种单质不同,是由于:
A.其组成元素不属于金属(或非金属); B.其组成元素不属于周期表中的同一族;C.其组成元素不属于周期表中的同一周期; D.其组成元素不属于主族(或副族)元素;(E)在常温常压下呈不同物态;(F)在常温下遇水能(或不能)迅速产生气体。
| 答案1 | 答案2 | 答案3 | 答案4 | 答案5 | 答案6 | |
| 单质 | Si | |||||
| 挑选理由 | A |
9-10高一下·西藏拉萨·期末 查看更多[1]
(已下线)2010年西藏拉萨中学高一第二学期期末考试化学试题
更新时间:2010-08-27 10:55:35
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】食品包装袋中有一个小纸袋,上面写着“石灰干燥剂”。
(1)“石灰干燥剂”的主要成分生石灰是________ (填化学式),“生石灰”所属的物质类型是________ (填序号)。
①金属氧化物;②碱性氧化物;③碱;④碱性干燥剂;⑤化合物;⑥盐
(2)生石灰可做干燥剂的理由是___________________________ (用化学方程式表示)。
(3)你认为下列内容还必须在这种小纸袋上注明的是________ (填序号)。
①禁止食用;②可以食用;③禁止未成年人用手拿;④生产日期
(4)小纸袋中的物质能否长期做干燥剂?为什么?_____________________ 。
(5)某同学将浓硫酸、氢氧化钠固体、生石灰等物质划分为一类。该同学的分类依据为________ (填字母)。
A.酸类 B.碱类 C.氧化物 D.干燥剂
(1)“石灰干燥剂”的主要成分生石灰是
①金属氧化物;②碱性氧化物;③碱;④碱性干燥剂;⑤化合物;⑥盐
(2)生石灰可做干燥剂的理由是
(3)你认为下列内容还必须在这种小纸袋上注明的是
①禁止食用;②可以食用;③禁止未成年人用手拿;④生产日期
(4)小纸袋中的物质能否长期做干燥剂?为什么?
(5)某同学将浓硫酸、氢氧化钠固体、生石灰等物质划分为一类。该同学的分类依据为
A.酸类 B.碱类 C.氧化物 D.干燥剂
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
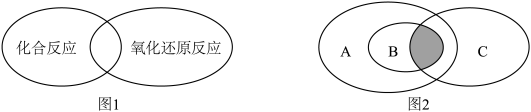
【推荐2】(1)人们常用图示法表示不同反应类型之间的关系,如化合反应和氧化还原反应的关系可用图1表示。图2为离子反应、氧化还原反应和置换反应三者之间的关系,则表示置换反应的是_______ (填字母),请写出符合图2阴影部分的一个离子方程式_______ 。
(2)胃液中含有盐酸(HCl),服用适量的小苏打(NaHCO3),能治疗胃酸过多,请写出其反应的离子方程式是_______ ;两者反应会产生CO2,实验室中常用澄清石灰水检验CO2,产生白色沉淀,反应的离子方程式是_______ 。如果病人同时患胃溃疡,不能服用小苏打,此时最好服用含氢氧化铝(Al(OH)3)的胃药(如胃舒平),反应的离子方程式为_______ 。
(3)现有失去标签的四瓶无色溶液A,B,C,D,只知道它们是K2CO3、K2SO4、NaHSO4、Ba(NO3)2,为鉴别它们,进行如下实验:
Ⅰ.A+D→溶液+气体
Ⅱ.B+C→溶液+沉淀
Ⅲ.B+D→溶液+沉淀
Ⅳ.A+B→溶液+沉淀
Ⅴ.将Ⅳ得到的沉淀物加入Ⅲ所得的溶液中,沉淀很快溶解并产生无色无味的气体。根据以上实验事实,请完成如下问题。
①写出实验Ⅰ中反应中相关的离子方程式_______ 。
②写出实验Ⅱ中反应中相关的离子方程式_______ 。

(2)胃液中含有盐酸(HCl),服用适量的小苏打(NaHCO3),能治疗胃酸过多,请写出其反应的离子方程式是
(3)现有失去标签的四瓶无色溶液A,B,C,D,只知道它们是K2CO3、K2SO4、NaHSO4、Ba(NO3)2,为鉴别它们,进行如下实验:
Ⅰ.A+D→溶液+气体
Ⅱ.B+C→溶液+沉淀
Ⅲ.B+D→溶液+沉淀
Ⅳ.A+B→溶液+沉淀
Ⅴ.将Ⅳ得到的沉淀物加入Ⅲ所得的溶液中,沉淀很快溶解并产生无色无味的气体。根据以上实验事实,请完成如下问题。
①写出实验Ⅰ中反应中相关的离子方程式
②写出实验Ⅱ中反应中相关的离子方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】分类是学习化学的重要方法,从物质的元素组成和化学性质视角对物质进行科学分类,可体现化学学科独有的魅力。
回答下列问题:
(1)现有下列物质:①铜 ② ③
③ ④
④ ⑤酒精 ⑥氨水 ⑦稀硫酸 ⑧
⑤酒精 ⑥氨水 ⑦稀硫酸 ⑧ 以上物质中,属于电解质的是
以上物质中,属于电解质的是_______ (填序号);向②的溶液中滴加③的溶液至恰好沉淀完全,离子反应方程式为_______ ,此过程中溶液的导电能力_______ (填“增强”、“减弱”或“不变”)。
(2)通过对物质进行分类,能够根据类别通性预测物质的性质。
已知 属于酸性氧化物,则
属于酸性氧化物,则 与
与 溶液反应的化学方程式为
溶液反应的化学方程式为_______ ;亚磷酸 是二元弱酸,它与足量
是二元弱酸,它与足量 溶液充分反应后生成的盐为
溶液充分反应后生成的盐为_______ (填化学式),该盐属于_______ (填“正盐”或“酸式盐”)。
回答下列问题:
(1)现有下列物质:①铜 ②
 ③
③ ④
④ ⑤酒精 ⑥氨水 ⑦稀硫酸 ⑧
⑤酒精 ⑥氨水 ⑦稀硫酸 ⑧ 以上物质中,属于电解质的是
以上物质中,属于电解质的是(2)通过对物质进行分类,能够根据类别通性预测物质的性质。
已知
 属于酸性氧化物,则
属于酸性氧化物,则 与
与 溶液反应的化学方程式为
溶液反应的化学方程式为 是二元弱酸,它与足量
是二元弱酸,它与足量 溶液充分反应后生成的盐为
溶液充分反应后生成的盐为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】酸式盐是盐的一种,可看作是多元酸中的氢离子未被完全中和所得到的盐,常见的有NaHCO3、NaHSO4、KH2PO4、K2HPO4等。已知H3PO2(次磷酸)与足量的NaOH反应只生成一种盐NaH2PO2,H3PO2水溶液中存在H3PO2分子。
(1)H3PO2属于___________ 酸;NaH2PO2为___________ 盐(填序号)
①一元酸,②二元酸,③三元酸,④强酸,⑤弱酸,⑥正盐,⑦酸式盐
(2)写出H3PO2溶液与足量NaOH溶液反应的离子方程式___________ 。
(1)H3PO2属于
①一元酸,②二元酸,③三元酸,④强酸,⑤弱酸,⑥正盐,⑦酸式盐
(2)写出H3PO2溶液与足量NaOH溶液反应的离子方程式
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】分类是学习和研究化学物质及其变化的一种常用的科学方法,回答下列问题:
(1)实验室常根据物质分类的原则存放药品,某学校实验室中的四个药品柜已经存放了如下部分药品,硫酸钠应放在___________ (填选项字母,下同);晶体碘应放在___________ 。
(2)现有碳、一氧化碳、二氧化碳、碳酸钠四种物质,采用下列分类标准,无法将其中两种物质归为一类的是___________ (填选项字母)。
a.具有还原性 b.属于氧化物 c.属于电解质 d.碳元素化合价相同
(3)写出下列离子方程式对应的一个化学方程式。
 :
:___________ ;
 :
:___________ ;
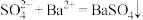 :
:___________ 。
(1)实验室常根据物质分类的原则存放药品,某学校实验室中的四个药品柜已经存放了如下部分药品,硫酸钠应放在
| 药品柜 | a.甲柜 | b.乙柜 | c.丙柜 | d.丁柜 |
| 药品 | 乙醇、乙酸 | 活性炭、红磷 | 锌粒、铜片 | 氯化钠、氯化钾 |
a.具有还原性 b.属于氧化物 c.属于电解质 d.碳元素化合价相同
(3)写出下列离子方程式对应的一个化学方程式。
 :
: :
: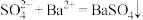 :
:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】宏观和微观相结合是认识物质结构与性质的重要方法,请回答下列问题。
(1)氧原子的结构示意图为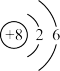 ,硫原子的结构示意图为
,硫原子的结构示意图为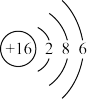 。
。
①一个硫原子得到二个电子形成一种新粒子,该粒子的符号为___________ 。
②氧气和硫单质分别与氢气反应生成 和
和 。
。 、
、 中氧与硫元素的化合价均为
中氧与硫元素的化合价均为 价,从原子结构上分析它们化合价相同的原因是
价,从原子结构上分析它们化合价相同的原因是___________ 。
(2) 溶液和
溶液和 溶液反应的微观示意图如图1所示。该反应中实际参加反应的离子是
溶液反应的微观示意图如图1所示。该反应中实际参加反应的离子是___________ (填离子符号)。
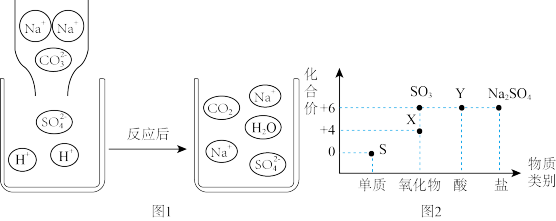
(3)硫及其化合物的“化合价-物质类别”关系图如图2所示。物质X的化学式为___________ 。
(1)氧原子的结构示意图为
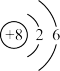 ,硫原子的结构示意图为
,硫原子的结构示意图为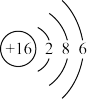 。
。①一个硫原子得到二个电子形成一种新粒子,该粒子的符号为
②氧气和硫单质分别与氢气反应生成
 和
和 。
。 、
、 中氧与硫元素的化合价均为
中氧与硫元素的化合价均为 价,从原子结构上分析它们化合价相同的原因是
价,从原子结构上分析它们化合价相同的原因是(2)
 溶液和
溶液和 溶液反应的微观示意图如图1所示。该反应中实际参加反应的离子是
溶液反应的微观示意图如图1所示。该反应中实际参加反应的离子是
(3)硫及其化合物的“化合价-物质类别”关系图如图2所示。物质X的化学式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】如表是某城市场上销售的一种“加碘盐”包装上的部分文字说明。
回答下列问题:
(1)结合物质分类中的树状分类法,根据物质的组成对物质进行分类。在下列五种___ (填“混合物”“化合物”“盐”或“氧化物”)中与碘酸钾(KIO3)属于同类物质的是__ (填序号)。
①HIO3②NaIO3③KOH④I2O5⑤NaCl
(2)推测碘酸钾(KIO3)的物理性质:碘酸钾(KIO3)___ (填“能”或“不能”)溶于水;化学性质:碘酸钾(KIO3)在受热时___ (填“易分解”或“不易分解”)。
| 配料表 | 精制海盐、碘酸钾(KIO3) |
| 含碘量 | 20~40mg·kg-1 |
| 储藏方法 | 密封、避光、防潮 |
| 食用方法 | 烹调时待食品熟后加入碘盐 |
回答下列问题:
(1)结合物质分类中的树状分类法,根据物质的组成对物质进行分类。在下列五种
①HIO3②NaIO3③KOH④I2O5⑤NaCl
(2)推测碘酸钾(KIO3)的物理性质:碘酸钾(KIO3)
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】按要求完成下列各题
(1)按照物质的树状分类和交叉分类,HNO3应属于_____ (填字母代号)。
①酸 ②氢化物 ③氧化物 ④含氧酸 ⑤难挥发性酸 ⑥化合物 ⑦一元酸
A. ①②③④⑤⑥⑦ B. ①④⑥⑦ C. ①③⑤⑥ D. ①④⑤⑥⑦
(2)现有以下物质:①NaCl晶体、 ②液态HCl、 ③CaCO3固体、 ④熔融KCl、⑤蔗糖、 ⑥铜、 ⑦CO2、 ⑧H2SO4。
其中:属于电解质的是____ ,属于非电解质的是____ 。
(3)Fe(OH)3胶体呈红褐色,插入两个惰性电极,通直流电一段时间,阴极附近的颜色逐渐变深,这种现象叫_____ ;光束通过Fe(OH)3胶体,可看到明亮的通路,这种现象叫_____ ;向Fe(OH)3胶体中逐滴加入稀盐酸,刚开始有红褐色沉淀生成,这是因为____ ,然后红褐色沉淀又逐渐溶解,原因是___ (用离子方程式解释)。
(1)按照物质的树状分类和交叉分类,HNO3应属于
①酸 ②氢化物 ③氧化物 ④含氧酸 ⑤难挥发性酸 ⑥化合物 ⑦一元酸
A. ①②③④⑤⑥⑦ B. ①④⑥⑦ C. ①③⑤⑥ D. ①④⑤⑥⑦
(2)现有以下物质:①NaCl晶体、 ②液态HCl、 ③CaCO3固体、 ④熔融KCl、⑤蔗糖、 ⑥铜、 ⑦CO2、 ⑧H2SO4。
其中:属于电解质的是
(3)Fe(OH)3胶体呈红褐色,插入两个惰性电极,通直流电一段时间,阴极附近的颜色逐渐变深,这种现象叫
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】无机化合物可根据其组成和性质进行分类。
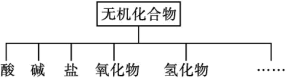
(1)上图所示的物质的分类方法的名称是___________ 。
(2)从H、C、N、O、Na、S中任选两种或三种元素组成合适的物质,填表。
(3)写出⑧转化为⑤的化学方程式:___________ 。
(4)实验室制备⑦常用___________ (填名称)与①的水溶液反应,并用④的水溶液检验该气体。写出检验该气体时反应的离子方程式:___________ 。

(1)上图所示的物质的分类方法的名称是
(2)从H、C、N、O、Na、S中任选两种或三种元素组成合适的物质,填表。
| 物质类别 | 酸 | 碱 | 盐 | 氧化物 | 氢化物 |
| 化学式 | ①HCl ② | ③ ④Ca(OH)2 | ⑤Na2CO3 ⑥ | ⑦CO2 ⑧Na2O | ⑨NH3 ⑩H2O2 |
(3)写出⑧转化为⑤的化学方程式:
(4)实验室制备⑦常用
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】元素在周期表中的位置,反映了元素的原子结构和元素的性质,右图是元素周期表的一部分。
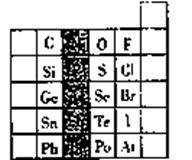
(1)阴影部分元素在元素周期表中的位置为第_________ 族。根据元素周期律、预测;酸性强弱H3AsO4______ H3PO4(用“>”或“<”表示)
(2)元素S的最高正价和最低负价的代数和为________ ,在一定条件下,S与H2反应有一定限度(可理解为反应进行的程度)。请判断:在相同条件下Se与H2反应的限度比S与H2反应限度____________ 。(选填“更大”、“更小”或“相同”)
(3)Br2具有较强的氧化性,SO2具有较强的还原性,将SO2气体通入溴水后,溶液中存在的主要离子是__________
(4)下列说法正确的是__________
A.C、N、O、F的原子半径随着原子数的增大而减小
B.Si、P、S、Cl元素的非金属性随着核电荷数的增加而增强
C.干冰升华、液态水转变为气态都要克服分子内的共价键
D.HF、HCl、HBr、HI的热稳定性依次减弱

(1)阴影部分元素在元素周期表中的位置为第
(2)元素S的最高正价和最低负价的代数和为
(3)Br2具有较强的氧化性,SO2具有较强的还原性,将SO2气体通入溴水后,溶液中存在的主要离子是
(4)下列说法正确的是
A.C、N、O、F的原子半径随着原子数的增大而减小
B.Si、P、S、Cl元素的非金属性随着核电荷数的增加而增强
C.干冰升华、液态水转变为气态都要克服分子内的共价键
D.HF、HCl、HBr、HI的热稳定性依次减弱
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】元素周期表有____ 个横行,叫周期,每一周期中元素原子的_________ 相同,从左到右元素的金属性____ (填增强或减弱);元素周期表中有_____ 列,第ⅥA族处在第_____ 列,同一主族从上到下,元素的非金属性依次_______ (填增强或减弱)。
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】在下列各元素组中,除一种元素外,其余都可以按照某种共性归属为一类,请选出各组的例外元素,并将该组其他元素的可能归属按所给六种类型的编号填入表中。其他元素可能归属类型:①主族元素;②过渡元素;③同周期元素;④同主族元素;⑤金属元素;⑥非金属元素。
| 元素组 | 元素组的例外元素 | 其他元素所属类型编号 |
| (1)S、Na、Mg、N | ||
| (2)N、P、Sn、As | ||
| (3)K、Ca、Al、Zn | ||
| (4)Cu、Fe、Ag、Ca |
您最近一年使用:0次



