元素在周期表中的位置,反映了元素的原子结构和元素的性质,右图是元素周期表的一部分。
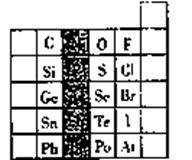
(1)阴影部分元素在元素周期表中的位置为第_________ 族。根据元素周期律、预测;酸性强弱H3AsO4______ H3PO4(用“>”或“<”表示)
(2)元素S的最高正价和最低负价的代数和为________ ,在一定条件下,S与H2反应有一定限度(可理解为反应进行的程度)。请判断:在相同条件下Se与H2反应的限度比S与H2反应限度____________ 。(选填“更大”、“更小”或“相同”)
(3)Br2具有较强的氧化性,SO2具有较强的还原性,将SO2气体通入溴水后,溶液中存在的主要离子是__________
(4)下列说法正确的是__________
A.C、N、O、F的原子半径随着原子数的增大而减小
B.Si、P、S、Cl元素的非金属性随着核电荷数的增加而增强
C.干冰升华、液态水转变为气态都要克服分子内的共价键
D.HF、HCl、HBr、HI的热稳定性依次减弱

(1)阴影部分元素在元素周期表中的位置为第
(2)元素S的最高正价和最低负价的代数和为
(3)Br2具有较强的氧化性,SO2具有较强的还原性,将SO2气体通入溴水后,溶液中存在的主要离子是
(4)下列说法正确的是
A.C、N、O、F的原子半径随着原子数的增大而减小
B.Si、P、S、Cl元素的非金属性随着核电荷数的增加而增强
C.干冰升华、液态水转变为气态都要克服分子内的共价键
D.HF、HCl、HBr、HI的热稳定性依次减弱
10-11高三上·北京·阶段练习 查看更多[2]
更新时间:2010-09-25 14:12:22
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】硫——重要的非金属元素
| 硫元素位置 | 原子结构示意图 | 非金属性 | 主要化合价 |
| 第 | 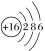 | 比氧弱 |
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】有人推测尚未合成的第114号元素有相当稳定的同位素,恰处在不稳定核素的“海洋”中浮起的一群较稳定核素的“岛屿”的中心。114号元素是第_______ 周期第_______ 族元素,它的可能氧化态_______ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】下表是元素周期表一部分,列出了九种元素在周期表中的位置:
请用化学用语回答下列问题
(1)在上述元素中,金属性最强的是____________ 。
(2)①~⑨中元素最高价氧化物对应的水化物中酸性最强的是________ (填物质化学式)。写出⑥和⑧的最高价氧化物对应的水化物反应的离子方程式 _______________________________ 。
(3)只由④形成的18电子微粒的电子式________________ 。
(4)写出由①和③形成的离子化合物的化学式____________________________ 。
(5)用电子式表示⑦和⑨形成的化合物的形成过程_________________________________ 。
(6)表中元素③和⑤可形成一种相对分子质量为66的共价化合物Y,Y分子中各原子均达到“8电子稳定结构”,Y的结构式_________________ 。
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | ⑤ | ||||
| 3 | ⑥ | ⑦ | ⑧ | ⑨ |
请用化学用语回答下列问题
(1)在上述元素中,金属性最强的是
(2)①~⑨中元素最高价氧化物对应的水化物中酸性最强的是
(3)只由④形成的18电子微粒的电子式
(4)写出由①和③形成的离子化合物的化学式
(5)用电子式表示⑦和⑨形成的化合物的形成过程
(6)表中元素③和⑤可形成一种相对分子质量为66的共价化合物Y,Y分子中各原子均达到“8电子稳定结构”,Y的结构式
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】根据元素周期表1~20号元素的性质和递变规律,回答下列问题。
(1)属于金属元素的有_____ 种,金属性最强的元素与氧反应生成的化合物为_______ (填两种化合物的化学式)。
(2)正化合价最高的元素是________ ,其最高正化合价为________ 。
(3)单质既能与HCl反应,又能与NaOH反应的是________ ,其最高价氧化物对应水化物具有________ (填“酸性”、“碱性”或“两性”)。
(4)第三周期中,原子半径最大的是(稀有气体元素除外)________ 。
(5)推测Si、N最简单氢化物的稳定性________ 大于________ 。(填化学式)
(1)属于金属元素的有
(2)正化合价最高的元素是
(3)单质既能与HCl反应,又能与NaOH反应的是
(4)第三周期中,原子半径最大的是(稀有气体元素除外)
(5)推测Si、N最简单氢化物的稳定性
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】为纪念元素周期表诞生150周年,IUPAC等向世界介绍了118位优秀青年化学家,并形成一张“青年化学家元素周期表”。中国学者雷晓光、姜雪峰、刘庄分别成为“ ,
, 、
、 ”元素的代言人。回答下列问题:
”元素的代言人。回答下列问题:
(1)根据汞的原子结构示意图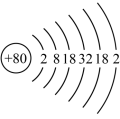 判断,汞在第
判断,汞在第___________ 周期。工业上冶炼金属汞的方法为___________ 。
(2)硒(Se)与硫位于同一主族,均是生命必需元素。下列推断不正确的是___________ 。
A.硒元素的最低负化合价为 价
价
B.还原性: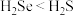
C.二氧化硒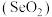 具有还原性
具有还原性
(3)氮是自然界各种生物体生命活动不可缺少的重要元素,磷(P)、砷(As)也是氮族元素。
①砷有多种同位素原子,其中稳定的核素是 ,它的中子数为
,它的中子数为___________ 。
②已知 与
与 的性质相似,则对
的性质相似,则对 性质的推测正确的是
性质的推测正确的是___________ 。
A.含有离子键和共价键
B.能与 溶液反应
溶液反应
C.加热充分分解时与 分解产物的种类完全一样
分解产物的种类完全一样
③下列关于第ⅤA族元素及其化合物的说法正确的是___________ 。
A.热稳定性:
B.As的氧化物的水化物是强碱
C.简单离子半径随原子序数递增而增大
(4)砷酸 可用于制造杀虫剂、药物等。
可用于制造杀虫剂、药物等。 溶于稀硝酸中可得砷酸,此反应的化学方程式为
溶于稀硝酸中可得砷酸,此反应的化学方程式为___________ 。
 ,
, 、
、 ”元素的代言人。回答下列问题:
”元素的代言人。回答下列问题:(1)根据汞的原子结构示意图
 判断,汞在第
判断,汞在第(2)硒(Se)与硫位于同一主族,均是生命必需元素。下列推断不正确的是
A.硒元素的最低负化合价为
 价
价B.还原性:
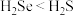
C.二氧化硒
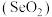 具有还原性
具有还原性(3)氮是自然界各种生物体生命活动不可缺少的重要元素,磷(P)、砷(As)也是氮族元素。
①砷有多种同位素原子,其中稳定的核素是
 ,它的中子数为
,它的中子数为②已知
 与
与 的性质相似,则对
的性质相似,则对 性质的推测正确的是
性质的推测正确的是A.含有离子键和共价键
B.能与
 溶液反应
溶液反应C.加热充分分解时与
 分解产物的种类完全一样
分解产物的种类完全一样③下列关于第ⅤA族元素及其化合物的说法正确的是
A.热稳定性:

B.As的氧化物的水化物是强碱
C.简单离子半径随原子序数递增而增大
(4)砷酸
 可用于制造杀虫剂、药物等。
可用于制造杀虫剂、药物等。 溶于稀硝酸中可得砷酸,此反应的化学方程式为
溶于稀硝酸中可得砷酸,此反应的化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】下表是ⅥA族部分元素的相关性质。
请回答下列问题:
(1)硒的熔点范围可能是_______ 。
(2)碲的化合价可能有_______ 。
(3)硫、硒、碲的氢化物水溶液的酸性由强至弱的顺序是_______ (填化学式)。
(4)氢硒酸有较强的_______ (填“氧化性”或“还原性”),因此放在空气中易变质,其可能发生的化学方程式为_______ 。
(5)工业上Al2Te3可用来制备H2Te,完成下列化学方程式:_______
_______Al2Te3+_______=2Al(OH)3↓+_______H2Te↑
| 元素 性质 | 8O | 16S | 34Se | 52Te |
| 单质熔点(℃) | -218.4 | 113 | 450 | |
| 单质沸点(℃) | -183 | 444.6 | 685 | 1390 |
| 主要化合价 | -2 | -2、+4、+6 | -2、+4、+6 | |
| 原子半径 | 逐渐增大 | |||
| 单质与H2反应情况 | 点燃时易化合 | 加热化合 | 加热难化合 | 不能直接化合 |
请回答下列问题:
(1)硒的熔点范围可能是
(2)碲的化合价可能有
(3)硫、硒、碲的氢化物水溶液的酸性由强至弱的顺序是
(4)氢硒酸有较强的
(5)工业上Al2Te3可用来制备H2Te,完成下列化学方程式:
_______Al2Te3+_______=2Al(OH)3↓+_______H2Te↑
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】元素周期表体现了元素“位—构—性”的关系,揭示了元素间的内在联系。下图是元素周期表的一部分,回答下列问题:
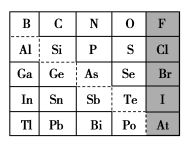
(1)元素Ga在元素周期表中的位置为:第___________ 周期第___________ 族;
(2)Sn的最高正价为___________ ,Bi的最高价氧化物为___________ ;
(3)根据元素周期律,推断:
①阴影部分元素氢化物热稳定性最强的是___________ 元素(填元素符号);
②H3AsO4、H2SeO4的酸性强弱:H3AsO4___________ (填“>”“<”或“=”)H2SeO4;
③氢化物的还原性:H2O___________ (填“>”“<”或“=”)H2S;

(1)元素Ga在元素周期表中的位置为:第
(2)Sn的最高正价为
(3)根据元素周期律,推断:
①阴影部分元素氢化物热稳定性最强的是
②H3AsO4、H2SeO4的酸性强弱:H3AsO4
③氢化物的还原性:H2O
您最近一年使用:0次



