油酸甘油酯(相对分子质量884)在体内代谢时可发生如下反应:C57H104O6(s)+80O2(g)=57CO2(g)+52H2O(l)。已知燃烧1kg该化合物释放出热量3.8×104kJ。油酸甘油酯的燃烧热△H为
| A.3.8×104kJ·mol-1 | B.-3.8×104kJ·mol-1 |
| C.3.4×104kJ·mol-1 | D.-3.4×104kJ·mol-1 |
2016·海南·高考真题 查看更多[33]
第一章 化学反应的热效应 第一节 反应热 第2课时 热化学方程式 燃烧热(已下线)第六章 化学反应与能量 第34讲 反应热的计算广西桂林市第十八中学2021-2022学年高二下学期开学考试化学试题黑龙江省哈尔滨市第一六二中学2021-2022学年高三上学期第三次月考化学试题(已下线)1.2 反应热的计算-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)(已下线)课时29 盖斯定律及反应热计算-2022年高考化学一轮复习小题多维练(全国通用)海南省八所中学2020届高三上学期期末考试化学试题广东省揭阳市第三中学2020-2021学年高二上学期期中考化学试题人教版(2019)高二选择性必修第一册 第一章 化学反应的热效应 第一节 反应热 高考帮天津市南开中学2020届高三教学质量监测理科综合化学部分2020届湖南省长沙市礼雅中学高中毕业班四月份网络教学质量监测卷理科综合化学部分河南省郑州市第一中学2020年高中毕业班教学质量监测卷理科综合化学试题安徽省定远县育才学校2019-2020学年高二4月月考化学试题(已下线)专题九 化学能与热能(真题汇编)-2020年高考二轮模块化复习之《化学基本原理》名师讲案与提分特训2020届高三化学二轮冲刺新题专练——燃烧热的定义与应用山西省大同市天镇县第一中学校2019-2020学年高二上学期第二次月考化学试题湖南省师范大学附属中学2020届高三上学期第二次月考化学试题海南省文昌中学2019-2020学年高二上学期第二次月考化学试题(已下线)2019年高考总复习巅峰冲刺-专题05 化学反应中的能量变化应试策略2016年全国普通高等学校招生统一考试化学(海南卷参考版)(已下线)考点08 化学反应中的热效应——备战2019年浙江新高考化学考点(已下线)2019高考备考二轮复习精品资料-专题8 化学反应中与能量变化(教学案)【全国百强校】山西省山西大学附属中学2018-2019学年高二上学期10月模块诊断化学试题(已下线)解密08 化学反应与热能(教师版)——备战2018年高考化学之高频考点解密(已下线)《考前20天终极攻略》-5月24日 盖斯定律及反应热的有关计算福建省泉州市泉港区第一中学2017-2018学年高二年上学期期末考化学试题安徽省合肥八中、马鞍山二中、阜阳一中2017-2018学年第一学期联考高二化学试卷湖北省新洲一中、黄陂一中、麻城一中2017-2018学年高二上学期期中联考化学试题2017届河北省沧州市第一中学高三上周测化学试卷2016-2017学年河北冀州市中学高二上开学调研化学卷2015-2016学年黑龙江哈尔滨六中高二下期末化学试卷2016年全国普通高等学校招生统一考试化学(海南卷精编版)2016-2017学年广东省仲元中学高二上学期期末考试化学(理)试卷
更新时间:2016-07-11 20:34:51
|
相似题推荐
单选题
|
较易
(0.85)
【推荐1】在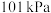 时,
时,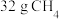 完全燃烧生成
完全燃烧生成 气体和液态水,放出的热量为
气体和液态水,放出的热量为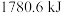 ,则
,则 的燃烧热为
的燃烧热为
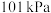 时,
时,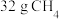 完全燃烧生成
完全燃烧生成 气体和液态水,放出的热量为
气体和液态水,放出的热量为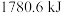 ,则
,则 的燃烧热为
的燃烧热为A.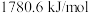 | B. |
C.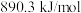 | D. |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】在燃烧1.12L(标准状况)CO与O2的混合气体时,放出5.66kJ的热量,在相同的状况下,最后产物的密度为原来气体密度的1.25倍,则CO的燃烧热为
| A.283kJ·mol-1 | B.-283kJ·mol-1 |
| C.-566kJ·mol-1 | D.566kJ·mol-1 |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐3】甲醇是一种高效清洁的新能源,0.25mol甲醇完全燃烧生成液态水时放出225kJ热量,则下列关于甲醇燃烧热的热化学方程式中正确的是
| A.2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l) ΔH=-1800 kJ·mol-1 |
B.CH3OH(l)+ O2(g)=CO2(g)+2H2O(g) ΔH=-900 kJ·mol-1 O2(g)=CO2(g)+2H2O(g) ΔH=-900 kJ·mol-1 |
C.CH3OH(l)+ O2(g)=CO2(g)+2H2O(l) ΔH=-900 kJ·mol-1 O2(g)=CO2(g)+2H2O(l) ΔH=-900 kJ·mol-1 |
| D.CH3OH(l)+3O2(g)=CO2(g)+2H2O(l) ΔH=-900 kJ·mol-1 |
您最近半年使用:0次



