18. 氢能是发展中的新能源,它的利用包括氢的制备、储存和应用三个环节。回答下列问题:
(1)已知氢气在氧气中燃烧生成3.6g液态水放热57.16kJ的热量,请写出表示氢气燃烧热的热化学方程式
___________________________;若断开H
2(g)中1molH-H需要吸收436kJ的能量,生成H
2O(g)中的1mol H-O键放出463 kJ的能量,18g液态水转化为水蒸气需要吸收44 kJ的能量,则断开1molO
2中的共价键需要吸收
___________kJ的能量。
(2)氢气直接燃烧的能量转换率远低于燃料电池,写出碱性氢氧燃料电池的正极反应式:
___(3)利用太阳能直接分解水制氢,是最具吸引力的制氢途径,其能量转化形式为
_______(4)在恒温恒容的密闭容器中,某储氢反应:MH
x(s)+yH
2(g)

MH
x+2y(s) ΔH<0达到化学平衡。下列有关叙述正确的是
________a.容器内气体压强保持不变
b. 1 mol MH
x能够吸收ymol H
2c.若降温,该反应的平衡常数增大
d.若向容器内通入少量氢气,则c(H
2)增大
(5)化工生产的副产氢也是氢气的来源。电解法制取有广泛用途的Na
2FeO
4,同时获得氢气:Fe+2H
2O+2OH
−
FeO
42−+3H
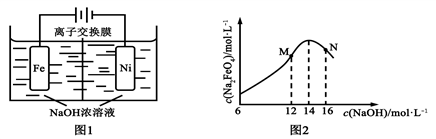
2↑,工作原理如图1所示。装置通电后,铁电极附近生成紫红色的FeO
42−,镍电极有气泡产生。若氢氧化钠溶液浓度过高,铁电极区会产生红褐色物质。已知:Na
2FeO
4只在强碱性条件下稳定,易被H
2还原。
①请写出阳极电极反应式
________________________②电解过程中,须将阴极产生的气体及时排出,其原因是
______________________③c( Na
2FeO
4)随初始c(NaOH)的变化如图2,请分析在实验中控制NaOH浓度为14mol/L的原因:
______________。