根据要求结合化学用语解释下列问题:
(1)NaHCO3溶液呈碱性的原因:__________________
(2)可用CuO除去CuCl2溶液中的FeCl3溶液的原因:_________________
(3)水垢中含有CaSO4,可先用Na2CO3溶液处理,使之转化为疏松、易溶于酸的CaCO3,而后用酸除去,请分析转化原理:_________________
(4)将密封的NO2气体加热,气体颜色变深的原因:______________________
(1)NaHCO3溶液呈碱性的原因:
(2)可用CuO除去CuCl2溶液中的FeCl3溶液的原因:
(3)水垢中含有CaSO4,可先用Na2CO3溶液处理,使之转化为疏松、易溶于酸的CaCO3,而后用酸除去,请分析转化原理:
(4)将密封的NO2气体加热,气体颜色变深的原因:
更新时间:2018-02-22 20:57:20
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】甲烷水蒸气重整制取合成气的反应如下:CH4(g)+H2O(g) CO(g)+3H2(g) ΔH=+206kJ∙mol-1。
CO(g)+3H2(g) ΔH=+206kJ∙mol-1。
请回答下列问题:
(1)上述反应能自发进行的理由是___ ,条件是___ (填“低温”、“高温”或“任何条件”)。
(2)向体积为2L的密闭容器中,按n(H2O)∶n(CH4)=1投料:
a.保持温度为T1时,测得CH4(g)的浓度随时间变化曲线如图1所示。
b.其他条件相同时,在不同催化剂(Ⅰ、Ⅱ、Ⅲ)作用下,反应相同时间后,CH4的转化率随反应温度的变化如图2所示。

①结合图1,写出反应达平衡的过程中的能量变化:吸收__ kJ(用含有x、y的代数式表示)。
②在图1中画出:起始条件相同,保持温度为T2(T2>T1)时,c(CH4)随时间的变化曲线__ 。
③根据图2判断:
ⅰ.a点所处的状态不是化学平衡状态,理由是__ 。
ⅱ.CH4的转化率:c>b,原因是___ 。
(3)①设起始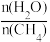 =Z,在恒压(P0)下,平衡时φ(CH4)与Z和T(温度)的关系如图3所示:(其中φ(CH4)为CH4的体积分数)
=Z,在恒压(P0)下,平衡时φ(CH4)与Z和T(温度)的关系如图3所示:(其中φ(CH4)为CH4的体积分数)

比较图3中a、b与3的大小关系____ (请按从大到小的顺序书写)。
②对于气相反应,用某组分B的平衡压强p(B)代替物质的量浓度c(B)也可表示平衡常数,记作Kp,如p(B)=px(B),p为平衡总压强,x(B)为平衡系统中B的物质的量分数。则图3中X点时,Kp=___ 。
 CO(g)+3H2(g) ΔH=+206kJ∙mol-1。
CO(g)+3H2(g) ΔH=+206kJ∙mol-1。请回答下列问题:
(1)上述反应能自发进行的理由是
(2)向体积为2L的密闭容器中,按n(H2O)∶n(CH4)=1投料:
a.保持温度为T1时,测得CH4(g)的浓度随时间变化曲线如图1所示。
b.其他条件相同时,在不同催化剂(Ⅰ、Ⅱ、Ⅲ)作用下,反应相同时间后,CH4的转化率随反应温度的变化如图2所示。

①结合图1,写出反应达平衡的过程中的能量变化:吸收
②在图1中画出:起始条件相同,保持温度为T2(T2>T1)时,c(CH4)随时间的变化曲线
③根据图2判断:
ⅰ.a点所处的状态不是化学平衡状态,理由是
ⅱ.CH4的转化率:c>b,原因是
(3)①设起始
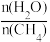 =Z,在恒压(P0)下,平衡时φ(CH4)与Z和T(温度)的关系如图3所示:(其中φ(CH4)为CH4的体积分数)
=Z,在恒压(P0)下,平衡时φ(CH4)与Z和T(温度)的关系如图3所示:(其中φ(CH4)为CH4的体积分数)
比较图3中a、b与3的大小关系
②对于气相反应,用某组分B的平衡压强p(B)代替物质的量浓度c(B)也可表示平衡常数,记作Kp,如p(B)=px(B),p为平衡总压强,x(B)为平衡系统中B的物质的量分数。则图3中X点时,Kp=
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】消除氮氧化物的污染是当前科学研究的热点,根据所学知识回答下列问题:
(1)已知①
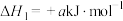 ;②
;② 的燃烧热为
的燃烧热为
 ,则反应
,则反应 的
的
_________  (用含a、b的代数式表示)。
(用含a、b的代数式表示)。
(2)已知 和
和 可以相互转化,反应
可以相互转化,反应

 。在温度一定时,平衡体系中
。在温度一定时,平衡体系中 的体积分数
的体积分数 随压强的变化情况如图所示。
随压强的变化情况如图所示。

①A、C两点的正反应速率的关系为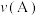
_________ (填“>”、“<”或“=”)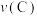 。
。
②A、B、C、D、E各状态, 的是状态
的是状态_________ 。
③E→A所需时间为x,DC所需时间为y,则x_________ (填“>”、<"或“=”)y。
(3)在一定条件下, 可还原氮氧化物,消除氮氧化物污染。工业上,常用
可还原氮氧化物,消除氮氧化物污染。工业上,常用 和
和 在催化剂作用下合成
在催化剂作用下合成 。在催化剂作用下,
。在催化剂作用下, 时,发生反应,平衡混合气中
时,发生反应,平衡混合气中 的物质的量分数随温度和压强变化的关系如图所示。
的物质的量分数随温度和压强变化的关系如图所示。
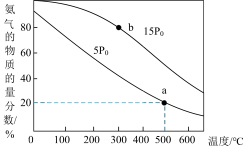
①该反应的平衡常数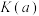
_________ (填“<”、“=”或“>”)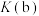 。
。
②500℃、压强为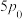 时,
时, 的转化率为
的转化率为_________ %(保留三位有效数字),
_________ 。[ 为平衡分压代替平衡浓度计算求得的平衡常数(分压=总压×物质的量分数)]
为平衡分压代替平衡浓度计算求得的平衡常数(分压=总压×物质的量分数)]
(1)已知①

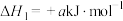 ;②
;② 的燃烧热为
的燃烧热为
 ,则反应
,则反应 的
的
 (用含a、b的代数式表示)。
(用含a、b的代数式表示)。(2)已知
 和
和 可以相互转化,反应
可以相互转化,反应

 。在温度一定时,平衡体系中
。在温度一定时,平衡体系中 的体积分数
的体积分数 随压强的变化情况如图所示。
随压强的变化情况如图所示。
①A、C两点的正反应速率的关系为
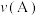
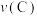 。
。②A、B、C、D、E各状态,
 的是状态
的是状态③E→A所需时间为x,DC所需时间为y,则x
(3)在一定条件下,
 可还原氮氧化物,消除氮氧化物污染。工业上,常用
可还原氮氧化物,消除氮氧化物污染。工业上,常用 和
和 在催化剂作用下合成
在催化剂作用下合成 。在催化剂作用下,
。在催化剂作用下, 时,发生反应,平衡混合气中
时,发生反应,平衡混合气中 的物质的量分数随温度和压强变化的关系如图所示。
的物质的量分数随温度和压强变化的关系如图所示。
①该反应的平衡常数
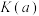
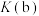 。
。②500℃、压强为
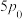 时,
时, 的转化率为
的转化率为
 为平衡分压代替平衡浓度计算求得的平衡常数(分压=总压×物质的量分数)]
为平衡分压代替平衡浓度计算求得的平衡常数(分压=总压×物质的量分数)]
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】已知A(g)+B(g) C(g)+D(g)反应的平衡常数和温度的关系如下:
C(g)+D(g)反应的平衡常数和温度的关系如下:
回答下列问题:
(1)该反应的平衡常数表达式K=____ ,ΔH=___ (填“<”、“>”或“=”)0。
(2)830℃时,向一个5 L的密闭容器中充入0.20molA和0.80molB,如反应初始6s内A的平均反应速率v(A)=0.003 mol·L-1·s-1。则6 s时c(A)=____ mol·L-1,C的物质的量为___ mol;若反应经一段时间后,达到平衡时A的转化率为____ ,如果这时向该密闭容器中再充入1 mol氩气,平衡时A的转化率为_____ 。
(3)判断该反应是否达到平衡的依据为_____ 。
a.压强不随时间改变
b.气体的密度不随时间改变
c.c(A)不随时间改变
d.单位时间里生成C和D的物质的量相等
 C(g)+D(g)反应的平衡常数和温度的关系如下:
C(g)+D(g)反应的平衡常数和温度的关系如下:| 温度/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
| 平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
(1)该反应的平衡常数表达式K=
(2)830℃时,向一个5 L的密闭容器中充入0.20molA和0.80molB,如反应初始6s内A的平均反应速率v(A)=0.003 mol·L-1·s-1。则6 s时c(A)=
(3)判断该反应是否达到平衡的依据为
a.压强不随时间改变
b.气体的密度不随时间改变
c.c(A)不随时间改变
d.单位时间里生成C和D的物质的量相等
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】KHSO4溶液显________ 性,用离子方程式表示为_______________ 。室温时KHCO3溶液的pH________ 7(填“>”“<”或“=”),用离子方程式表示为________________ 。将上述两种溶液混合,现象是________ ,离子方程式是_____________ 。
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】完成下列问题。
(1)用离子方程式表示下列盐溶液的水解反应,不能发生水解的写“不发生水解”字样,并说明溶液的酸碱性:
①K2CO3_______ ,溶液呈_______ 性;
②Na2SO4_______ ,溶液呈_______ 性;
③CuCl2_______ ,溶液呈_______ 性。
(2)将AlCl3溶于水后,经加热蒸发、蒸干,灼烧,最后所得白色固体的主要成分是_______ ;用化学方程式表述产生白色固体的过程:_______ 、_______ 。
(1)用离子方程式表示下列盐溶液的水解反应,不能发生水解的写“不发生水解”字样,并说明溶液的酸碱性:
①K2CO3
②Na2SO4
③CuCl2
(2)将AlCl3溶于水后,经加热蒸发、蒸干,灼烧,最后所得白色固体的主要成分是
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】物质在水中可能存在电离平衡、盐的水解平衡和沉淀的溶解平衡,它们都可看作化学平衡.请根据所学知识的回答:
(1)A为0.1mol/L的(NH4)2SO4溶液,在该溶液中各种离子的浓度由大到小顺序为________________
(2)B为0.1mol/LNaHCO3溶液,在NaHCO3溶液中存在的各种平衡体系为(用离子方程式表示):____________ ;___________ ;__________ 。
实验测得NaHCO3溶液的pH>7,请分析NaHCO3溶液显碱性的原因:________________
(3)C为FeCl3溶液,实验室中配制FeCl3溶液时通常需要向其中加入________________ 目的是_____________ ;若把B和C溶液混合,将产生红褐色沉淀和无色气体,该反应的离子方程为_________________ .
(4)D为含有足量AgCl固体的饱和溶液,氯化银在水中存在沉淀溶解平衡:
AgCl(s) Ag+(aq)+Cl-(aq)
Ag+(aq)+Cl-(aq)
在25℃时,氯化银的Ksp=1.8×10-10mol2/L2.现将足量氯化银分别放入:
① 100mL蒸馏水中;
② 100mL 0.2mol/LAgNO3溶液中;
③ 100mL 0.1mol/L氯化铝溶液中;
④ 100mL 0.1mol/L盐酸溶液中.充分搅拌后,相同温度下银离子浓度由大到小的顺序_____________ (填写序号);②中氯离子的浓度为_________ mol/L,③中银离子的浓度为______ mol/L
(1)A为0.1mol/L的(NH4)2SO4溶液,在该溶液中各种离子的浓度由大到小顺序为
(2)B为0.1mol/LNaHCO3溶液,在NaHCO3溶液中存在的各种平衡体系为(用离子方程式表示):
实验测得NaHCO3溶液的pH>7,请分析NaHCO3溶液显碱性的原因:
(3)C为FeCl3溶液,实验室中配制FeCl3溶液时通常需要向其中加入
(4)D为含有足量AgCl固体的饱和溶液,氯化银在水中存在沉淀溶解平衡:
AgCl(s)
 Ag+(aq)+Cl-(aq)
Ag+(aq)+Cl-(aq)在25℃时,氯化银的Ksp=1.8×10-10mol2/L2.现将足量氯化银分别放入:
① 100mL蒸馏水中;
② 100mL 0.2mol/LAgNO3溶液中;
③ 100mL 0.1mol/L氯化铝溶液中;
④ 100mL 0.1mol/L盐酸溶液中.充分搅拌后,相同温度下银离子浓度由大到小的顺序
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐1】牙齿表面由一层硬的、组成为Ca5(PO4)3OH的物质保护着,它在唾液中存在下列溶解平衡:Ca5(PO4)3OH(s)⇌5Ca2+(aq)+3 PO43—(aq)+OH−(aq)。试回答问题:
(1)小孩吃糖后,如果不及时刷牙或漱口,细菌和酶就会作用于糖,在口腔内产生有机羧酸,久而久之,牙齿就会受到腐蚀,其原因是___________ 。
(2)已知Ca5 (PO4)3F(s)的溶解度比上述矿化产物Ca5(PO4)3OH的溶解度更小,质地更坚硬。当牙膏中配有氟化物添加剂后能防止龋齿,其原因是(用离子方程式和简要文字说明)___________ 。
(3)根据以上原理,请你提出一种其他促进矿化的方法:_________________________________ 。
(1)小孩吃糖后,如果不及时刷牙或漱口,细菌和酶就会作用于糖,在口腔内产生有机羧酸,久而久之,牙齿就会受到腐蚀,其原因是
(2)已知Ca5 (PO4)3F(s)的溶解度比上述矿化产物Ca5(PO4)3OH的溶解度更小,质地更坚硬。当牙膏中配有氟化物添加剂后能防止龋齿,其原因是(用离子方程式和简要文字说明)
(3)根据以上原理,请你提出一种其他促进矿化的方法:
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)对于Ag2S(s) 2Ag+(aq)+S2-(aq),其Ksp的表达式为
2Ag+(aq)+S2-(aq),其Ksp的表达式为_______________________ 。
(2)下列说法不正确的是____ (填序号)。
①用稀盐酸洗涤AgCl沉淀比用水洗涤损耗AgCl少
②一般来说,物质的溶解度随温度的升高而增加,故物质的溶解过程大多是吸热过程
③对于Al(OH)3(s) Al3+(aq)+3OH-(aq)和Al(OH)3
Al3+(aq)+3OH-(aq)和Al(OH)3 Al3++3OH-,前者为溶解平衡,后者为电离平衡
Al3++3OH-,前者为溶解平衡,后者为电离平衡
④除去溶液中的Mg2+,用OH-沉淀比用C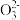 好,说明Mg(OH)2的溶解度比MgCO3大
好,说明Mg(OH)2的溶解度比MgCO3大
⑤沉淀反应中常加入过量的沉淀剂,其目的是使沉淀更完全
(3)如何除去Mg(OH)2中混有的Ca(OH)2_______________________________________________ 。
 2Ag+(aq)+S2-(aq),其Ksp的表达式为
2Ag+(aq)+S2-(aq),其Ksp的表达式为(2)下列说法不正确的是
①用稀盐酸洗涤AgCl沉淀比用水洗涤损耗AgCl少
②一般来说,物质的溶解度随温度的升高而增加,故物质的溶解过程大多是吸热过程
③对于Al(OH)3(s)
 Al3+(aq)+3OH-(aq)和Al(OH)3
Al3+(aq)+3OH-(aq)和Al(OH)3 Al3++3OH-,前者为溶解平衡,后者为电离平衡
Al3++3OH-,前者为溶解平衡,后者为电离平衡④除去溶液中的Mg2+,用OH-沉淀比用C
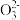 好,说明Mg(OH)2的溶解度比MgCO3大
好,说明Mg(OH)2的溶解度比MgCO3大⑤沉淀反应中常加入过量的沉淀剂,其目的是使沉淀更完全
(3)如何除去Mg(OH)2中混有的Ca(OH)2
您最近半年使用:0次



