已知A(g)+B(g) C(g)+D(g)反应的平衡常数和温度的关系如下:
C(g)+D(g)反应的平衡常数和温度的关系如下:
回答下列问题:
(1)该反应的平衡常数表达式K=____ ,ΔH=___ (填“<”、“>”或“=”)0。
(2)830℃时,向一个5 L的密闭容器中充入0.20molA和0.80molB,如反应初始6s内A的平均反应速率v(A)=0.003 mol·L-1·s-1。则6 s时c(A)=____ mol·L-1,C的物质的量为___ mol;若反应经一段时间后,达到平衡时A的转化率为____ ,如果这时向该密闭容器中再充入1 mol氩气,平衡时A的转化率为_____ 。
(3)判断该反应是否达到平衡的依据为_____ 。
a.压强不随时间改变
b.气体的密度不随时间改变
c.c(A)不随时间改变
d.单位时间里生成C和D的物质的量相等
 C(g)+D(g)反应的平衡常数和温度的关系如下:
C(g)+D(g)反应的平衡常数和温度的关系如下:| 温度/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
| 平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
(1)该反应的平衡常数表达式K=
(2)830℃时,向一个5 L的密闭容器中充入0.20molA和0.80molB,如反应初始6s内A的平均反应速率v(A)=0.003 mol·L-1·s-1。则6 s时c(A)=
(3)判断该反应是否达到平衡的依据为
a.压强不随时间改变
b.气体的密度不随时间改变
c.c(A)不随时间改变
d.单位时间里生成C和D的物质的量相等
更新时间:2019-05-25 17:02:47
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】已知: ,向一恒温恒容的密闭容器中充入
,向一恒温恒容的密闭容器中充入 和
和 发生反应,
发生反应, 时达到平衡状态Ⅰ,在
时达到平衡状态Ⅰ,在 时改变某一条件,
时改变某一条件, 时重新达到平衡状态Ⅱ,正反应速率随时间的变化如图所示。
时重新达到平衡状态Ⅱ,正反应速率随时间的变化如图所示。
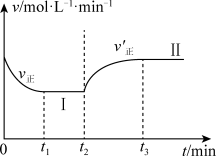
(1)容器内压强不变,表明反应达到平衡。(______)
(2) 时改变的条件是向容器中加入C。(______)
时改变的条件是向容器中加入C。(______)
 ,向一恒温恒容的密闭容器中充入
,向一恒温恒容的密闭容器中充入 和
和 发生反应,
发生反应, 时达到平衡状态Ⅰ,在
时达到平衡状态Ⅰ,在 时改变某一条件,
时改变某一条件, 时重新达到平衡状态Ⅱ,正反应速率随时间的变化如图所示。
时重新达到平衡状态Ⅱ,正反应速率随时间的变化如图所示。
(1)容器内压强不变,表明反应达到平衡。(______)
(2)
 时改变的条件是向容器中加入C。(______)
时改变的条件是向容器中加入C。(______)
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】碳和氮的化合物在生产生活中广泛存在。低碳烃类(甲烷、乙烯、丙烯等)作为重要的基本化工原料,在现代石油和化学工业中具有举足轻重的作用。
一定条件下,碘甲烷 热裂解制低碳烯烃的主要反应有:
热裂解制低碳烯烃的主要反应有:
反应①: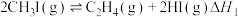
反应②: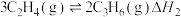
反应①和②在不同温度下的分压平衡常数 如下表,回答下列问题:
如下表,回答下列问题:
(1)根据表中数据推出反应①的活化能 (正)
(正)___________ (填“>”或“<”) (逆);
(逆);
(2)反应②的正、逆反应速率表达式有: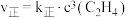 ,
,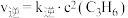 (
( 、
、 为反应速率常数,只与温度有关)。1889年,瑞典物理化学家阿仑尼乌斯根据实验结果,提出了速率常数与温度关系的经验公式:
为反应速率常数,只与温度有关)。1889年,瑞典物理化学家阿仑尼乌斯根据实验结果,提出了速率常数与温度关系的经验公式: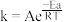 [k为速率常数;A为常数;e为自然对数的底数]。在相同温度下,活化能越大,速率常数越
[k为速率常数;A为常数;e为自然对数的底数]。在相同温度下,活化能越大,速率常数越___________ (填“大”或“小”)。当该反应达到平衡后,升高温度,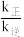 的值
的值___________ (填“增大”“减小”或“不变”);
一定条件下,碘甲烷
 热裂解制低碳烯烃的主要反应有:
热裂解制低碳烯烃的主要反应有:反应①:
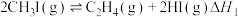
反应②:
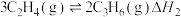
反应①和②在不同温度下的分压平衡常数
 如下表,回答下列问题:
如下表,回答下列问题: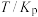 |  |  |  |  |  |  |
| 反应① | 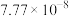 | 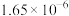 | 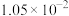 | 2.80 |  | 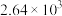 |
| 反应② | 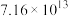 | 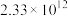 | 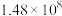 | 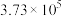 | 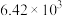 | 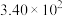 |
(1)根据表中数据推出反应①的活化能
 (正)
(正) (逆);
(逆);(2)反应②的正、逆反应速率表达式有:
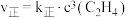 ,
,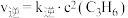 (
( 、
、 为反应速率常数,只与温度有关)。1889年,瑞典物理化学家阿仑尼乌斯根据实验结果,提出了速率常数与温度关系的经验公式:
为反应速率常数,只与温度有关)。1889年,瑞典物理化学家阿仑尼乌斯根据实验结果,提出了速率常数与温度关系的经验公式: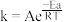 [k为速率常数;A为常数;e为自然对数的底数]。在相同温度下,活化能越大,速率常数越
[k为速率常数;A为常数;e为自然对数的底数]。在相同温度下,活化能越大,速率常数越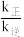 的值
的值
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】回答下列问题:
(1)取一支试管,加入2mL0.1mol/L 溶液。溶液中存在的平衡为
溶液。溶液中存在的平衡为___________ (用离子方程式表示),体系中两种含铬元素的离子颜色分别为 :
:___________ ,另一种:___________ 。
(2)用如图所示装置进行如下实验:

①在检验装置气密性后,向试管a中加入10mL1mol/L的稀硝酸和铜片,立即用橡皮塞塞紧试管口。请写出在试管a中反应的离子方程式___________ 。
②在实验过程中常常反应开始时速率缓慢,随后逐渐加快。速率随后逐渐加快的影响因素是___________ (填标号,下同),当反应进行一段时间后速率又逐渐减小的影响因素是___________ 。
A.浓度B.压强C.温度D.催化剂
③欲较快地制得NO,可采取的措施有___________ (填标号)。
A.微热B.使用铜粉C.稀释HNO3D.使用浓硝酸
(3)1200℃时,在一密闭容器中发生反应: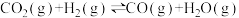 K=2.6。相同温度下,在某时刻反应混合物中CO2、H2、CO、
K=2.6。相同温度下,在某时刻反应混合物中CO2、H2、CO、 的物质的量分别为4mol、4mol、2mol、2mol,则此时用CO表示的v(正)
的物质的量分别为4mol、4mol、2mol、2mol,则此时用CO表示的v(正)___________ v(逆)(填“>”“=”或“<”)
(1)取一支试管,加入2mL0.1mol/L
 溶液。溶液中存在的平衡为
溶液。溶液中存在的平衡为 :
:(2)用如图所示装置进行如下实验:

①在检验装置气密性后,向试管a中加入10mL1mol/L的稀硝酸和铜片,立即用橡皮塞塞紧试管口。请写出在试管a中反应的离子方程式
②在实验过程中常常反应开始时速率缓慢,随后逐渐加快。速率随后逐渐加快的影响因素是
A.浓度B.压强C.温度D.催化剂
③欲较快地制得NO,可采取的措施有
A.微热B.使用铜粉C.稀释HNO3D.使用浓硝酸
(3)1200℃时,在一密闭容器中发生反应:
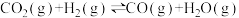 K=2.6。相同温度下,在某时刻反应混合物中CO2、H2、CO、
K=2.6。相同温度下,在某时刻反应混合物中CO2、H2、CO、 的物质的量分别为4mol、4mol、2mol、2mol,则此时用CO表示的v(正)
的物质的量分别为4mol、4mol、2mol、2mol,则此时用CO表示的v(正)
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】氨是一种重要的化工原料,在工农业生产中有广泛的应用。
(1)在一定温度下,在固定体积的密闭容器中进行可逆反应:N2(g)+3H2(g) 2NH3(g)。该可逆反应达到平衡的标志是
2NH3(g)。该可逆反应达到平衡的标志是____ (填字母)。
(2)工业上可用天然气为原料来制取氢气。某研究性学习小组的同学模拟工业制取氢气的原理,在一定温度下,在体积为2L的恒容密闭容器中测得如表所示数据:
①分析表中数据,判断5min时反应____ (填“是”或“不是”)处于平衡状态,前5min内,反应的平均反应速率v(CH4)=____ 。
②反应在7~10min内,CO的物质的量减少的原因可能是____ (填字母)。
A.减少CH4的物质的量 B.降低温度
C.升高温度 D.充入H2
(3)氨的催化氧化:4NH3(g)+5O2(g) 4NO(g)+6H2O(g)是工业制硝酸的重要反应。在1L密闭容器中充入4molNH3(g)和5molO2(g),保持其他条件不变,测得c(NO)与温度的关系如图所示。该反应的△H
4NO(g)+6H2O(g)是工业制硝酸的重要反应。在1L密闭容器中充入4molNH3(g)和5molO2(g),保持其他条件不变,测得c(NO)与温度的关系如图所示。该反应的△H_____ 0(填“>”“<”或“=”);T0℃-T℃时该平衡是否向逆反应方向移动____ (填“是”或“否”)。
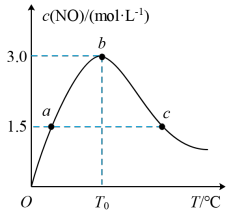
(1)在一定温度下,在固定体积的密闭容器中进行可逆反应:N2(g)+3H2(g)
 2NH3(g)。该可逆反应达到平衡的标志是
2NH3(g)。该可逆反应达到平衡的标志是| A.混合气体的物质的量不再随时间变化 |
| B.混合气体的质量不再随时间变化 |
| C.混合气体的颜色不再随时间变化 |
| D.混合气体的密度不再随时间变化 |
| 时间/min | CH4/mol | H2O/mol | CO/mol | H2/mol |
| 0 | 0.40 | 1.00 | 0 | 0 |
| 5 | a | 0.80 | c | 0.60 |
| 7 | 0.20 | b | 0.20 | d |
| 10 | 0.21 | 0.81 | 0.19 | 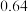 |
①分析表中数据,判断5min时反应
②反应在7~10min内,CO的物质的量减少的原因可能是
A.减少CH4的物质的量 B.降低温度
C.升高温度 D.充入H2
(3)氨的催化氧化:4NH3(g)+5O2(g)
 4NO(g)+6H2O(g)是工业制硝酸的重要反应。在1L密闭容器中充入4molNH3(g)和5molO2(g),保持其他条件不变,测得c(NO)与温度的关系如图所示。该反应的△H
4NO(g)+6H2O(g)是工业制硝酸的重要反应。在1L密闭容器中充入4molNH3(g)和5molO2(g),保持其他条件不变,测得c(NO)与温度的关系如图所示。该反应的△H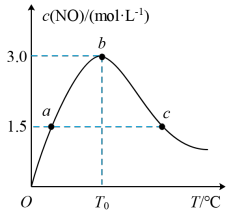
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】一定条件下,在体积为3L的密闭容器中化学反应CO(g)+2H2(g) CH3OH(g)达到平衡状态。
CH3OH(g)达到平衡状态。

(1)该反应的平衡常数表达式K=_______ ;
(2)500℃时,从反应开始到达到化学平衡,以H2的浓度变化表 示的化学反应速率是______ (用 nB,tB表示)。
(3)判断该可逆反应达到化学平衡状态的标志是_________ (填字母,下同)。
a.v生成(CH3OH)=v消耗(CO)
b.混合气体的密度不再改变
c.混合气体的平均相对分子质量不再改变
d.CO、H2、CH3OH的浓度均不再变化
 CH3OH(g)达到平衡状态。
CH3OH(g)达到平衡状态。
(1)该反应的平衡常数表达式K=
(2)500℃时,从反应开始到达到化学平衡,以H2的浓度变化表 示的化学反应速率是
(3)判断该可逆反应达到化学平衡状态的标志是
a.v生成(CH3OH)=v消耗(CO)
b.混合气体的密度不再改变
c.混合气体的平均相对分子质量不再改变
d.CO、H2、CH3OH的浓度均不再变化
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)反应N2+3H2  2NH3,已知断裂1molN2中的共价键吸收的能量为946kJ,断裂1molH2中的共价键吸收的能量为436kJ,形成1molNH3中的共价键放出的能量为1173kJ,则由N2 和H2生成2molNH3过程中的能量变化为
2NH3,已知断裂1molN2中的共价键吸收的能量为946kJ,断裂1molH2中的共价键吸收的能量为436kJ,形成1molNH3中的共价键放出的能量为1173kJ,则由N2 和H2生成2molNH3过程中的能量变化为________________ 。
(2)把3mol A和2.5mol B混合于2L固定容积的密闭容器中,在恒温下发生反应:3A(g)+B(g) xC(g)+2D(g),5min后反应达到平衡,生成0.5mol C,测得D的平均反应速率为0.1mol/(L•min),则
xC(g)+2D(g),5min后反应达到平衡,生成0.5mol C,测得D的平均反应速率为0.1mol/(L•min),则
①A的平均反应速率为______________ ;
②x=___________ ;
③平衡时容器内压强为P平,开始时容器内压强为P始,则P平:P始=_________________ ;
④判断该反应达到化学平衡状态的依据是_____________ (填字母)。
a. 同一物质的正反应速率等于逆反应速率 b. 混合气体的密度不变
c. 混合气体中c(D)不再改变 d.c(B)=c(C)
e.单位时间内,每生成1 mol B,同时生成2 mol D
f.混合气体的压强不再改变 g.υ(A)正=1/3υ(B)逆
 2NH3,已知断裂1molN2中的共价键吸收的能量为946kJ,断裂1molH2中的共价键吸收的能量为436kJ,形成1molNH3中的共价键放出的能量为1173kJ,则由N2 和H2生成2molNH3过程中的能量变化为
2NH3,已知断裂1molN2中的共价键吸收的能量为946kJ,断裂1molH2中的共价键吸收的能量为436kJ,形成1molNH3中的共价键放出的能量为1173kJ,则由N2 和H2生成2molNH3过程中的能量变化为(2)把3mol A和2.5mol B混合于2L固定容积的密闭容器中,在恒温下发生反应:3A(g)+B(g)
 xC(g)+2D(g),5min后反应达到平衡,生成0.5mol C,测得D的平均反应速率为0.1mol/(L•min),则
xC(g)+2D(g),5min后反应达到平衡,生成0.5mol C,测得D的平均反应速率为0.1mol/(L•min),则①A的平均反应速率为
②x=
③平衡时容器内压强为P平,开始时容器内压强为P始,则P平:P始=
④判断该反应达到化学平衡状态的依据是
a. 同一物质的正反应速率等于逆反应速率 b. 混合气体的密度不变
c. 混合气体中c(D)不再改变 d.c(B)=c(C)
e.单位时间内,每生成1 mol B,同时生成2 mol D
f.混合气体的压强不再改变 g.υ(A)正=1/3υ(B)逆
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】甲醇汽油是一种新能源清洁燃料,可以作为汽油的替代物。将 转化为甲醇,既可减少
转化为甲醇,既可减少 的排放,又可节约能源,转化过程涉及如下反应:
的排放,又可节约能源,转化过程涉及如下反应:
反应i:
反应ii:
(1)①写出反应的平衡常数表达式
___________ 。
②在图中画出,不同温度下( ),反应i中
),反应i中 的平衡转化率随压强变化的关系图(
的平衡转化率随压强变化的关系图(请在图上标注温度  、
、 )。
)。___________

(2)为研究反应ii平衡时 的转化率与反应物投料比(
的转化率与反应物投料比( )及温度的关系,研究小组在10L的密闭容器中进行模拟反应,并绘出下图:
)及温度的关系,研究小组在10L的密闭容器中进行模拟反应,并绘出下图:

①反应热a___________ 0(“>”或“<”),判断依据是___________ 。
②若其它条件相同,I、Ⅱ曲线分别表示投料比不同时的反应过程。投料比:I___________ Ⅱ(填“>”或“<)。若Ⅱ反应的 、投料比为0.5,A点的平衡常数
、投料比为0.5,A点的平衡常数
___________ ,B点的平衡常数
___________  (填“>”或“<”或“=”)。
(填“>”或“<”或“=”)。
 转化为甲醇,既可减少
转化为甲醇,既可减少 的排放,又可节约能源,转化过程涉及如下反应:
的排放,又可节约能源,转化过程涉及如下反应:反应i:

反应ii:

(1)①写出反应的平衡常数表达式

②在图中画出,不同温度下(
 ),反应i中
),反应i中 的平衡转化率随压强变化的关系图(
的平衡转化率随压强变化的关系图( 、
、 )。
)。
(2)为研究反应ii平衡时
 的转化率与反应物投料比(
的转化率与反应物投料比( )及温度的关系,研究小组在10L的密闭容器中进行模拟反应,并绘出下图:
)及温度的关系,研究小组在10L的密闭容器中进行模拟反应,并绘出下图:
①反应热a
②若其它条件相同,I、Ⅱ曲线分别表示投料比不同时的反应过程。投料比:I
 、投料比为0.5,A点的平衡常数
、投料比为0.5,A点的平衡常数

 (填“>”或“<”或“=”)。
(填“>”或“<”或“=”)。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】在10L的密闭容器中,进行如下化学反应:CO2(g)+H2(g)⇌CO(g)+H2O(g),其化学平衡常数K与温度t的关系如下表:
请回答:
(1)该反应为___________ (填“吸热”或“放热”)反应。
(2)该反应的化学平衡常数表达式为K=___________ 。保持温度和体积不变,充入一定量的CO2,则平衡常数___________ 。(填“增大”、“减小”或“不变”)
(3)下列措施可以提高H2的平衡转化率的是(填选项序号)___________ 。
a.选择适当的催化剂 b.增大压强 c.及时分离H2O(g) d.升高温度
(4)某温度下,c(CO2)=2mol/L,c(H2)=3mol/L,开始反应,达到平衡时CO2转化率为60%,则平衡常数K=___________ 。
(5)与(4)相同的温度下,某时刻测得c(CO2)=0.5mol/L,c(H2)=1.5mol/L,c(CO)=0.5mol/L、c(H2O)=0.5mol/L,则此时反应是否达到平衡状态_______ (填“是”或“否”)。此时,v(正)_______ v(逆)(填“ ”、“
”、“ ”或“
”或“ ”)。
”)。
(6)该反应的反应速率(v)随时间(t)变化的关系如图所示,若t2、t4时刻只改变一个条件,下列说法正确的是(填选项序号)___________ 。
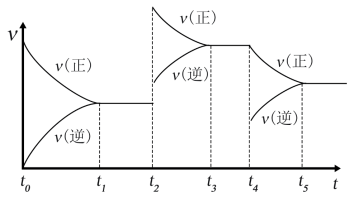
a.在t1-t2时,可依据容器内气体的压强保持不变判断反应已达到平衡状态
b.在t2时,采取的措施可以是升高温度
c.在t4时,采取的措施可以是增加CO2的浓度。
d.在t5时,容器内CO的体积分数是整个过程中的最大值
| t(℃) | 700 | 800 | 830 | 1000 | 1200 |
| K | 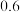 |  |  | 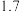 |  |
请回答:
(1)该反应为
(2)该反应的化学平衡常数表达式为K=
(3)下列措施可以提高H2的平衡转化率的是(填选项序号)
a.选择适当的催化剂 b.增大压强 c.及时分离H2O(g) d.升高温度
(4)某温度下,c(CO2)=2mol/L,c(H2)=3mol/L,开始反应,达到平衡时CO2转化率为60%,则平衡常数K=
(5)与(4)相同的温度下,某时刻测得c(CO2)=0.5mol/L,c(H2)=1.5mol/L,c(CO)=0.5mol/L、c(H2O)=0.5mol/L,则此时反应是否达到平衡状态
 ”、“
”、“ ”或“
”或“ ”)。
”)。(6)该反应的反应速率(v)随时间(t)变化的关系如图所示,若t2、t4时刻只改变一个条件,下列说法正确的是(填选项序号)

a.在t1-t2时,可依据容器内气体的压强保持不变判断反应已达到平衡状态
b.在t2时,采取的措施可以是升高温度
c.在t4时,采取的措施可以是增加CO2的浓度。
d.在t5时,容器内CO的体积分数是整个过程中的最大值
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】工业生产中可以以 与
与 为原料制备清洁能源甲醇:
为原料制备清洁能源甲醇: 
(1)在一定条件下,改变条件,使化学平衡向正反应方向移动,下列结论正确的是___________。
(2)将 和
和 按下表所示加入两个体积均为
按下表所示加入两个体积均为 的恒容密闭容器中,进行反应并达到平衡(已知
的恒容密闭容器中,进行反应并达到平衡(已知 ):
):

该反应是___________ (填“吸热”或“放热”)反应。以下为 的平衡转化率随某一物理量变化的曲线图,则横坐标x表示的物理量除压强外,还可以是
的平衡转化率随某一物理量变化的曲线图,则横坐标x表示的物理量除压强外,还可以是___________ (任意㝍一种)。
(3)高炉炼铁基本反应如下: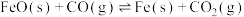

①该反应的平衡常数表达式为___________ 。
②若平衡后,保持温度不变,加入 后,
后, 将
将___________ (填“增大”、“减小”或“不变”)。1100℃时 ,测得高炉中
,测得高炉中 ,
, ,此时,化学反应速率是
,此时,化学反应速率是
___________  (填“>”、“<”、“=”),其理由是
(填“>”、“<”、“=”),其理由是___________ 。
(4)温度升高,化学平衡移动后达到新的平衡,
___________ 。(填“增大”、“减小”或“不变")。指出两条提高 的平衡转化率的措施
的平衡转化率的措施___________ 。
 与
与 为原料制备清洁能源甲醇:
为原料制备清洁能源甲醇: 
(1)在一定条件下,改变条件,使化学平衡向正反应方向移动,下列结论正确的是___________。
| A.生成物的百分含量一定增大 | B.生成物的产量一定增加 |
| C.反应物A的转化率一定增大 | D.反应物的百分含量一定都降低 |
 和
和 按下表所示加入两个体积均为
按下表所示加入两个体积均为 的恒容密闭容器中,进行反应并达到平衡(已知
的恒容密闭容器中,进行反应并达到平衡(已知 ):
):| 实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所 | ||
 |  |  |  | 需时间/min | ||
| 1 |  | 1 | 3 |  |  | |
| 2 |  | 1 | 3 | 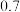 |  | |

该反应是
 的平衡转化率随某一物理量变化的曲线图,则横坐标x表示的物理量除压强外,还可以是
的平衡转化率随某一物理量变化的曲线图,则横坐标x表示的物理量除压强外,还可以是(3)高炉炼铁基本反应如下:
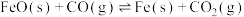

①该反应的平衡常数表达式为
②若平衡后,保持温度不变,加入
 后,
后, 将
将 ,测得高炉中
,测得高炉中 ,
, ,此时,化学反应速率是
,此时,化学反应速率是
 (填“>”、“<”、“=”),其理由是
(填“>”、“<”、“=”),其理由是(4)温度升高,化学平衡移动后达到新的平衡,

 的平衡转化率的措施
的平衡转化率的措施
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】能源短缺是人类面临的重大问题之一。甲醇是一种可再生能源,具有广泛的开发和应用前景。工业上合成甲醇一般采用以下反应:
CO(g)+2H2(g) CH3OH(g)+Q
CH3OH(g)+Q
下表所列数据是上述反应在不同温度下的化学平衡常数(K)
(1)在一定条件下将2molCO和6molH2充入2L的密闭容器中发生反应,5分钟后测得c(H2)=1.5mol/L,则此段时间内的反应速率(用CH3OH表达)___ mol/(L·min)。
(2)由表中数据分析可知,Q___ 0(填“>”、“<”或“=”)。其它条件不变的情况下,若压缩容器的体积,则平衡移动___ (“向正反应方向”“向逆反应方向”或“不”),化学平衡常数K___ (填“增大”、“减小”或“不变”)。
(3)在体积一定的密闭容器中,能说明该反应已处于化学平衡状态的是___ (填编号)。
a.V正(CO)= V正(H2) b.混合气体的密度保持不变
V正(H2) b.混合气体的密度保持不变
c.反应体系中的热效应不再变化 d.c(CO):c(CH3OH)=1:1
(4)寻找到合适的催化剂是实现反应工业化的关键。该反应使用催化剂无法实现的目标是___ (填编号)。
a.提高单位时间内甲醇的产量 b.增大混合气体中甲醇的体积分数
c.缩短达到平衡所需时间 d.提高一氧化碳的转化率
CO(g)+2H2(g)
 CH3OH(g)+Q
CH3OH(g)+Q下表所列数据是上述反应在不同温度下的化学平衡常数(K)
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
(1)在一定条件下将2molCO和6molH2充入2L的密闭容器中发生反应,5分钟后测得c(H2)=1.5mol/L,则此段时间内的反应速率(用CH3OH表达)
(2)由表中数据分析可知,Q
(3)在体积一定的密闭容器中,能说明该反应已处于化学平衡状态的是
a.V正(CO)=
 V正(H2) b.混合气体的密度保持不变
V正(H2) b.混合气体的密度保持不变c.反应体系中的热效应不再变化 d.c(CO):c(CH3OH)=1:1
(4)寻找到合适的催化剂是实现反应工业化的关键。该反应使用催化剂无法实现的目标是
a.提高单位时间内甲醇的产量 b.增大混合气体中甲醇的体积分数
c.缩短达到平衡所需时间 d.提高一氧化碳的转化率
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】NH3水溶液呈弱碱性,并可用作农业化肥,现进行下列研究:现将一定量的H2和N2充入10L的密闭容器中,在一定条件下使其发生反应,有关H2、N2、NH3三者的物质的量的变化与时间的关系如图所示:

(1)若t1=10min,则0至t1时间内H2的反应速率为_________ ;
(2)下列几种情形中可以证明合成氨的反应N2(g)+3H2(g) 2NH3(g)已达平衡状态的是
2NH3(g)已达平衡状态的是_____ 。
①单位时间内生成nmolN2的同时生成2nmolNH3;
②1个N≡N键断裂的同时,有6个N—H键形成;
③1个N≡N键断裂的同时,有3个H—H键形成;
④混合气体的压强不再改变的状态;
⑤混合气体的密度不再改变的状态;
⑥混合气体的平均相对分子质量不再改变的状态。
(3)根据图中曲线变化情况判断,t1时刻改变的反应条件可能是_____ (填字母)
a.加入了催化剂 b.降低了反应的温度 c.缩小容器体积增大压强
(4)t2时刻后反应达平衡,N2总共的转化率为______ 。
(5)在t1时刻对应的反应条件下,该反应的平衡常数是______ 。

(1)若t1=10min,则0至t1时间内H2的反应速率为
(2)下列几种情形中可以证明合成氨的反应N2(g)+3H2(g)
 2NH3(g)已达平衡状态的是
2NH3(g)已达平衡状态的是①单位时间内生成nmolN2的同时生成2nmolNH3;
②1个N≡N键断裂的同时,有6个N—H键形成;
③1个N≡N键断裂的同时,有3个H—H键形成;
④混合气体的压强不再改变的状态;
⑤混合气体的密度不再改变的状态;
⑥混合气体的平均相对分子质量不再改变的状态。
(3)根据图中曲线变化情况判断,t1时刻改变的反应条件可能是
a.加入了催化剂 b.降低了反应的温度 c.缩小容器体积增大压强
(4)t2时刻后反应达平衡,N2总共的转化率为
(5)在t1时刻对应的反应条件下,该反应的平衡常数是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】乙炔是重要的化工原料,广泛用于有机合成和氧炔焊等。生产乙炔的方法有多种,如电石法、甲烷裂解法等。
(1)在Co(NO3)2催化下,乙炔可被50%的浓硝酸(硝酸被还原为NO2)在20~70℃时直接氧化为H2C2O4·2H2O。
①该反应的化学方程式为_______ ;
②实际生产中硝酸可循环利用而不被消耗,用方程式说明:_______ 。
(2)电石法原理为:由石油焦与生石灰在电炉中生成电石CaC2(含Ca3P2、CaS等杂质),电石与水反应生成C2H4(含PH3及H2S等杂质)。
①已知焦炭固体与氧化钙固体每生成lgCaC2固体,同时生成CO气体吸收7.25kJ的热量,则该反应的热化学方程式为_______ ;
②用CuSO4溶液净化乙炔气体,去除PH3的反应之一为:4CuSO4+PH3+4H2O=4Cu↓+H3PO4+4H2SO4,每去除1molPH3,该反应中转移电子的物质的量为_______ ;
③反应H2S(aq)+Cu2+(aq)=CuS(s)+2H+(aq)的平衡常数为_______ ;(已知Ksp(CuS)=1.25×10-36,H2S的Kal=1×10-7,Ka2=1×10-13)
④电石法工艺流程简单、容易操作、乙炔纯度高,缺点是_______ (举1例)。
(3)甲烷裂解法原理为:2CH4(g) C2H2(g)+3H2(g) ΔH,实验测得该反应的Kp(用平衡分压代替浓度计算的平衡常数,分压=总压×物质的量分数)与温度的关系如图所示:
C2H2(g)+3H2(g) ΔH,实验测得该反应的Kp(用平衡分压代替浓度计算的平衡常数,分压=总压×物质的量分数)与温度的关系如图所示:

①该反应的ΔH_______ 0(填“>”、“=”或“<”);
②图中G点v(正)_______ v(逆)(填“>”、“=”或“<”);
③M点时,若容器中气体的总物质的量为1mol,则总压p与n(CH4)、n(C2H2)及n(H2)之间的关系为_______ 。
(1)在Co(NO3)2催化下,乙炔可被50%的浓硝酸(硝酸被还原为NO2)在20~70℃时直接氧化为H2C2O4·2H2O。
①该反应的化学方程式为
②实际生产中硝酸可循环利用而不被消耗,用方程式说明:
(2)电石法原理为:由石油焦与生石灰在电炉中生成电石CaC2(含Ca3P2、CaS等杂质),电石与水反应生成C2H4(含PH3及H2S等杂质)。
①已知焦炭固体与氧化钙固体每生成lgCaC2固体,同时生成CO气体吸收7.25kJ的热量,则该反应的热化学方程式为
②用CuSO4溶液净化乙炔气体,去除PH3的反应之一为:4CuSO4+PH3+4H2O=4Cu↓+H3PO4+4H2SO4,每去除1molPH3,该反应中转移电子的物质的量为
③反应H2S(aq)+Cu2+(aq)=CuS(s)+2H+(aq)的平衡常数为
④电石法工艺流程简单、容易操作、乙炔纯度高,缺点是
(3)甲烷裂解法原理为:2CH4(g)
 C2H2(g)+3H2(g) ΔH,实验测得该反应的Kp(用平衡分压代替浓度计算的平衡常数,分压=总压×物质的量分数)与温度的关系如图所示:
C2H2(g)+3H2(g) ΔH,实验测得该反应的Kp(用平衡分压代替浓度计算的平衡常数,分压=总压×物质的量分数)与温度的关系如图所示:
①该反应的ΔH
②图中G点v(正)
③M点时,若容器中气体的总物质的量为1mol,则总压p与n(CH4)、n(C2H2)及n(H2)之间的关系为
您最近一年使用:0次



