下图是部分短周期元素原子半径与原子序数的关系图。则下列说法正确的是( )
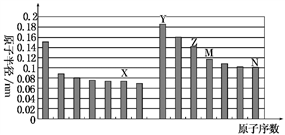

| A.Z、N两种元素的离子半径相比,前者较大 |
| B.X、N两种元素的气态氢化物的沸点相比,前者较低 |
| C.由X与M两种元素组成的化合物不能与任何酸反应,但能与强碱反应 |
| D.Z的氧化物能分别溶解于Y的氢氧化物和N的氢化物的水溶液 |
2014·全国·一模 查看更多[10]
(已下线)2014高考名师推荐化学元素周期律及其应用2015-2016学年江西省玉山一中高一下第一次月考化学试卷22015-2016学年黑龙江省哈尔滨六中高二下期中化学试卷2015-2016学年湖北省襄阳一中高一下学期期末化学试卷北京四中2017-2018学年高一下学期第一次月考化学试题甘肃省兰州市第一中学2017-2018学年高一下学期第一次月考化学试题甘肃省静宁县第一中学2017-2018学年高一下学期第二次月考化学试题河北省衡水市桃城区第十四中学2019-2020学年高一下学期第五次综合测试化学试题湖北省黄冈市黄梅国际育才高级中学2018-2019学年高一下学期5月月考化学试题上海市闵行区七宝中学2020届高三化学等级考练习(四)
更新时间:2016-07-26 08:58:54
|
相似题推荐
单选题
|
容易
(0.94)
解题方法
【推荐1】X、Y、Z、W是原子序数依次增大的短周期主族元素且均为非金属元素,X原子最外层电子数为内层电子数的2倍,Z是地壳中含量(质量分数)最高的元素,W与X位于同一主族。下列说法正确的是
| A.XZ、YZ均为酸性氧化物 | B.非金属性: |
C.简单氢化物的沸点: | D.氧化物对应水化物的酸性: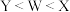 |
您最近一年使用:0次
单选题
|
容易
(0.94)
名校
解题方法
【推荐2】已知同周期X、Y、Z三种元素的最高价氧化物对应水化物酸性由强到弱的顺序为HXO4>H2YO4>H3ZO4,则下列判断中正确的是
| A.单质的氧化性按X、Y、Z的顺序增强 |
| B.阴离子的还原性按X、Y、Z的顺序减弱 |
| C.气态氢化物的稳定性按X、Y、Z的顺序增强 |
| D.元素非金属性按X、Y、Z的顺序减弱 |
您最近一年使用:0次
单选题
|
容易
(0.94)
名校
【推荐1】下列各图曲线分别表示物质的某种性质与核电荷数的关系(Z为核电荷数,γ为元素的有关性质),下列选项中的对应关系错误的是
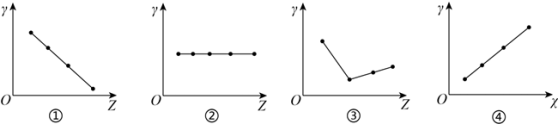

| A.图①可以表示F-、Na+、Mg2+、Al3+四种离子的离子半径大小关系 |
| B.图②可以表示ⅡA族元素的最外层电子数 |
| C.图③可以表示ⅤA族元素氢化物的沸点高低关系 |
| D.图④可以表示第三周期中的非金属元素的氢化物的稳定性 |
您最近一年使用:0次
单选题
|
容易
(0.94)
名校
【推荐2】类比是研究物质性质的常用方法之一,可预测许多物质的性质。但类比是相对的,不能违背客观实际。下列各说法中正确的是
| A.F、Cl原子同主族, Cl元素的最高正价为+7价, 故F元素最高正价也为+7 |
| B.已知Al能与O2生成致密氧化膜保护金属,推测Fe也与O2生成氧化膜保护金属 |
| C.AlCl3与过量NaOH溶液反应生成AlO2-,则与过量NH3·H2O也生成AlO2- |
| D.已知SO2通入BaCl2溶液中不产生沉淀,推测CO2通入BaCl2溶液中也不产生沉淀 |
您最近一年使用:0次
单选题
|
容易
(0.94)
名校
解题方法
【推荐1】 、
、 是元素周期表第Ⅶ
是元素周期表第Ⅶ 族中的两种元素,下列叙述能说明
族中的两种元素,下列叙述能说明 元素原子得电子能力比
元素原子得电子能力比 强的是
强的是
 、
、 是元素周期表第Ⅶ
是元素周期表第Ⅶ 族中的两种元素,下列叙述能说明
族中的两种元素,下列叙述能说明 元素原子得电子能力比
元素原子得电子能力比 强的是
强的是A. 的电子层数比 的电子层数比 的电子层数多 的电子层数多 |
B. 的酸性比 的酸性比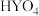 的弱 的弱 |
C. 比 比 稳定 稳定 |
D. 的单质能将 的单质能将 的单质从 的单质从 的溶液中置换出来 的溶液中置换出来 |
您最近一年使用:0次
单选题
|
容易
(0.94)
【推荐2】下列说法中,正确的是
| A.在周期表里,主族元素所在的族序数等于原子核外电子数 |
| B.在周期表里,元素所在的周期数等于原子核外电子层数 |
| C.最外层电子数为8的粒子是稀有气体元素的原子 |
| D.元素的原子序数越大,其族序数也越大 |
您最近一年使用:0次



