某结晶水合物含有两种阳离子和一种阴离子。称取两份质量均为1.96g的该结晶水合物,分别制成溶液。一份加入足量Ba(OH)2溶液,生成白色沉淀,随即沉淀变为灰绿色,最后带有红褐色;加热该混合物,逸出能使湿润的红色石蕊试纸变蓝的气体;用稀盐酸处理沉淀物,经洗涤和干燥,得到白色固体2.33 g。另一份加入含0.001 molKMnO4的酸性溶液,MnO4-恰好完全被还原为Mn2+。
请回答以下问题:
(1)该结晶水合物中含有的两种阳离子是________ 和__________ ,阴离子是________ 。
(2)试通过计算确定该结晶水合物的化学式________________ 。
请回答以下问题:
(1)该结晶水合物中含有的两种阳离子是
(2)试通过计算确定该结晶水合物的化学式
11-12高一上·辽宁沈阳·期中 查看更多[2]
更新时间:2016-12-09 09:01:50
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】已知铜与稀 发生反应
发生反应 ,
,
(1)上述反应的离子方程式为_______ 。
(2)上述反应中,氧化剂是_______ (填化学式),氧化产物是_______ (填化学式)。
(3)若反应中消耗了2mol ,则生成标况下NO的体积为
,则生成标况下NO的体积为_______ 。
(4)用单线桥法标出该反应的电子转移_____ 。
 发生反应
发生反应 ,
,(1)上述反应的离子方程式为
(2)上述反应中,氧化剂是
(3)若反应中消耗了2mol
 ,则生成标况下NO的体积为
,则生成标况下NO的体积为(4)用单线桥法标出该反应的电子转移
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】为实现消除碘缺乏病的目标,国家卫生部规定食盐必须加碘,其中碘以碘酸钾或碘化钾的形式存在。
(1)有人烹调时,分别含有碘化钾和碘酸钾的加碘食盐混合,当滴食醋时,产生紫色蒸气,反应的离子方程式为_______________ 。
(2)可以利用Na2S2O3滴定I2来测定食盐中的含碘量,发生的反应如下: I2+2Na2S2O3===2NaI+Na2S4O6,判断滴定终点的现象是___________________ ,该滴定实验必须在中性或弱酸性溶液中进行。因为在碱性溶液中,I2会发生反应(已知IO3-比IO-更稳定),其离子方程式为_________________________________________ ,而且I2与S2O32-发生副发应,其离子方程式为______________________________ 。
(3)若在强酸性溶液中,Na2S2O3会发生分解,其离子方程式为____________ ,同时I 离子容易与空气中的氧气发生反应,其反应的离子方程为
离子容易与空气中的氧气发生反应,其反应的离子方程为____________ 。
(1)有人烹调时,分别含有碘化钾和碘酸钾的加碘食盐混合,当滴食醋时,产生紫色蒸气,反应的离子方程式为
(2)可以利用Na2S2O3滴定I2来测定食盐中的含碘量,发生的反应如下: I2+2Na2S2O3===2NaI+Na2S4O6,判断滴定终点的现象是
(3)若在强酸性溶液中,Na2S2O3会发生分解,其离子方程式为
 离子容易与空气中的氧气发生反应,其反应的离子方程为
离子容易与空气中的氧气发生反应,其反应的离子方程为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】氯及其化合物在生产、生活中有着广泛的用途。
(1)①写出实验室中制取氯气的离子方程式:_______ 。
②已知KMnO4与浓盐酸反应的化学方程式:2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O,该反应也可以用来制取氯气,15.8gKMnO4能氧化_______ molHCl。
③实验室还可以利用反应KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O制取氯气。若制取标准状况下6.72L氯气,反应过程中转移电子的数目为_______ ;用双线桥表示该反应电子转移的方向和数目:_______ 。
(2)①浸泡衣物时加入“84”消毒液,在空气中放置一段时间漂白效果更好,原因为:_______ (用离子方程式表示,已知酸性:H2CO3>HClO> )。
)。
②某温度下,将氯气通入NaOH溶液中,反应得到NaCl、NaClO和NaClO3的混合溶液,经测定ClO-与 ;的物质的量之比为1:1,写出该反应的化学方程式:
;的物质的量之比为1:1,写出该反应的化学方程式:_______ 。
(3)世界卫生组织将ClO2定为A级高效安全灭菌消毒剂,它在食品保鲜、消毒等方面有广泛应用。消毒效率是用单位质量的消毒剂得电子数来表示的,ClO2作消毒剂时和氯气一样,还原产物均为Cl-,ClO2的消毒效率是氯气的_______ 倍(保留两位小数)。
(1)①写出实验室中制取氯气的离子方程式:
②已知KMnO4与浓盐酸反应的化学方程式:2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O,该反应也可以用来制取氯气,15.8gKMnO4能氧化
③实验室还可以利用反应KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O制取氯气。若制取标准状况下6.72L氯气,反应过程中转移电子的数目为
(2)①浸泡衣物时加入“84”消毒液,在空气中放置一段时间漂白效果更好,原因为:
 )。
)。②某温度下,将氯气通入NaOH溶液中,反应得到NaCl、NaClO和NaClO3的混合溶液,经测定ClO-与
 ;的物质的量之比为1:1,写出该反应的化学方程式:
;的物质的量之比为1:1,写出该反应的化学方程式:(3)世界卫生组织将ClO2定为A级高效安全灭菌消毒剂,它在食品保鲜、消毒等方面有广泛应用。消毒效率是用单位质量的消毒剂得电子数来表示的,ClO2作消毒剂时和氯气一样,还原产物均为Cl-,ClO2的消毒效率是氯气的
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】铜是生产和生活中用量较多的金属。
(1)下列有关铜元素的说法中,不正确的是__________ (填字母)
A.青铜、不锈钢、硬铝都是合金
B.铜表面易形成致密的氧化膜
C.铜与O2反应生成黑色的CuO
D.CuSO4·5H2O是一种混合物,加热后变为白色固体
(2)某化学小组为测定某铜铝混合物中铜的质量分数,设计了如下实验方案:
方案Ⅰ:铜铝混合物 测定生成气体的体积
测定生成气体的体积
方案Ⅱ:铜铝混合物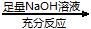 测定剩余固体的质量
测定剩余固体的质量
①请写出方案Ⅰ中铜与稀硝酸反应的离子方程式:___________ ,该方案中稀硝酸表现出来的性质是___________ (填字母)。
A.挥发性 B.酸性 C.氧化性 D.还原性
②方案Ⅱ比方案Ⅰ更易于实施,理由是________________ 。请写出方案Ⅱ中发生反应的化学方程式:____________ ,该反应产生气体在标准状况下的体积为________ (铜铝混合物质量是m1g,反应后剩余固体的质量m2g,用含m1、m2的代数式表示)。
(1)下列有关铜元素的说法中,不正确的是
A.青铜、不锈钢、硬铝都是合金
B.铜表面易形成致密的氧化膜
C.铜与O2反应生成黑色的CuO
D.CuSO4·5H2O是一种混合物,加热后变为白色固体
(2)某化学小组为测定某铜铝混合物中铜的质量分数,设计了如下实验方案:
方案Ⅰ:铜铝混合物
 测定生成气体的体积
测定生成气体的体积方案Ⅱ:铜铝混合物
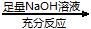 测定剩余固体的质量
测定剩余固体的质量①请写出方案Ⅰ中铜与稀硝酸反应的离子方程式:
A.挥发性 B.酸性 C.氧化性 D.还原性
②方案Ⅱ比方案Ⅰ更易于实施,理由是
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】回答下列小题
(1)为什么化学变化中总是伴随着能量的变化_____ ?
(2)如何除去NO气体中混有的少量的NO2气体杂质_____ ?
(3)酸雨的产生那些物质有关?酸雨造成的危害有哪些_____ ?
(1)为什么化学变化中总是伴随着能量的变化
(2)如何除去NO气体中混有的少量的NO2气体杂质
(3)酸雨的产生那些物质有关?酸雨造成的危害有哪些
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐3】在浓硝酸中加入铜片,回答问题。
(1)开始反应的化学方程式为_________________________ ,实验现象为____________ 。
(2)待反应停止后,再加入少量质量分数为25%的稀硫酸,这时铜片上又有气泡产生,其原因是(用离子方程式表示)___________________________________ 。
(3)若将12.8 g铜跟一定量的浓硝酸反应,铜耗完时,共产生气体(NO和NO2的混合气体)5.6 L(标准状况),则所消耗的硝酸的物质的量是_______ ,所得气体的平均相对分子质量为_______ 。
(1)开始反应的化学方程式为
(2)待反应停止后,再加入少量质量分数为25%的稀硫酸,这时铜片上又有气泡产生,其原因是(用离子方程式表示)
(3)若将12.8 g铜跟一定量的浓硝酸反应,铜耗完时,共产生气体(NO和NO2的混合气体)5.6 L(标准状况),则所消耗的硝酸的物质的量是
您最近半年使用:0次



