氯及其化合物在生产、生活中有着广泛的用途。
(1)①写出实验室中制取氯气的离子方程式:_______ 。
②已知KMnO4与浓盐酸反应的化学方程式:2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O,该反应也可以用来制取氯气,15.8gKMnO4能氧化_______ molHCl。
③实验室还可以利用反应KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O制取氯气。若制取标准状况下6.72L氯气,反应过程中转移电子的数目为_______ ;用双线桥表示该反应电子转移的方向和数目:_______ 。
(2)①浸泡衣物时加入“84”消毒液,在空气中放置一段时间漂白效果更好,原因为:_______ (用离子方程式表示,已知酸性:H2CO3>HClO> )。
)。
②某温度下,将氯气通入NaOH溶液中,反应得到NaCl、NaClO和NaClO3的混合溶液,经测定ClO-与 ;的物质的量之比为1:1,写出该反应的化学方程式:
;的物质的量之比为1:1,写出该反应的化学方程式:_______ 。
(3)世界卫生组织将ClO2定为A级高效安全灭菌消毒剂,它在食品保鲜、消毒等方面有广泛应用。消毒效率是用单位质量的消毒剂得电子数来表示的,ClO2作消毒剂时和氯气一样,还原产物均为Cl-,ClO2的消毒效率是氯气的_______ 倍(保留两位小数)。
(1)①写出实验室中制取氯气的离子方程式:
②已知KMnO4与浓盐酸反应的化学方程式:2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O,该反应也可以用来制取氯气,15.8gKMnO4能氧化
③实验室还可以利用反应KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O制取氯气。若制取标准状况下6.72L氯气,反应过程中转移电子的数目为
(2)①浸泡衣物时加入“84”消毒液,在空气中放置一段时间漂白效果更好,原因为:
 )。
)。②某温度下,将氯气通入NaOH溶液中,反应得到NaCl、NaClO和NaClO3的混合溶液,经测定ClO-与
 ;的物质的量之比为1:1,写出该反应的化学方程式:
;的物质的量之比为1:1,写出该反应的化学方程式:(3)世界卫生组织将ClO2定为A级高效安全灭菌消毒剂,它在食品保鲜、消毒等方面有广泛应用。消毒效率是用单位质量的消毒剂得电子数来表示的,ClO2作消毒剂时和氯气一样,还原产物均为Cl-,ClO2的消毒效率是氯气的
更新时间:2022-08-19 19:37:50
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】用双线桥法标出下列反应的电子转移情况和化合价升降情况
Fe+H2SO4=FeSO4+H2↑_____________________________________
Fe+H2SO4=FeSO4+H2↑
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】“探险队员”(饱和 溶液)不小心走入了化学迷宫,不知怎样走出来,因为迷宫里面有许多“吃人的野兽”(即能与饱和
溶液)不小心走入了化学迷宫,不知怎样走出来,因为迷宫里面有许多“吃人的野兽”(即能与饱和 溶液反应的物质),饱和
溶液反应的物质),饱和 溶液必须避开他们,否则无法通过。
溶液必须避开他们,否则无法通过。
已知: 为中强酸,酸性:
为中强酸,酸性: 。
。

请回答下列问题:
(1)请你帮助他走出迷宫(用图中物质前的序号连接起来表示所走的路线):______ 。
(2)图中不能与饱和 溶液反应的物质中属于非电解质的是
溶液反应的物质中属于非电解质的是______ (填序号)。
(3)图中能与饱和 溶液反应且反应的产物中有单质的物质有
溶液反应且反应的产物中有单质的物质有______ 种,写出上述反应中 中硫元素得电子反应的化学方程式,并用单线桥法标出电子转移的方向和数目:
中硫元素得电子反应的化学方程式,并用单线桥法标出电子转移的方向和数目:______ 。
(4)图中能吃掉饱和 溶液且产生白色沉淀的物质为
溶液且产生白色沉淀的物质为______ (填化学式),饱和 溶液与足量该物质的溶液反应的离子方程式为
溶液与足量该物质的溶液反应的离子方程式为____________ 。
(5)图中能吃掉饱和 溶液的盐的俗名为
溶液的盐的俗名为______ ,写出两者之间发生反应的离子方程式:____________ 。
 溶液)不小心走入了化学迷宫,不知怎样走出来,因为迷宫里面有许多“吃人的野兽”(即能与饱和
溶液)不小心走入了化学迷宫,不知怎样走出来,因为迷宫里面有许多“吃人的野兽”(即能与饱和 溶液反应的物质),饱和
溶液反应的物质),饱和 溶液必须避开他们,否则无法通过。
溶液必须避开他们,否则无法通过。已知:
 为中强酸,酸性:
为中强酸,酸性: 。
。
请回答下列问题:
(1)请你帮助他走出迷宫(用图中物质前的序号连接起来表示所走的路线):
(2)图中不能与饱和
 溶液反应的物质中属于非电解质的是
溶液反应的物质中属于非电解质的是(3)图中能与饱和
 溶液反应且反应的产物中有单质的物质有
溶液反应且反应的产物中有单质的物质有 中硫元素得电子反应的化学方程式,并用单线桥法标出电子转移的方向和数目:
中硫元素得电子反应的化学方程式,并用单线桥法标出电子转移的方向和数目:(4)图中能吃掉饱和
 溶液且产生白色沉淀的物质为
溶液且产生白色沉淀的物质为 溶液与足量该物质的溶液反应的离子方程式为
溶液与足量该物质的溶液反应的离子方程式为(5)图中能吃掉饱和
 溶液的盐的俗名为
溶液的盐的俗名为
您最近一年使用:0次
【推荐3】(1)某反应中反应物与生成物有:AsH3、H2SO4、KBrO3、K2SO4、H3AsO4、H2O和一种未知物质X。(As为砷元素)
①已知KBrO3在反应中得到电子,则该反应的还原剂是____________________
②已知0.2mol KBrO3在反应中得到1mol电子生成X,则X的化学式为_____________
③根据上述反应可推知_______
a.氧化性:KBrO3>H3AsO4 b.氧化性:H3AsO4> KBrO3
c.还原性:AsH3>X d.还原性:X > AsH3
(2)①向MnSO4和硫酸的混合溶液里加入K2S2O8(过二硫酸钾),溶液会发如下反应:Mn2++S2O82-+H2O→MnO4-+SO42-+H+,该反应常用于检验Mn2+的存在。其特征现象是_________________ ,若反应中有0.1 mol还原剂参加反应,则消耗氧化剂的物质的量为__________
②将NaBiO3固体(黄色微溶)加入到MnSO4和H2SO4的混合溶液里加热,固体溶解变为澄清溶液,发生如下反应:NaBiO3+MnSO4+H2SO4→Na2SO4+Bi2(SO4)3+NaMnO4+H2O,配平上述反应的化学方程式,并用双线桥标出电子转移的方向和数目__________ ;
①已知KBrO3在反应中得到电子,则该反应的还原剂是
②已知0.2mol KBrO3在反应中得到1mol电子生成X,则X的化学式为
③根据上述反应可推知
a.氧化性:KBrO3>H3AsO4 b.氧化性:H3AsO4> KBrO3
c.还原性:AsH3>X d.还原性:X > AsH3
(2)①向MnSO4和硫酸的混合溶液里加入K2S2O8(过二硫酸钾),溶液会发如下反应:Mn2++S2O82-+H2O→MnO4-+SO42-+H+,该反应常用于检验Mn2+的存在。其特征现象是
②将NaBiO3固体(黄色微溶)加入到MnSO4和H2SO4的混合溶液里加热,固体溶解变为澄清溶液,发生如下反应:NaBiO3+MnSO4+H2SO4→Na2SO4+Bi2(SO4)3+NaMnO4+H2O,配平上述反应的化学方程式,并用双线桥标出电子转移的方向和数目
您最近一年使用:0次
【推荐1】近年来,我国储氢纳米碳管研究获重大进展,电弧法合成的碳纳米管常伴有大量物质――碳纳米颗粒。这种碳纳米颗粒可用氧化气化法提纯。其反应的化学方程式为:C+ K2Cr2O7+ H2SO4(稀) → CO2↑+ K2SO4+ Cr2(SO4)3+______
(1)完成并配平上述反应的化学方程式______ 。
(2)此反应的氧化剂是______ ,氧化产物是______ 。
(3)H2SO4在上述反应中表现出来的性质是______ (填选项编号)。
A.酸性 B.氧化性 C.吸水性 D.脱水性
(4)上述反应中若产生11g气体物质,则转移电子的数目为______ 。
(1)完成并配平上述反应的化学方程式
(2)此反应的氧化剂是
(3)H2SO4在上述反应中表现出来的性质是
A.酸性 B.氧化性 C.吸水性 D.脱水性
(4)上述反应中若产生11g气体物质,则转移电子的数目为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】从物质类别和元素化合价两个维度研究物质的性质及转化是重要的化学学习方法。氯及其化合物有重要用途,如图为氯元素的“价类二维图”的部分信息。请回答下列问题:
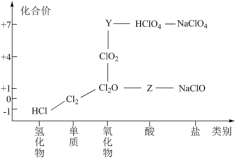
(1)根据图中信息写出Y、Z的化学式______ 、______ 。
(2)漂白液的有效成分是______ ,氯气既有氧化性又有还原性,结合图示说明理由______ 。
(3)实验室可用二氧化锰与浓盐酸在加热条件下制得氯气。写出该反应的化学方程式______ ,该反应中盐酸表现______ (填字母)。
A.酸性 B.氧化性 C.还原性
(4)84消毒液使用说明中特别提醒不可与洁厕灵混合使用,否则会产生氯气,有关反应方程式为NaClO+2HCl═NaCl+Cl2↑+H2O,下列有关该反应说法不正确 的是______ 。
(5)ClO2在杀菌消毒过程中会产生副产物亚氯酸盐(ClO ),需将其转化为Cl-除去,下列试剂中可将ClO
),需将其转化为Cl-除去,下列试剂中可将ClO 转化为Cl-的是
转化为Cl-的是______ (填字母)。

(1)根据图中信息写出Y、Z的化学式
(2)漂白液的有效成分是
(3)实验室可用二氧化锰与浓盐酸在加热条件下制得氯气。写出该反应的化学方程式
A.酸性 B.氧化性 C.还原性
(4)84消毒液使用说明中特别提醒不可与洁厕灵混合使用,否则会产生氯气,有关反应方程式为NaClO+2HCl═NaCl+Cl2↑+H2O,下列有关该反应说法
| A.n(氧化剂)∶n(还原剂)=1∶1 | B.n(氧化剂)∶n(还原剂)=1∶2 |
| C.氧化性:NaClO>Cl2 | D.Cl2既是氧化产物又是还原产物 |
 ),需将其转化为Cl-除去,下列试剂中可将ClO
),需将其转化为Cl-除去,下列试剂中可将ClO 转化为Cl-的是
转化为Cl-的是| A.O3 | B.FeSO4 | C.KI | D.KMnO4 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】按要求书写方程式
(1) 在水溶液中的电离方程式
在水溶液中的电离方程式___________ 。
(2)碳酸钙溶解在醋酸中的离子反应方程式___________ 。
(3)除去 粉末中混有少量
粉末中混有少量 的化学方程式
的化学方程式___________ 。
(4)“84”消毒液与除垢剂(有效成分是盐酸)混合使用会产生黄绿色、有刺激性气味的气体,该反应的离子方程式是___________ 。
(5)衣服上不小心沾到了蓝色墨水,可以先涂上酸性高锰酸钾溶液,即可除去蓝墨水中的鞣酸亚铁,再用乙二酸的稀溶液擦洗,可以迅速除去过量的高锰酸钾,配平该反应的离子方程式:________ 。

(1)
 在水溶液中的电离方程式
在水溶液中的电离方程式(2)碳酸钙溶解在醋酸中的离子反应方程式
(3)除去
 粉末中混有少量
粉末中混有少量 的化学方程式
的化学方程式(4)“84”消毒液与除垢剂(有效成分是盐酸)混合使用会产生黄绿色、有刺激性气味的气体,该反应的离子方程式是
(5)衣服上不小心沾到了蓝色墨水,可以先涂上酸性高锰酸钾溶液,即可除去蓝墨水中的鞣酸亚铁,再用乙二酸的稀溶液擦洗,可以迅速除去过量的高锰酸钾,配平该反应的离子方程式:

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】人体必需的一些元素在周期表中的分布情况如下:

(1)请在上图中画出金属与非金属的分界线_______ 。
(2)Na与O形成的原子个数比为1:1的化合物所含的化学键类型为_______ 。
(3)锡(Sn)与C为同一主族元素,Sn原子比C原子多三个电子层,则Sn的原子序数为_______ 。
(4)X射线衍射法可以测定某些分子的结构,下列分子结构模型中正确的是_______ (填字母)。
(5)前四周期同族元素的某种性质X随核电荷数的变化趋势如图所示,则下列说法正确的是_______(填字母)。

(6)铬是胰岛素不可缺少的辅助成分,但食用不当也会带来很大的危害。六价铬的化合物有剧毒,所以要对Cr(VI)(罗马数字表示元素的化合价,下同)废水进行化学处理,可转化为重要产品磁性铁铬氧体(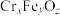 ):先向含
):先向含 的污水中加入适量的硫酸及硫酸亚铁,待充分反应后再通入适量空气(氧化部分
的污水中加入适量的硫酸及硫酸亚铁,待充分反应后再通入适量空气(氧化部分 )并加入NaOH,就可以使铬、铁元素全部转化为磁性铁铬氧体。
)并加入NaOH,就可以使铬、铁元素全部转化为磁性铁铬氧体。
①写出 在酸性条件下被
在酸性条件下被 还原为
还原为 的离子方程式:
的离子方程式:_______ 。
②若处理含1mol (不考虑其他含铬微粒)的污水时恰好消耗10mol
(不考虑其他含铬微粒)的污水时恰好消耗10mol ,则当铁铬氧体中
,则当铁铬氧体中 时,铁铬氧体的化学式为
时,铁铬氧体的化学式为_______ 。

(1)请在上图中画出金属与非金属的分界线
(2)Na与O形成的原子个数比为1:1的化合物所含的化学键类型为
(3)锡(Sn)与C为同一主族元素,Sn原子比C原子多三个电子层,则Sn的原子序数为
(4)X射线衍射法可以测定某些分子的结构,下列分子结构模型中正确的是
| A | B | C | D |
| HCl |  |  |  |
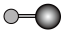 |  | 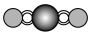 | 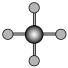 |
| 直线形 | 直线形 | 直线形 | 平面正方形 |

| A.若a、b、c表示碱金属元素,则X表示对应单质的密度 |
| B.若a、b、c表示卤族元素,则X表示对应简单离子的还原性 |
| C.若a、b、c表示氧族元素,则X表示对应氢化物的稳定性 |
| D.若a、b、c表示第IIA族元素,则X表示最高价氧化物对应水化物的碱性 |
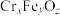 ):先向含
):先向含 的污水中加入适量的硫酸及硫酸亚铁,待充分反应后再通入适量空气(氧化部分
的污水中加入适量的硫酸及硫酸亚铁,待充分反应后再通入适量空气(氧化部分 )并加入NaOH,就可以使铬、铁元素全部转化为磁性铁铬氧体。
)并加入NaOH,就可以使铬、铁元素全部转化为磁性铁铬氧体。①写出
 在酸性条件下被
在酸性条件下被 还原为
还原为 的离子方程式:
的离子方程式:②若处理含1mol
 (不考虑其他含铬微粒)的污水时恰好消耗10mol
(不考虑其他含铬微粒)的污水时恰好消耗10mol ,则当铁铬氧体中
,则当铁铬氧体中 时,铁铬氧体的化学式为
时,铁铬氧体的化学式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】如图为钠和氯的价类二维图,请据图完成下列问题:
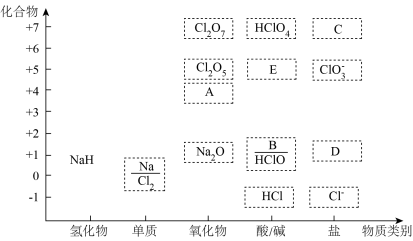
(1)NaH中的氢为___________ 价。可与水反应生成氢气,该反应中氧化产物和还原产物的质量比为___________ 。
(2)A是氯的氧化物,其化学式为___________ 。A可用于自来水消毒。其消毒效率是 的
的___________ 倍(还原产物都是 ,消毒效率以单位物质的量的物质得到的电子数表示)。
,消毒效率以单位物质的量的物质得到的电子数表示)。
(3)B属于碱,其水溶液与 反应生成D的离子方程式为
反应生成D的离子方程式为___________ 。
(4)C是高氯酸钠,受热分解可产生 和非含氧酸盐,则高氯酸钠热分解的化学方程式为
和非含氧酸盐,则高氯酸钠热分解的化学方程式为___________ 。
(5) 可与水反应生成
可与水反应生成 ,
, 生成E也是发生类似的反应,请写出
生成E也是发生类似的反应,请写出 与B在水中生成
与B在水中生成 的离子反应方程式
的离子反应方程式___________ 。

(1)NaH中的氢为
(2)A是氯的氧化物,其化学式为
 的
的 ,消毒效率以单位物质的量的物质得到的电子数表示)。
,消毒效率以单位物质的量的物质得到的电子数表示)。(3)B属于碱,其水溶液与
 反应生成D的离子方程式为
反应生成D的离子方程式为(4)C是高氯酸钠,受热分解可产生
 和非含氧酸盐,则高氯酸钠热分解的化学方程式为
和非含氧酸盐,则高氯酸钠热分解的化学方程式为(5)
 可与水反应生成
可与水反应生成 ,
, 生成E也是发生类似的反应,请写出
生成E也是发生类似的反应,请写出 与B在水中生成
与B在水中生成 的离子反应方程式
的离子反应方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】下图是氯的“价类二维图”,请根据所学回答下列问题:

(1)已知A、H均为一元酸,写出A、H的化学式:___________ 、___________ 。
(2)写出B物质的一种用途:___________ 。
(3)洁厕灵溶于水会有A物质生成,物质F为84消毒液的有效成分,当洗洁过程中两者混合使用,可能会发生中毒事件,试用离子方程式说明原因:___________ 。
(4)物质D是一种比氯气更优的消毒剂,它的消毒能力(每摩尔消毒剂得电子数的多少)是氯气的___________ 倍(已知两种消毒剂均被还原为 )。
)。

(1)已知A、H均为一元酸,写出A、H的化学式:
(2)写出B物质的一种用途:
(3)洁厕灵溶于水会有A物质生成,物质F为84消毒液的有效成分,当洗洁过程中两者混合使用,可能会发生中毒事件,试用离子方程式说明原因:
(4)物质D是一种比氯气更优的消毒剂,它的消毒能力(每摩尔消毒剂得电子数的多少)是氯气的
 )。
)。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】无水AlCl3可用作有机合成的催化剂,食品膨松剂等。已知AlCl3、FeCl3分别在183℃、315℃时升华,无水AlCl3遇潮湿空气即产生大量白雾。
I.工业上由铝土矿(主要成分是Al2O3和Fe2O3)和石油焦(主要成分是碳单质)制备无水AlCl3的流程如下:

(1)焙烧炉中发生反应:①Fe2O3(s)+3C(s) 2Fe(s) +3CO(g);
2Fe(s) +3CO(g);
②3CO(g)+Fe2O3(s) 2Fe(s)+3CO2(g)
2Fe(s)+3CO2(g)
则反应②的平衡常数的表达式为K=_____ 。
(2)氯化炉中Al2O3、Cl2和C在高温下发生反应的化学方程式为_____ ;炉气中含有大量CO和少量Cl2,可用Na2SO3溶液除去Cl2,其离子方程式为____ 。
(3)精制无水AlCl3的合格品中,AlCl3的质量分数不得低于96%。现称取16.25g精制后的无水AlCl3样品,溶于过量的NaOH溶液,过滤出沉淀物,沉淀物经洗涤、灼烧、冷却、称重,其残留固体质量为0.16g。该样品中AlCl3的质量分数为_____ 。
II.实验室可用下列装置制备无水AlCl3。装置B、C中应盛放的试剂名称分别为_____ 、_____ ,F中所盛放试剂的作用是_____ 。

I.工业上由铝土矿(主要成分是Al2O3和Fe2O3)和石油焦(主要成分是碳单质)制备无水AlCl3的流程如下:

(1)焙烧炉中发生反应:①Fe2O3(s)+3C(s)
 2Fe(s) +3CO(g);
2Fe(s) +3CO(g);②3CO(g)+Fe2O3(s)
 2Fe(s)+3CO2(g)
2Fe(s)+3CO2(g)则反应②的平衡常数的表达式为K=
(2)氯化炉中Al2O3、Cl2和C在高温下发生反应的化学方程式为
(3)精制无水AlCl3的合格品中,AlCl3的质量分数不得低于96%。现称取16.25g精制后的无水AlCl3样品,溶于过量的NaOH溶液,过滤出沉淀物,沉淀物经洗涤、灼烧、冷却、称重,其残留固体质量为0.16g。该样品中AlCl3的质量分数为
II.实验室可用下列装置制备无水AlCl3。装置B、C中应盛放的试剂名称分别为

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】某校化学研究性学习小组要利用已经学过的化学知识制取少量漂白粉,并进一步探究漂白粉的化学性质。他们查阅资料得知:2Cl2+2Ca(OH)2=Ca(ClO)2+CaCl2+2H2O是放热反应,温度稍高时便发生副反应:6Cl2+6Ca(OH)2=Ca(ClO3)2+5CaCl2+6H2O。某学生设计出了甲、乙、丙三套装置:

(1)请从甲、乙、丙各套装置中选取合理的部分,按气体从左至右的流向组装成一套较合理的装置(填各部分仪器的编号)____ 。
(2)部分学生认为上述组装仍存在缺点,他们指出在前两个仪器之间应增加如图装置:
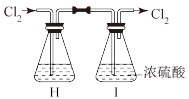
你认为H洗气瓶中所盛液体是____ ,其作用是____ 。若无此装置,对制漂白粉有什么不利影响____ ;洗气瓶I有无必要理由是____ 。

(1)请从甲、乙、丙各套装置中选取合理的部分,按气体从左至右的流向组装成一套较合理的装置(填各部分仪器的编号)
(2)部分学生认为上述组装仍存在缺点,他们指出在前两个仪器之间应增加如图装置:

你认为H洗气瓶中所盛液体是
您最近一年使用:0次



