用双线桥法标出下列反应的电子转移情况和化合价升降情况
Fe+H2SO4=FeSO4+H2↑_____________________________________
Fe+H2SO4=FeSO4+H2↑
10-11高一上·山西吕梁·期中 查看更多[1]
(已下线)2010年山西省汾阳中学高一上学期期中考试化学试卷
更新时间:2010-12-13 11:09:48
|
相似题推荐
【推荐1】回答下列问题:
(1)下列微粒:①S②SO ③Fe2+④Al3+⑤Na⑥HCl⑦Na2O2。在化学反应中只能被氧化的是
③Fe2+④Al3+⑤Na⑥HCl⑦Na2O2。在化学反应中只能被氧化的是___ (填序号),只能表现出氧化性的是___ (填序号)。
(2)在一定条件下,实验室分别以过氧化氢、高锰酸钾、氯酸钾、过氧化钠为原料制取氧气,当制得相同质量的氧气时,四个反应中转移的电子数之比为___ 。
(3)自来水中的NO 对人类健康产生危害。为了降低自来水中NO
对人类健康产生危害。为了降低自来水中NO 的浓度,某研究人员提出在碱性条件下用Al粉还原NO
的浓度,某研究人员提出在碱性条件下用Al粉还原NO ,产物是N2。发生的反应可表示如下,请完成方程式的配平
,产物是N2。发生的反应可表示如下,请完成方程式的配平___ 。
Al+ NO + OH-→ AlO
+ OH-→ AlO + N2↑+ H2O
+ N2↑+ H2O
(4)把Cl2通入浓氨水中,发生如下反应:3Cl2+8NH3=6NH4Cl+N2。
①用双线桥表示反应的电子转移方向和数目:___ 。
②反应中发生电子转移的Cl2与NH3的分子数之比为:___ 。
(1)下列微粒:①S②SO
 ③Fe2+④Al3+⑤Na⑥HCl⑦Na2O2。在化学反应中只能被氧化的是
③Fe2+④Al3+⑤Na⑥HCl⑦Na2O2。在化学反应中只能被氧化的是(2)在一定条件下,实验室分别以过氧化氢、高锰酸钾、氯酸钾、过氧化钠为原料制取氧气,当制得相同质量的氧气时,四个反应中转移的电子数之比为
(3)自来水中的NO
 对人类健康产生危害。为了降低自来水中NO
对人类健康产生危害。为了降低自来水中NO 的浓度,某研究人员提出在碱性条件下用Al粉还原NO
的浓度,某研究人员提出在碱性条件下用Al粉还原NO ,产物是N2。发生的反应可表示如下,请完成方程式的配平
,产物是N2。发生的反应可表示如下,请完成方程式的配平Al+ NO
 + OH-→ AlO
+ OH-→ AlO + N2↑+ H2O
+ N2↑+ H2O(4)把Cl2通入浓氨水中,发生如下反应:3Cl2+8NH3=6NH4Cl+N2。
①用双线桥表示反应的电子转移方向和数目:
②反应中发生电子转移的Cl2与NH3的分子数之比为:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】下图为铁及其化合物的“价-类”二维图。
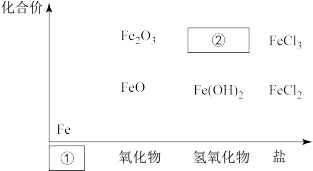
(1)填写二维图缺失的类别①___________ 和化学式②___________ 。
(2)某同学利用以下试剂研究 性质,进行了如下预测:
性质,进行了如下预测:
① ②Fe ③NaOH ④
②Fe ③NaOH ④ ⑤
⑤
从物质类别上看, 属于
属于___________ ,可能与___________ 发生反应(填序号)﹔
从化合价角度看, 具有
具有___________ 性,可能与___________ 发生反应(填序号)。
(3)某工厂用 溶液腐蚀镀有铜的绝缘板生产印刷电路,其化学原理为如下反应:
溶液腐蚀镀有铜的绝缘板生产印刷电路,其化学原理为如下反应:
①用双线桥表示电子转移________ 。
②写出该反应的离子方程式___________
(4)工业废水中含有的重铬酸根离子( )有毒,必须处理达标后才能排放。工业上常用绿矾(
)有毒,必须处理达标后才能排放。工业上常用绿矾( )做处理剂,反应的离子方程式如下:
)做处理剂,反应的离子方程式如下: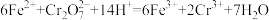 。并用单线桥法标出方程式中电子转移的方向和数目
。并用单线桥法标出方程式中电子转移的方向和数目___________ ;在该反应中,还原剂是___________ (填离子符号,下同),还原产物是___________ 。

(1)填写二维图缺失的类别①
(2)某同学利用以下试剂研究
 性质,进行了如下预测:
性质,进行了如下预测:①
 ②Fe ③NaOH ④
②Fe ③NaOH ④ ⑤
⑤
从物质类别上看,
 属于
属于从化合价角度看,
 具有
具有(3)某工厂用
 溶液腐蚀镀有铜的绝缘板生产印刷电路,其化学原理为如下反应:
溶液腐蚀镀有铜的绝缘板生产印刷电路,其化学原理为如下反应:
①用双线桥表示电子转移
②写出该反应的离子方程式
(4)工业废水中含有的重铬酸根离子(
 )有毒,必须处理达标后才能排放。工业上常用绿矾(
)有毒,必须处理达标后才能排放。工业上常用绿矾( )做处理剂,反应的离子方程式如下:
)做处理剂,反应的离子方程式如下: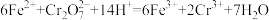 。并用单线桥法标出方程式中电子转移的方向和数目
。并用单线桥法标出方程式中电子转移的方向和数目
您最近一年使用:0次
【推荐3】Ⅰ.(1)等质量的二氧化硫和二氧化碳,它们的物质的量之比___ ,所含原子数之比为___ ,同温同压下的密度之比为___ 。
(2)有氢原子数相等的甲烷和氨气(NH3)的质量之比为___ 。
(3)3.22g的Na2SO4·10H2O溶于水中,要使每100个分子中含有1个Na+,则需要水的质量为___ 。
(4)同温同压下某容器充满氮气重64g,充满氦气重52g,现在充满某气体重66g,则该气体的摩尔质量为___ 。
Ⅱ.(1)油画所用颜料含有某种白色铅化物,此颜料置于空气中长时间后就会变成黑色PbS,从而使油画的色彩变暗,若用双氧水H2O2来清洗,则可将PbS变成PbSO4,从而使油画复原。上述清洗反应的化学方程式为PbS+4H2O2=PbSO4+4M(已配平)。
生成物M的化学式为___ ;若发生转移的电子数目4mol时,参加反应的H2O2的质量为___ 。
(2)在反应2KMnO4+16HCl=2KCl+2MnCl2+5Cl2+8H2O中,氧化剂是___ ,氧化产物是___ ,氧化产物与还原产物物质的量之比是___ ,氧化剂和还原剂的物质的量之比为___ ,若有36.5gHCl被氧化,则产生Cl2的质量为___ 。
(3)2.3g的金属钠,在干燥的空气中被氧化后得到固体的质量为3.5g,则反应后固体中氧化钠的质量为___ 。
(4)配平下列方程式并用单线桥表示电子的转移(不需写出配平过程)___
Cu+HNO3(稀)=Cu(NO3)2+NO↑+H2O
(2)有氢原子数相等的甲烷和氨气(NH3)的质量之比为
(3)3.22g的Na2SO4·10H2O溶于水中,要使每100个分子中含有1个Na+,则需要水的质量为
(4)同温同压下某容器充满氮气重64g,充满氦气重52g,现在充满某气体重66g,则该气体的摩尔质量为
Ⅱ.(1)油画所用颜料含有某种白色铅化物,此颜料置于空气中长时间后就会变成黑色PbS,从而使油画的色彩变暗,若用双氧水H2O2来清洗,则可将PbS变成PbSO4,从而使油画复原。上述清洗反应的化学方程式为PbS+4H2O2=PbSO4+4M(已配平)。
生成物M的化学式为
(2)在反应2KMnO4+16HCl=2KCl+2MnCl2+5Cl2+8H2O中,氧化剂是
(3)2.3g的金属钠,在干燥的空气中被氧化后得到固体的质量为3.5g,则反应后固体中氧化钠的质量为
(4)配平下列方程式并用单线桥表示电子的转移(不需写出配平过程)
Cu+HNO3(稀)=Cu(NO3)2+NO↑+H2O
您最近一年使用:0次
【推荐1】认识氧化还原反应,根据所学知识填空:
(1)氧化还原反应的特征是___________ ;氧化还原反应的本质是___________ 。
对于反应MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
(2)MnO2中的Mn元素化合价___________ (填“升高”或“降低”),在反应中___________ 电子(填“得到”或“失去”),发生___________ 反应(填“氧化”或“还原”)。
(3)HCl中的Cl元素化合价___________ (填“升高”或“降低”),在反应中___________ 电子(填“得到”或“失去”),发生___________ 反应(填“氧化”或“还原”)。
(1)氧化还原反应的特征是
对于反应MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O(2)MnO2中的Mn元素化合价
(3)HCl中的Cl元素化合价
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】物质的分类是学习化学的一种重要方法,科学合理的分类对于提高学习效率、解决问题都有着重要的意义。请回答下列问题:
I.纯净物根据其组成和性质有如图分类形式

(1)图中所示所属的分类方法为_______
(2)下列物质能导电的是_______ (填数字序号,下同),属于混合物的有_______ ,属于电解质的是_______ 。
①NaCl晶体 ②CO2 ③K2CO3溶液 ④铜 ⑤CaCO3固体 ⑥乙醇 ⑦氨水 ⑧稀硫酸 ⑨熔化的NaHSO4
(3)写出NaHSO4在水溶液中的电离方程式_______ 。
(4)写出③和⑧反应的离子方程式_______ 。
II.我们可以从不同角度认识化学反应,四种基本反应类型与氧化还原反应的关系如图所示。

(5)下列化学反应属于阴影区域的是_______
A. SO2+H2O2=H2SO4
B. 3CO+Fe2O3 2Fe+3CO2
2Fe+3CO2
C. 2Na2O2+2H2O=4NaOH+O2↑
D.Br2+2KI=I2+2KBr
E. 2Fe(OH)3 Fe2O3+3H2O
Fe2O3+3H2O
I.纯净物根据其组成和性质有如图分类形式

(1)图中所示所属的分类方法为
(2)下列物质能导电的是
①NaCl晶体 ②CO2 ③K2CO3溶液 ④铜 ⑤CaCO3固体 ⑥乙醇 ⑦氨水 ⑧稀硫酸 ⑨熔化的NaHSO4
(3)写出NaHSO4在水溶液中的电离方程式
(4)写出③和⑧反应的离子方程式
II.我们可以从不同角度认识化学反应,四种基本反应类型与氧化还原反应的关系如图所示。

(5)下列化学反应属于阴影区域的是
A. SO2+H2O2=H2SO4
B. 3CO+Fe2O3
 2Fe+3CO2
2Fe+3CO2C. 2Na2O2+2H2O=4NaOH+O2↑
D.Br2+2KI=I2+2KBr
E. 2Fe(OH)3
 Fe2O3+3H2O
Fe2O3+3H2O
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】分类是研究物质性质的常用方法,有价值的分类会带来物质认识的独特视角。下表是生产生活中常见的物质。
(1)①~⑥中属于电解质的是___________ (填编号,下同),该状态下能导电的有___________ 。
(2)从物质类别角度分析,⑥属于___________ (填"酸"或"碱"或"盐"),因其受热分解产生气体,常用作膨松剂,写出相关化学方程式___________ 。
(3)从氮元素化合价角度分析,②可能具有的性质___________ (填序号)。
a.只有氧化性 b.既有氧化性又有还原性
c.只有还原性 d.既无氧化性也无还原性
(4)将④的水溶液与⑤混合,反应的离子方程式为___________ 。
| 编号 | ① | ② | ③ | ④ | ⑤ | ⑥ |
| 物质 | 酒精(CH3CH2OH) | 亚硝酸钠晶体(NaNO2) | 铜丝 | 液氨 | 稀硫酸 | 小苏打粉末 |
(1)①~⑥中属于电解质的是
(2)从物质类别角度分析,⑥属于
(3)从氮元素化合价角度分析,②可能具有的性质
a.只有氧化性 b.既有氧化性又有还原性
c.只有还原性 d.既无氧化性也无还原性
(4)将④的水溶液与⑤混合,反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】用双线桥法标出下列反应中电子转移的方向和数目:
3Cu + 2NO3— + 8H+ 3Cu2+ + 2NO↑ + 4H2O
3Cu2+ + 2NO↑ + 4H2O __________________
(1)此反应中,还原剂是_____ ,氧化剂是 _____ ;__ 元素被还原。
(2)由此可知,氧化还原反应的实质是__________________________ 。
(3)据你的理解再写一个常见的氧化还原反应的化学方程式:_________________ 。
3Cu + 2NO3— + 8H+
 3Cu2+ + 2NO↑ + 4H2O
3Cu2+ + 2NO↑ + 4H2O (1)此反应中,还原剂是
(2)由此可知,氧化还原反应的实质是
(3)据你的理解再写一个常见的氧化还原反应的化学方程式:
您最近一年使用:0次
【推荐2】回答下列问题:
(1)下列微粒:①S ② ③Fe2+ ④Al3+ ⑤Na ⑥HCl ⑦Na2O2,只能表现出氧化性的是
③Fe2+ ④Al3+ ⑤Na ⑥HCl ⑦Na2O2,只能表现出氧化性的是_____ (填序号)。
(2)在一定条件下,实验室分别以过氧化氢、高锰酸钾、氯酸钾、过氧化钠为原料制取氧气,当制得相同质量的氧气时,四个反应中转移的电子数之比为_____ 。
(3)把Cl2通入浓氨水中,发生如下反应:3Cl2+8NH3=6NH4Cl+N2。
①用双线桥法表示反应的电子转移方向和数目_____ 。
②反应中被还原的Cl2与被氧化的NH3的分子数之比为:____ 。
(4)下列三个氧化还原反应中,反应③中盐酸表现的性质是:____ 。
①2FeCl3+2KI=2FeCl2+2KCl+I2
②2FeCl2+Cl2=2FeCl3
③2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
若溶液中Cl-与I-共存,为了氧化I-而Cl-不被氧化,除Cl2单质外,还可应用上述反应中的____ 作氧化剂。
(1)下列微粒:①S ②
 ③Fe2+ ④Al3+ ⑤Na ⑥HCl ⑦Na2O2,只能表现出氧化性的是
③Fe2+ ④Al3+ ⑤Na ⑥HCl ⑦Na2O2,只能表现出氧化性的是(2)在一定条件下,实验室分别以过氧化氢、高锰酸钾、氯酸钾、过氧化钠为原料制取氧气,当制得相同质量的氧气时,四个反应中转移的电子数之比为
(3)把Cl2通入浓氨水中,发生如下反应:3Cl2+8NH3=6NH4Cl+N2。
①用双线桥法表示反应的电子转移方向和数目
②反应中被还原的Cl2与被氧化的NH3的分子数之比为:
(4)下列三个氧化还原反应中,反应③中盐酸表现的性质是:
①2FeCl3+2KI=2FeCl2+2KCl+I2
②2FeCl2+Cl2=2FeCl3
③2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
若溶液中Cl-与I-共存,为了氧化I-而Cl-不被氧化,除Cl2单质外,还可应用上述反应中的
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】按要求完成下列试题
(1)用单线桥标出下列反应电子转移的方向和数目
2Na+2H2O=2NaOH+H2↑____
(2)用双线桥标出下列反应化合价升降、电子得失、被氧化或被还原
C+2H2SO4(浓) CO2↑+2SO2↑+2H2O
CO2↑+2SO2↑+2H2O_____
(3)写出下列物质在水溶液中的电离方程式。
CH3COOH:_________ 。
KAl(SO4)2:_______________ 。
(4)写出硫酸铜溶液与氢氧化钡溶液反应的离子方程式:__________
(1)用单线桥标出下列反应电子转移的方向和数目
2Na+2H2O=2NaOH+H2↑
(2)用双线桥标出下列反应化合价升降、电子得失、被氧化或被还原
C+2H2SO4(浓)
 CO2↑+2SO2↑+2H2O
CO2↑+2SO2↑+2H2O(3)写出下列物质在水溶液中的电离方程式。
CH3COOH:
KAl(SO4)2:
(4)写出硫酸铜溶液与氢氧化钡溶液反应的离子方程式:
您最近一年使用:0次



