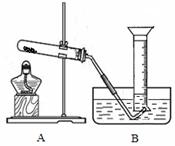
掌握仪器的名称、组装及使用方法是中学化学实验的基础,右图为两套实验装置。
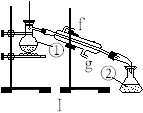
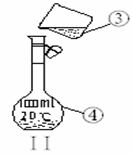
(1)写出下列仪器的名称:
①____________ ;②____________ ;④__________ ;
(2)仪器①~④中,使用时必须检查是否漏水的有________________ ;图I实验过程中使用冷凝管时应从____________ 处进水(均填序号)。
(3)若利用装置I分离四氯化碳和酒精的混合物,还缺少的仪器有___________ ;将仪器补充完整后进行的实验操作的名称为:_______________ 。现需配制500 ml 0.2 mol/L NaCl溶液,装置II是某同学转移溶液的示意图,图中的错误是 ________________ 。


(1)写出下列仪器的名称:
①
(2)仪器①~④中,使用时必须检查是否漏水的有
(3)若利用装置I分离四氯化碳和酒精的混合物,还缺少的仪器有
更新时间:2016-12-09 17:30:25
|
相似题推荐
解答题-实验探究题
|
较难
(0.4)
【推荐1】硫酸铜受热分解生成氧化铜和气体,受热温度不同,该气体成分也不同。气体成分可能含SO2、SO3和O2中的一种、二种或三种。某化学课外活动小组通过设计一探究性实验,探索测定反应产生的SO2、SO3和O2的物质的量,并经计算确定各物质的化学计量数,从而确定CuSO4分解的化学方程式。实验可能用到的仪器如下图所示:
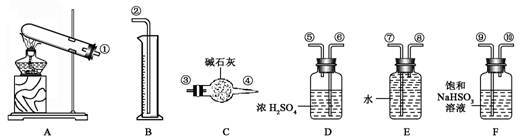
【提出猜想】
Ⅰ.所得气体的成分可能只含_________ 一种;
Ⅱ.所得气体的成分可能含有____________ 二种;
Ⅲ.所得气体的成分可能含有________________ 三种。
【实验探究】
实验操作过程(略)。已知实验结束时,硫酸铜完全分解。请回答下列问题:
(1)请你组装探究实验的装置,按从左至右的方向,各仪器接口连接顺序为:____________ 填序号)
(2)若实验结束,B中量筒没有收集到水,则证明猜想________ 正确。
(3)若实验结束,经测定装置C的总质量增加了,能否肯定气体产物中含有SO2而不含SO3?
请说明理由。答:__________________________________________________________
(4)有两个实验小组进行该实验,由于加热时的温度不同,实验结束后,测得相关数据也不同,数据如下:
请通过计算,推断出第一小组和第二小组的实验条件下CuSO4分解的化学反应方程式:
一组:__________________________________________________________ ;
二组:__________________________________________________________ 。
(5)该实验设计中,由于实验操作的原因容易给测定带来最大误差的两个仪器是________ 和_______ (填代号)。

【提出猜想】
Ⅰ.所得气体的成分可能只含
Ⅱ.所得气体的成分可能含有
Ⅲ.所得气体的成分可能含有
【实验探究】
实验操作过程(略)。已知实验结束时,硫酸铜完全分解。请回答下列问题:
(1)请你组装探究实验的装置,按从左至右的方向,各仪器接口连接顺序为:
(2)若实验结束,B中量筒没有收集到水,则证明猜想
(3)若实验结束,经测定装置C的总质量增加了,能否肯定气体产物中含有SO2而不含SO3?
请说明理由。答:
(4)有两个实验小组进行该实验,由于加热时的温度不同,实验结束后,测得相关数据也不同,数据如下:
| 实验小组 | 称取CuSO4 的质量(g) | 装置C增加 的质量(g) | 量筒中水的体积折算成标 准状况下气体的体积(mL) |
| 一 | 6.4 | 2.56 | 298.7 |
| 二 | 6.4 | 2.56 | 448 |
一组:
二组:
(5)该实验设计中,由于实验操作的原因容易给测定带来最大误差的两个仪器是
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐2】设计如下实验探究某矿石(仅含四种短周期元素)的组成和性质,已知矿石含有一定的结晶水:
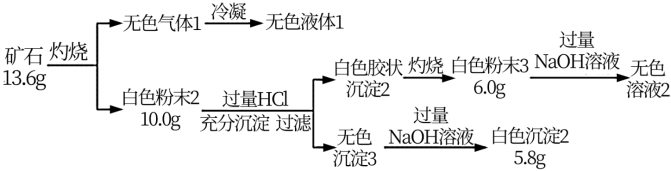
(1)矿石的组成元素是 H、O 和_____ 、 ______ (填元素符号),化学式为_____________ 。
(2)白色粉末3 溶于NaOH溶液的离子方程式是________ 。

(1)矿石的组成元素是 H、O 和
(2)白色粉末3 溶于NaOH溶液的离子方程式是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐3】某研究性实验小组欲验证浓硝酸在与Cu、Ag合金的反应过程中除生成NO2气体外,还会有少量NO生成、并测定Cu、Ag合金中Cu的质量分数。为此,他们设计了如图所示的装置。(已知:NO2的沸点为21℃;NO的沸点为-152℃)
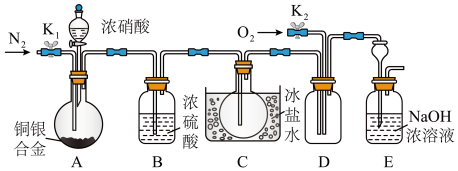
(1)写出A中Ag与硝酸反应的一个离子方程式___ 。
(2)反应前要先打开活塞K1持续通入一段时间的N2,其理由是___ ,若缺少装置B,对实验的影响是___ 。
(3)确认A中有NO生成,依据的现象是___ 。
(4)若已知Cu、Ag合金的质量为mg,且溶解完全只利用A装置中反应后的溶液进行简单的操作,即可以确定合金中Cu的质量分数,其实验操作过程为___ 。
(5)只将铜片直接放入浓硝酸中:
①实验现象为___ 。
②待反应停止后,若铜有剩余,再加入少量25%的稀硫酸,这时铜片上又有气泡产生,原因是__ (用离子方程式表示)。
③若将12.8g铜跟一定量的浓硝酸反应,铜耗完时,共产生气体5.6L(标况)。则所消耗硝酸的物质的量是___ mol。

(1)写出A中Ag与硝酸反应的一个离子方程式
(2)反应前要先打开活塞K1持续通入一段时间的N2,其理由是
(3)确认A中有NO生成,依据的现象是
(4)若已知Cu、Ag合金的质量为mg,且溶解完全只利用A装置中反应后的溶液进行简单的操作,即可以确定合金中Cu的质量分数,其实验操作过程为
(5)只将铜片直接放入浓硝酸中:
①实验现象为
②待反应停止后,若铜有剩余,再加入少量25%的稀硫酸,这时铜片上又有气泡产生,原因是
③若将12.8g铜跟一定量的浓硝酸反应,铜耗完时,共产生气体5.6L(标况)。则所消耗硝酸的物质的量是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐1】过氧化钙是一种重要的化工原料,温度在350℃以上容易分解。
(1)利用反应Ca(s)+O2 CaO2(s),在纯氧条件下,制取CaO2的装置示意图如下:
CaO2(s),在纯氧条件下,制取CaO2的装置示意图如下:

请回答下列问题:
①装置A中反应的化学方程式为____________;仪器a的名称为__________;装置D中盛有的液体是浓硫酸,其作用一是观察氧气的流速,判断氧气通入是否过快及氧气与钙反应进行的程度;二是_______________。仪器安装后应进行的实验操作:
a.通入氧气
b.检查装置气密性
c.加入药品
d.停止通氧气
e.点燃酒精灯
f.熄灭酒精灯
g.冷却至室温,
正确的操作顺序为________。
②完全反应后,有关数据记录如下:
据此可判断m2与理论值不符,则产物中的杂质可能是_________________________。
(2)利用反应Ca2++H2O2+2NH3·H2O+6H2O=CaO2·8H2O+2NH4+,在碱性环境中,制取CaO2的流程示意图如下:

请回答下列问题:
①主反应中,NH3·H2O在Ca2+和H2O2的反应历程中所起的作用是_______________;该反应所需的条件及操作为_______(填字母)。
a.把氯化钙溶液逐滴加入过氧化氢—氨水溶液中
b.把过氧化氢—氨水溶液逐滴加入氯化钙溶液中
c.滴加时先搅拌后静置,观察晶体析出
d.滴加时不停搅拌,直至晶体完全析出
e.反应体系热水浴加热 f.反应体系冰水浴冷却
洗涤CaO2·8H2O晶体时,判断晶体是否完全洗净的试剂为_____;滤液循环使用时需在反应器中加入一种物质,该物质的化学式为_____。
②利用反应2CaO2 2CaO+O2↑测量产品中CaO2含量时,停止反应且冷却至25℃后的装置示意图如下:若直接读数确定25℃、1大气压下气体的体积,则测量结果______(填“偏大”、“偏小”或“无影响”)。
2CaO+O2↑测量产品中CaO2含量时,停止反应且冷却至25℃后的装置示意图如下:若直接读数确定25℃、1大气压下气体的体积,则测量结果______(填“偏大”、“偏小”或“无影响”)。
(1)利用反应Ca(s)+O2
 CaO2(s),在纯氧条件下,制取CaO2的装置示意图如下:
CaO2(s),在纯氧条件下,制取CaO2的装置示意图如下:
请回答下列问题:
①装置A中反应的化学方程式为____________;仪器a的名称为__________;装置D中盛有的液体是浓硫酸,其作用一是观察氧气的流速,判断氧气通入是否过快及氧气与钙反应进行的程度;二是_______________。仪器安装后应进行的实验操作:
a.通入氧气
b.检查装置气密性
c.加入药品
d.停止通氧气
e.点燃酒精灯
f.熄灭酒精灯
g.冷却至室温,
正确的操作顺序为________。
②完全反应后,有关数据记录如下:
| 空瓷舟质量m0/g | 瓷舟与钙的质量m1/g | 瓷舟与产物的质量m2/g |
| 14.80 | 15.08 | 15.25 |
(2)利用反应Ca2++H2O2+2NH3·H2O+6H2O=CaO2·8H2O+2NH4+,在碱性环境中,制取CaO2的流程示意图如下:

请回答下列问题:
①主反应中,NH3·H2O在Ca2+和H2O2的反应历程中所起的作用是_______________;该反应所需的条件及操作为_______(填字母)。
a.把氯化钙溶液逐滴加入过氧化氢—氨水溶液中
b.把过氧化氢—氨水溶液逐滴加入氯化钙溶液中
c.滴加时先搅拌后静置,观察晶体析出
d.滴加时不停搅拌,直至晶体完全析出
e.反应体系热水浴加热 f.反应体系冰水浴冷却
洗涤CaO2·8H2O晶体时,判断晶体是否完全洗净的试剂为_____;滤液循环使用时需在反应器中加入一种物质,该物质的化学式为_____。
②利用反应2CaO2
 2CaO+O2↑测量产品中CaO2含量时,停止反应且冷却至25℃后的装置示意图如下:若直接读数确定25℃、1大气压下气体的体积,则测量结果______(填“偏大”、“偏小”或“无影响”)。
2CaO+O2↑测量产品中CaO2含量时,停止反应且冷却至25℃后的装置示意图如下:若直接读数确定25℃、1大气压下气体的体积,则测量结果______(填“偏大”、“偏小”或“无影响”)。
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐2】某学习小组在研究CH4还原Fe2O3的实验中,发现生成的黑色粉末能被磁铁吸引。查阅资料得知:在温度不同、受热不均时会生成具有磁性的Fe3O4。为进一步探究黑色粉末的组成及含量,他们进行如下实验。
(1)往黑色粉末中滴加盐酸,观察到有气泡产生,则黑色粉末中一定有___________ ;
(2)用以下装置可以说明产物有Fe3O4存在:检查装置的气密性,往装置中添加相应的药品,接下来的一步操作为_______________________________ 。
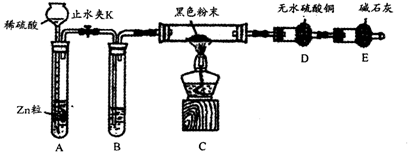
(3)为进一步证明黑色粉末是否含Fe3O4,某同学设计实验方案如下:取少量黑色粉末于试管,加足量盐酸,充分振荡使黑色粉末完全溶解,滴入KSCN溶液,观察现象。请分析此方案是否可行,并解释原因。______________________________________ 。
(1)往黑色粉末中滴加盐酸,观察到有气泡产生,则黑色粉末中一定有
(2)用以下装置可以说明产物有Fe3O4存在:检查装置的气密性,往装置中添加相应的药品,接下来的一步操作为

(3)为进一步证明黑色粉末是否含Fe3O4,某同学设计实验方案如下:取少量黑色粉末于试管,加足量盐酸,充分振荡使黑色粉末完全溶解,滴入KSCN溶液,观察现象。请分析此方案是否可行,并解释原因。
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐3】碘化钠用作甲状腺肿瘤防治剂、祛痰剂和利尿剂,食品添加剂、感光剂等。实验室用NaOH、单质碘和水合肼(N2H4·H2O)为原料可制备碘化钠。回答下列问题:
(1)水合肼的制备。
有关反应原理为:NaClO+2NH3=N2H4·H2O+NaCl。
①用下图装置制取水合肼,其连接顺序为_________ (按气流方向,用小写字母表示)。
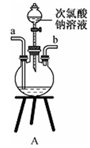

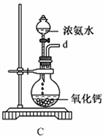
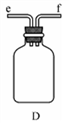
②装置C中发生反应的化学方程式为_____________________ ,装置D的作用是__________________ 。
(2)碘化钠的制备。
步骤一:向三口烧瓶中加入8.2gNaOH及30mL水,搅拌冷却,加入25.4g单质碘,开动磁力搅拌器,保持60~70℃至反应充分;
步骤二:继续加入稍过量的N2H4·H2O(水合肼),还原NaIO和NaIO3,得NaI溶液粗品,同时释放一种空气中的某气体;
步耀三:向上述反应液中加入1.0g活性炭,煮沸半小时,然后将溶液与活性炭分离;
步骤四:将步骤三分离出的溶液蒸发浓缩、冷却结晶、过滤、洗涤、干燥,得产品24.3g。
①步骤一反应温度不宜超过70℃的原因是________________________ ;该步骤反应完全的现象是________ 。
②步骤二中IO-参与反应的离子方程式为_______________________________ 。
③步骤三“将溶液与活性炭分离”的方法是_____________________________ 。
④本次实验产率为_________ 。
(1)水合肼的制备。
有关反应原理为:NaClO+2NH3=N2H4·H2O+NaCl。
①用下图装置制取水合肼,其连接顺序为




②装置C中发生反应的化学方程式为
(2)碘化钠的制备。
步骤一:向三口烧瓶中加入8.2gNaOH及30mL水,搅拌冷却,加入25.4g单质碘,开动磁力搅拌器,保持60~70℃至反应充分;
步骤二:继续加入稍过量的N2H4·H2O(水合肼),还原NaIO和NaIO3,得NaI溶液粗品,同时释放一种空气中的某气体;
步耀三:向上述反应液中加入1.0g活性炭,煮沸半小时,然后将溶液与活性炭分离;
步骤四:将步骤三分离出的溶液蒸发浓缩、冷却结晶、过滤、洗涤、干燥,得产品24.3g。
①步骤一反应温度不宜超过70℃的原因是
②步骤二中IO-参与反应的离子方程式为
③步骤三“将溶液与活性炭分离”的方法是
④本次实验产率为
您最近一年使用:0次



