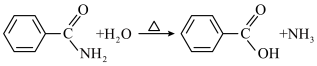
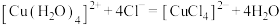下列与金属腐蚀有关的说法正确的是
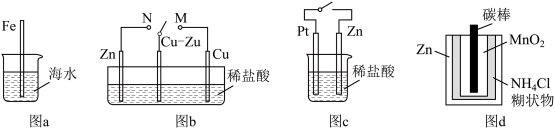

| A.图a中,插入海水中的铁棒,越靠近底端腐蚀越严重 |
| B.图d中,Zn - MnO2干电池自放电腐蚀主要是由MnO2的氧化作用引起的 |
| C.图c中,接通开关时Zn腐蚀速率增大,Zn上放出气体的速率也增大 |
| D.图b中,开关由M改置于N时,cu-zn合金的腐蚀速率减小 |
更新时间:2017-02-17 14:57:34
|
相似题推荐
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】如图所示,将铁棒和石墨棒插入l L l mol·L-1食盐水中。下列说法正确的是
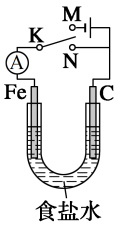

| A.若电键K与N连接,铁会发生还原反应而被腐蚀 |
| B.若电键K与N连接,负极反应式是:4OH-_4e-=2H2O+O2↑ |
| C.若电键K与M连接,将石墨棒换成铜棒,可实现铜棒上镀铁 |
| D.若电键K与M连接,当两极共产生5.6 L(标准状况)气体时,生成了0.25 mol NaOH |
您最近半年使用:0次
单选题
|
较难
(0.4)
【推荐2】验证牺牲阳极的阴极保护法,实验如下(烧杯内均为经过酸化的3%NaCl溶液)。
下列说法不正确 的是
| ① | ② | ③ |
|
|
|
| 在Fe表面生成蓝色沉淀 | 试管内无明显变化 | 试管内生成蓝色沉淀 |
| A.对比②③,可以判定Zn保护了Fe |
| B.对比①②,K3[Fe(CN)6]可能将Fe氧化 |
| C.验证Zn保护Fe时不能用①的方法 |
| D.将Zn换成Cu,用①的方法可判断Fe比Cu活泼 |
您最近半年使用:0次
单选题
|
较难
(0.4)
【推荐1】我国某科研机构设计下图装置,利用K2Cr2O7实现含苯酚废水的有效处理(达到可排放标准 ) ,一段时间后,中间室中NaCl溶液的浓度减小。下列说法不正确 的是
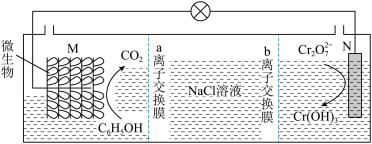

| A.该装置不适合在高温下处理含苯酚废水 |
| B.M电极的的电极反应式为:C6H5OH-28e-+11H2O=6CO2↑+28H+ |
| C.a为阳离子交换膜,b为阴离子交换膜 |
D.N电极反应式为:Cr2O +6e-+8H+=2Cr(OH)3↓+H2O +6e-+8H+=2Cr(OH)3↓+H2O |
您最近半年使用:0次
单选题
|
较难
(0.4)
【推荐2】微生物脱盐池是在微生物燃料电池的基础上发展而来的新兴生物电化学系统,原理如图所示,下列说法错误的是


A. 为正极 为正极 |
B. 为阴离子交换膜 为阴离子交换膜 |
| C.该装置能实现从海水中得到淡水,同时去除有机物并提供电能 |
D.负极反应为 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】“太阳水”电池装置如图所示,该电池由三个电极组成,其中 a 为TiO2电极,b 为Pt 电极,c 为 WO3电极,电解质溶液为 pH=3 的 Li2SO4-H2SO4溶液。锂离子交换膜将电池分为 A、B 两个区,A 区与大气相通,B 区为封闭体系并有 N2保护。下列关于该电池的说法错误的是
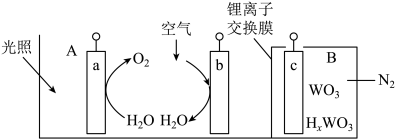

| A.若用导线连接a、c,则 a 为负极,该电极附近 pH 减小 |
| B.若用导线连接 a、c,则 c 电极的电极反应式为HxWO3-xe-=WO3+ xH+ |
| C.若用导线连接 b、c,b 电极的电极反应式为 O2+4H++4e-=2H2O |
| D.利用该装置,可实现太阳能向电能转化 |
您最近半年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】NA为阿伏加德罗常数的值。下列说法正确的是
A.锌-锰干电池电池反应: ,当有1 ,当有1  完全反应转移的电子数为4NA 完全反应转移的电子数为4NA |
B.电解硫酸铜t秒后在阴极析出铜片mg,通过溶液的电流为I安培,则NA可表示为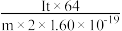 (每个电子的电量为 (每个电子的电量为 库仑) 库仑) |
C.常温下, 的 的 、 、 的混合溶液中, 的混合溶液中,  |
D.1L0.100的 溶液中,阴离子数为0.100NA 溶液中,阴离子数为0.100NA |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】纸电池为轻型、高效的新型能源存储带来希望之光。一种碱性纸电池如图所示,薄层纸片的两面分别附着锌和二氧化锰,电池总反应: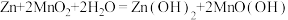 ,[已知
,[已知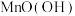 中
中 的化合价为+3]。下列有关说法错误的是
的化合价为+3]。下列有关说法错误的是
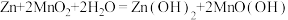 ,[已知
,[已知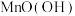 中
中 的化合价为+3]。下列有关说法错误的是
的化合价为+3]。下列有关说法错误的是
| A.薄层纸片的作用为载体和传导体 |
B.该新型电池工作时,电子由 沿内电路流回 沿内电路流回 |
C. 为正极材料,电极反应式为 为正极材料,电极反应式为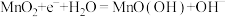 |
D.每转移 电子,负极材料质量增加17g 电子,负极材料质量增加17g |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】下列关于金属防护的说法中正确的是
| A.当镀锌铁制品的镀层破损时,镀层仍能对铁制品起保护作用 |
| B.地下输油钢管与外加直流电源的正极相连可保护其不受腐蚀 |
| C.在轮船船体四周镶嵌锌块保护船体不受腐蚀的方法叫阳极电化学保护法 |
| D.不锈钢有较强的抗腐蚀能力是因为在钢铁表面镀上了铬 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】利用数字化实验进行铁的电化学腐蚀实验探究,实验结果如图所示,以下说法正确的是
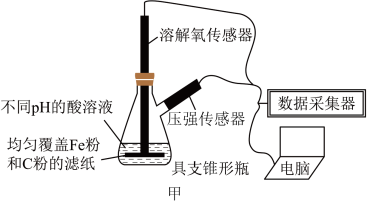
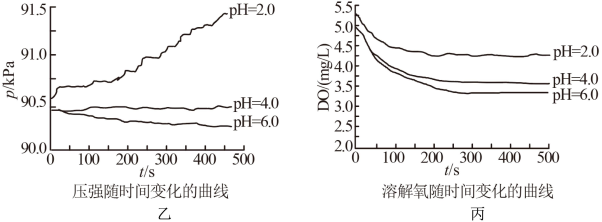
A. 时,正极只发生析氢腐蚀,故体系压强增大 时,正极只发生析氢腐蚀,故体系压强增大 |
B. 时,体系压强增大的原因之一是反应放热 时,体系压强增大的原因之一是反应放热 |
C. 和 和 时,正极电极的电极反应均只有: 时,正极电极的电极反应均只有: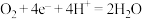 |
D.实验结束后,向锥形瓶中加入 溶液,溶液变红,说明整个过程中负极电极反应式均为 溶液,溶液变红,说明整个过程中负极电极反应式均为 |
您最近半年使用:0次
【推荐3】实验小组研究金属电化学腐蚀,实验如下:
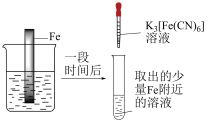
实验Ⅰ

5min时的现象:铁钉表面及周边未见明显变化。
25min时的现象:铁钉周边零星、随机出现极少量红色和蓝色区域,有少量红棕色铁锈生成。
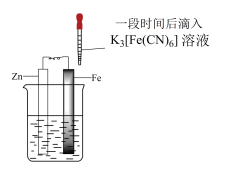
实验Ⅱ
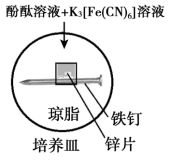
5min时的现象:铁钉周边出现红色区域,未见蓝色出现,锌片周边未见明显变化。
25min时的现象:铁钉周边红色加深,区域变大,未见蓝色出现,锌片周边未见明显变化。
下列说法不正确的是
实验Ⅰ

5min时的现象:铁钉表面及周边未见明显变化。
25min时的现象:铁钉周边零星、随机出现极少量红色和蓝色区域,有少量红棕色铁锈生成。
实验Ⅱ

5min时的现象:铁钉周边出现红色区域,未见蓝色出现,锌片周边未见明显变化。
25min时的现象:铁钉周边红色加深,区域变大,未见蓝色出现,锌片周边未见明显变化。
下列说法不正确的是
| A.实验Ⅱ中Zn保护了Fe,使铁的腐蚀速率比实验Ⅰ慢 |
B.实验Ⅱ中正极的电极反应式: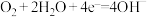 |
C.实验Ⅰ的现象说明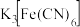 溶液与Fe反应生成了 溶液与Fe反应生成了 |
| D.若将Zn片换成Cu片,推测Cu片周边会出现红色,铁钉周边会出现蓝色 |
您最近半年使用:0次


 与
与 溶液反应:
溶液反应: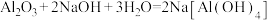

 溶液中加入浓
溶液中加入浓 溶液,发生反应:
溶液,发生反应: