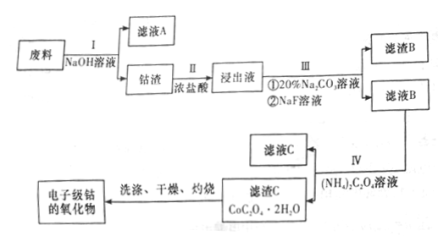
电子级钴的氧化物用于半导体工业和电子陶瓷等领域,是一种纯度很高的氧化物。现从废料(含Co3O4、Al、Si、Li2O、Fe2O3等物质)中提纯电子级钴的氧化物,其工业制取流程如下:
已知:
①物质的溶解性:LiF难溶于水,Li2CO3微溶于水;②钴元素常见的化合价为+ 2和+ 3;
③部分金属离子形成氢氧化物沉淀的pH见下表。
(1)废料在处理前要粉碎,其主要目的是(回答两个方面)___________ ;
步骤I得到的滤液A中的溶质为___________ (填化学式)。
(2)步骤II中有黄绿色气体生成,有关含钴化合物发生反应的离子方程式为_________ 。
(3)步骤III中Na2CO3溶液的作用是调节溶液的pH,应使溶液的pH的取值范围为___________ ;滤渣B的主要成分为____________ 。
(4)步骤I、III、IV中均用到的分离提纯方法为_______ ,在实验室中完成该操作用到的玻璃仪器是__ 。
(5)5.49gCoC2O4·2H2O(其相对分子质量为183)经过反复洗涤、干燥后,进行灼烧,其热重分析如下表。
290℃~320℃时若生成两种气体,则发生反应的化学方程式为___________ ,400℃~500℃所得固体的化学式为__________ 。
已知:
①物质的溶解性:LiF难溶于水,Li2CO3微溶于水;②钴元素常见的化合价为+ 2和+ 3;
③部分金属离子形成氢氧化物沉淀的pH见下表。
| Fe3+ | Co2+ | Co3+ | Al3+ | |
| pH(开始沉淀) | 1.9 | 7.15 | -0.23 | 3.4 |
| pH(完全沉淀) | 3.2 | 9.15 | 1.09 | 4.7 |
步骤I得到的滤液A中的溶质为
(2)步骤II中有黄绿色气体生成,有关含钴化合物发生反应的离子方程式为
(3)步骤III中Na2CO3溶液的作用是调节溶液的pH,应使溶液的pH的取值范围为
(4)步骤I、III、IV中均用到的分离提纯方法为
(5)5.49gCoC2O4·2H2O(其相对分子质量为183)经过反复洗涤、干燥后,进行灼烧,其热重分析如下表。
| 温度范围/℃ | 固体质量/g |
| 150~210 | 4.41 |
| 290~320 | 2.25 |
| 400~500 | 2.41 |
更新时间:2017-03-07 21:00:45
|
相似题推荐
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐1】二氯二氢硅(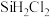 )常用于外延法工艺中重要的硅源。易燃、有毒,与水接触易水解,沸点为8.2℃。在铜催化作用下,HCl与Si在250~260℃条件下反应可以制得
)常用于外延法工艺中重要的硅源。易燃、有毒,与水接触易水解,沸点为8.2℃。在铜催化作用下,HCl与Si在250~260℃条件下反应可以制得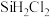 。
。

(1)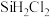 的电子式为
的电子式为___________ 。
(2)利用浓硫酸、氯化钠为原料,选用A装置制取HCl,该反应能发生的原理是___________ 。
(3)D装置中生成二氯二氢硅的化学方程式为___________ 。
(4)按照气体从左到右方向,制取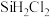 的装置(h处用止水夹夹好)连接次序为a→→→→→→→
的装置(h处用止水夹夹好)连接次序为a→→→→→→→___________ (填仪器接口的字母,其中装置C用到2次)。
(5)按从左到右的顺序,前面装置C中装的药品为___________ ,其作用为___________ 。
(6)氧化铜对该反应没有催化作用,仪器连接、气密性检验后应先___________ ,再对D处进行加热。
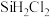 )常用于外延法工艺中重要的硅源。易燃、有毒,与水接触易水解,沸点为8.2℃。在铜催化作用下,HCl与Si在250~260℃条件下反应可以制得
)常用于外延法工艺中重要的硅源。易燃、有毒,与水接触易水解,沸点为8.2℃。在铜催化作用下,HCl与Si在250~260℃条件下反应可以制得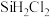 。
。
(1)
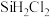 的电子式为
的电子式为(2)利用浓硫酸、氯化钠为原料,选用A装置制取HCl,该反应能发生的原理是
(3)D装置中生成二氯二氢硅的化学方程式为
(4)按照气体从左到右方向,制取
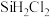 的装置(h处用止水夹夹好)连接次序为a→→→→→→→
的装置(h处用止水夹夹好)连接次序为a→→→→→→→(5)按从左到右的顺序,前面装置C中装的药品为
(6)氧化铜对该反应没有催化作用,仪器连接、气密性检验后应先
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐2】下图中的A~H是中学化学中常见的八种物质,所有物质均由短周期元素组成,其中B、F、H都含有同一种元素;B、D、E为单质,其他为化合物,常温常压下C为无色液体,D、E为气体;H的晶体熔点高、硬度大、闪烁着晶莹的光泽。A~H之间的转化关系如图所示。

(1)C的化学式为__________________ 、A的电子式为_____________ ;
(2)A、B的混合物加C后,可能发生的反应的化学方程式为_____________ 、_________________________ ;
(3)向F溶液中逐渐滴入盐酸直至过量,若看到的现象是先出现白色沉淀后沉淀消失,写出符合现象的离子方程式______________________________________ ,与之对应的D、E恰好完全反应生成C时A与B的物质的量之比为:________ 。

(1)C的化学式为
(2)A、B的混合物加C后,可能发生的反应的化学方程式为
(3)向F溶液中逐渐滴入盐酸直至过量,若看到的现象是先出现白色沉淀后沉淀消失,写出符合现象的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐3】材料科学是近年来与化学有关的科学研究热点。某新型无机非金属材料K由两种非金属元素组成。它是一种超硬物质,具有耐磨、耐腐蚀、抗冷热冲击、抗氧化的特征。它是以中学化学中常见物质为原料来生产的。下图虚线框内的其它转化是为探究C的组成而设。G、F、H均为难溶于水的白色固体;图中C、H、K均为含A元素。其余物质均为中学化学中常见物质。

请回答下列问题:
(1)指出K可能所属的晶体类型__________ ,K中含有的化学键类型为___________ 。
(2)写出化学式:化合物C____________________ ;化合物F______________ 。
(3)写出反应③的化学方程式:_______________________________________ 。
(4)写出反应⑤的离子方程式:_______________________________________ 。
(5)化合物K与化合物C类似,也能在一定条件下与水反应生成两种化合物,请写出K与水反应的化学方程式:_______________________________________ 。

请回答下列问题:
(1)指出K可能所属的晶体类型
(2)写出化学式:化合物C
(3)写出反应③的化学方程式:
(4)写出反应⑤的离子方程式:
(5)化合物K与化合物C类似,也能在一定条件下与水反应生成两种化合物,请写出K与水反应的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐1】M、N是两种金属单质,W是一种强碱,焰色试验呈黄色,Y在食品行业中可用于焙制糕点;a、b、c是常见的单质或氧化物,它们之间存在如下转化关系,按要求回答问题。

(1)c是常见的温室气体之一,则c的化学式为_______ 。
(2)在溶液中实现过程①和②的措施分别是①_______ 、②_______ (各限填一种)
(3)金属M长期置于空气中,最终后形成的物质是_______ (写化学式)。
(4)N→Z的离子方程式为_______ 。
(5)将1 mol F和2 mol Y置于密闭容器中,加热,充分反应后排出气体,排出气体的成分是_______ 。
(6)将2 mol F投入到含有1 mol G的溶液中充分反应,发生反应的总的离子方程式为_______ 。
(7)向0.1 mol/L 的G溶液中逐滴滴加0.1mol/L的W溶液至过量,整个过程中的实验现象为_______ 。

(1)c是常见的温室气体之一,则c的化学式为
(2)在溶液中实现过程①和②的措施分别是①
(3)金属M长期置于空气中,最终后形成的物质是
(4)N→Z的离子方程式为
(5)将1 mol F和2 mol Y置于密闭容器中,加热,充分反应后排出气体,排出气体的成分是
(6)将2 mol F投入到含有1 mol G的溶液中充分反应,发生反应的总的离子方程式为
(7)向0.1 mol/L 的G溶液中逐滴滴加0.1mol/L的W溶液至过量,整个过程中的实验现象为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐2】A、B、C、D、E 五种物质存在以下转化关系,已知A 为金属单质,在以下各步反应中E 是白色沉淀。

(1)试确定各物质的化学式:
A________________ B __________ C__________ D________________ E____________
(2)写出以下反应的离子方程式:
A →C_________________________________
B →E_________________________________

(1)试确定各物质的化学式:
A
(2)写出以下反应的离子方程式:
A →C
B →E
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐3】下图表示有关物质之间的转化关系,其中A为常见的金属单质,B为非金属单质(一般是黑色粉末),C是常见的无色无味液体,D是淡黄色的固体化合物(反应条件图中已省略)

(1)A,D代表的物质分别为:________ ,________ (填化学式);
(2)反应①中的C,D均过量,该反应的化学方程式是____________________________________ ;
(3)反应②中,若B与F物质的量之比为4∶3,G,H分别是_______ ,_______ (填化学式);其物质的量之比为__________ .
(4)反应③产物中K的化学式为____________ ;④的离子方程式为_____________________________ .

(1)A,D代表的物质分别为:
(2)反应①中的C,D均过量,该反应的化学方程式是
(3)反应②中,若B与F物质的量之比为4∶3,G,H分别是
(4)反应③产物中K的化学式为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐1】为了探究固体化合物X(仅含两种元素)的组成和性质,设计并完成如下实验(已知化合物A的摩尔质量:200g/mol<M<300g/mol):

请回答:
(1)白色沉淀E的化学式是_____ 。
(2)固体X中的元素是_____ 。(填元素符号)
(3)固体X在空气中煅烧生成化合物A和气体D的化学方程式_____ 。
(4)往溶液B通入适量氯气的离子方程式是_____ 。

请回答:
(1)白色沉淀E的化学式是
(2)固体X中的元素是
(3)固体X在空气中煅烧生成化合物A和气体D的化学方程式
(4)往溶液B通入适量氯气的离子方程式是
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐2】为探究某难溶性盐X(仅含三种常见元素)的组成,设计并完成以下实验(流程中部分物质已略去):

已知:气体A和气体B所含元素相同,都是无色无味气体,固体C为纯净物且具有磁性,单质D是目前建筑行业应用最广泛的金属。根据上述信息,回答下列问题:
(1)盐X的化学式为________________ 。
(2)无水条件下,少量NaH就能与固体C反应并放出大量的热,写出该反应的化学方程式___________________ 。
(3)将产生的气体A全部被100 mL 0.35 mol·L-1氢氧化钠溶液充分吸收,反应的总离子方程式为____________________ 。

已知:气体A和气体B所含元素相同,都是无色无味气体,固体C为纯净物且具有磁性,单质D是目前建筑行业应用最广泛的金属。根据上述信息,回答下列问题:
(1)盐X的化学式为
(2)无水条件下,少量NaH就能与固体C反应并放出大量的热,写出该反应的化学方程式
(3)将产生的气体A全部被100 mL 0.35 mol·L-1氢氧化钠溶液充分吸收,反应的总离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
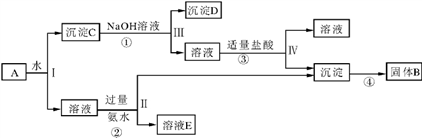
【推荐3】某混合物 A,含有 KAl(SO4)2、Al2O3 和 Fe2O3,在一定条件下可实现下图所示的物质之间的变化:
据此回答下列问题:
(1)Ⅰ、Ⅱ、Ⅲ、Ⅳ四步中对于溶液和沉淀的分离采取的方法是__________ 。
(2)根据上述框图反应关系,写出下列B、C、D 所含物质的化学式(提示:可为混合物)。
固体 B_________ ;沉淀 C__________ ;沉淀 D _________ ;
(3)写出①、②反应离子方程式。
①___________________________________________ ;
②___________________________________________ ;
(4)步骤③较难操作,如何将实验方案进行改进?_______________________________ 。

据此回答下列问题:
(1)Ⅰ、Ⅱ、Ⅲ、Ⅳ四步中对于溶液和沉淀的分离采取的方法是
(2)根据上述框图反应关系,写出下列B、C、D 所含物质的化学式(提示:可为混合物)。
固体 B
(3)写出①、②反应离子方程式。
①
②
(4)步骤③较难操作,如何将实验方案进行改进?
您最近一年使用:0次



