(1)将锌片和银片浸入稀硫酸中组成原电池,两电极间连接一个电流表。
锌片上发生的电极反应:__________________ ;银片上发生的电极反应:_________________ 。
(2)若该电池中两电极的总质量为60 g,工作一段时间后,取出锌片和银片洗净干燥后称重,总质量为47 g,试计算:
①产生氢气的体积(标准状况)___________ L;
②通过导线的电量________ C。(已知NA=6.02×1023mol-1,电子电荷为1.60×10-19C)
锌片上发生的电极反应:
(2)若该电池中两电极的总质量为60 g,工作一段时间后,取出锌片和银片洗净干燥后称重,总质量为47 g,试计算:
①产生氢气的体积(标准状况)
②通过导线的电量
10-11高二下·浙江杭州·阶段练习 查看更多[6]
(已下线)2010—2011学年浙江省杭州市萧山九中高二下学期第一次质量检测化学试卷(已下线)2011-2012学年河北省唐山一中高一下学期3月月考化学试卷2016-2017学年湖北省沙市中学高一下学期第三次双周考(A卷)化学试卷四川省资阳中学2016-2017学年高一下学期期中化学试题鲁科版(2019)高一必修第二册 第2章 化学键 反应规律 第二节 化学反应与能量转化 方法帮(人教版2019)必修第二册 第六章 化学反应与能量 第一节 化学反应与能量变化
更新时间:2017-03-28 23:28:34
|
相似题推荐
填空题
|
较难
(0.4)
名校
【推荐1】(1)高铁酸钾(K2FeO4)不仅是一种理想的水处理剂,而且高铁电池的研制也在进行中。如图是高铁电池的模拟实验装置:
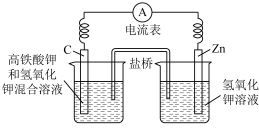
①该电池放电时正极的电极反应式为____________________ ;若维持电流强度为1 A,电池工作十分钟,理论上消耗Zn______ g(计算结果保留一位小数,已知F=96500 C·mol-1)。
②盐桥中盛有饱和KCl溶液,此盐桥中氯离子向______ (填“左”或“右”)移动;若用阳离子交换膜代替盐桥,则钾离子向________ (填“左”或“右”)移动。
③下图为高铁电池和常用的高能碱性电池的放电曲线,由此可得出高铁电池的优点有__________ 。
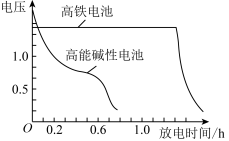
(2)有人设想以N2和H2为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氮的新型燃料电池,装置如图所示,电池正极的电极反应式是__________________________ ,A是________ 。
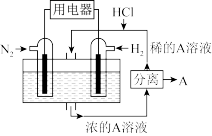
(3)利用原电池工作原理测定汽车尾气中CO的浓度,其装置如图所示。该电池中O2-可以在固体介质NASICON (固溶体)内自由移动,工作时O2-的移动方向________ (填“从a到b”或“从b到a”),负极发生的电极反应式为__________________________ 。
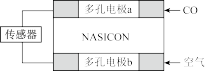

①该电池放电时正极的电极反应式为
②盐桥中盛有饱和KCl溶液,此盐桥中氯离子向
③下图为高铁电池和常用的高能碱性电池的放电曲线,由此可得出高铁电池的优点有

(2)有人设想以N2和H2为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氮的新型燃料电池,装置如图所示,电池正极的电极反应式是

(3)利用原电池工作原理测定汽车尾气中CO的浓度,其装置如图所示。该电池中O2-可以在固体介质NASICON (固溶体)内自由移动,工作时O2-的移动方向
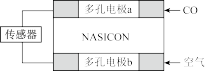
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】如图所示装置可构成原电池。试回答下列问题:
(1)电解质溶液为浓硝酸时,灯泡______ (填“亮”或“不亮”, 填“亮”做a题,填“不亮”做b题)。
a.若灯泡亮,则Mg电极上发生的反应为:_______________ ;
b.若灯泡不亮,其理由为:________________________
(2)电解质溶液为NaOH溶液时,灯泡______ (填“亮”或“不亮”, 填“亮”做a题,填“不亮”做b题)。
a.若灯泡亮,则Mg电极反应式为:_______________ ;Al电极反应式为: _______________ 。
b.若灯泡不亮,其理由为:________________________ 。
(Ⅰ)有一种节能的氯碱工业新工艺,将电解池与燃料电池相组合,相关流程如图所示(电极未标出):
回答下列有关问题:
(3)原电池的负极反应式为____________________ 。
(4)a、b、c的大小关系为:_________________ 。

(1)电解质溶液为浓硝酸时,灯泡
a.若灯泡亮,则Mg电极上发生的反应为:
b.若灯泡不亮,其理由为:
(2)电解质溶液为NaOH溶液时,灯泡
a.若灯泡亮,则Mg电极反应式为:
b.若灯泡不亮,其理由为:
(Ⅰ)有一种节能的氯碱工业新工艺,将电解池与燃料电池相组合,相关流程如图所示(电极未标出):

回答下列有关问题:
(3)原电池的负极反应式为
(4)a、b、c的大小关系为:
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐3】已知废旧酸性干电池可通过酸浸、过滤等操作形成 、
、 的混合溶液,为了实现废旧普通氯化铵干电池中锌与
的混合溶液,为了实现废旧普通氯化铵干电池中锌与 的同时回收,某研究小组设计了如图实验探究装置:
的同时回收,某研究小组设计了如图实验探究装置:

回答下列问题:
(1)甲池是将_______ 能转化_______ 能的装置。
(2)乙池中石墨电极_______ 电子(填“得”或“失”),发生_______ 反应(填“氧化”或“还原”)。
(3)写出电池负极的电极反应式_______ 。
(4)写出乙池回收锌与 的总反应的离子方程式为
的总反应的离子方程式为_______ 。
(5)若消耗2.24L(标准状况) ,且无能量损失,电解池中回收制得19.5g单质Zn,计算乙池中电流效率
,且无能量损失,电解池中回收制得19.5g单质Zn,计算乙池中电流效率
_______ 。( 生成目标产物消耗的电子数/转移的电子总数×100%)。
生成目标产物消耗的电子数/转移的电子总数×100%)。
 、
、 的混合溶液,为了实现废旧普通氯化铵干电池中锌与
的混合溶液,为了实现废旧普通氯化铵干电池中锌与 的同时回收,某研究小组设计了如图实验探究装置:
的同时回收,某研究小组设计了如图实验探究装置:
回答下列问题:
(1)甲池是将
(2)乙池中石墨电极
(3)写出电池负极的电极反应式
(4)写出乙池回收锌与
 的总反应的离子方程式为
的总反应的离子方程式为(5)若消耗2.24L(标准状况)
 ,且无能量损失,电解池中回收制得19.5g单质Zn,计算乙池中电流效率
,且无能量损失,电解池中回收制得19.5g单质Zn,计算乙池中电流效率
 生成目标产物消耗的电子数/转移的电子总数×100%)。
生成目标产物消耗的电子数/转移的电子总数×100%)。
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐1】(1)Mg、Si与NaOH溶液构成的原电池,负极反应式为_________ ,正极反应式为_________ 。
(2)熔盐电池具有高的发电效率,因而受到重视,可用Li2CO3和Na2CO3的熔融盐混合物作电解质,CO为负极燃气,空气与CO2的混合气为正极助燃气,制得在650℃下工作的燃料电池,电池总反应式为2CO+O2=2CO2。则负极反应式:_________ ,正极反应式:___________ 。
(3)最近,又有科学家制造出一种固体电解质的燃料电池。一个电极通入空气,另一个电极通入汽油蒸汽。其中固体电解质是掺杂了Y2O3的ZrO2固体,它在高温下能传导O2−离子(其中氧化反应发生完全)。以丁烷代表汽油。该电池的负极反应式为_____________ 。
(2)熔盐电池具有高的发电效率,因而受到重视,可用Li2CO3和Na2CO3的熔融盐混合物作电解质,CO为负极燃气,空气与CO2的混合气为正极助燃气,制得在650℃下工作的燃料电池,电池总反应式为2CO+O2=2CO2。则负极反应式:
(3)最近,又有科学家制造出一种固体电解质的燃料电池。一个电极通入空气,另一个电极通入汽油蒸汽。其中固体电解质是掺杂了Y2O3的ZrO2固体,它在高温下能传导O2−离子(其中氧化反应发生完全)。以丁烷代表汽油。该电池的负极反应式为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】如图所示装置可构成原电池。试回答下列问题:
(1)电解质溶液为浓硝酸时,灯泡______ (填“亮”或“不亮”, 填“亮”做a题,填“不亮”做b题)。
a.若灯泡亮,则Mg电极上发生的反应为:_______________ ;
b.若灯泡不亮,其理由为:________________________
(2)电解质溶液为NaOH溶液时,灯泡______ (填“亮”或“不亮”, 填“亮”做a题,填“不亮”做b题)。
a.若灯泡亮,则Mg电极反应式为:_______________ ;Al电极反应式为: _______________ 。
b.若灯泡不亮,其理由为:________________________ 。
(Ⅰ)有一种节能的氯碱工业新工艺,将电解池与燃料电池相组合,相关流程如图所示(电极未标出):
回答下列有关问题:
(3)原电池的负极反应式为____________________ 。
(4)a、b、c的大小关系为:_________________ 。

(1)电解质溶液为浓硝酸时,灯泡
a.若灯泡亮,则Mg电极上发生的反应为:
b.若灯泡不亮,其理由为:
(2)电解质溶液为NaOH溶液时,灯泡
a.若灯泡亮,则Mg电极反应式为:
b.若灯泡不亮,其理由为:
(Ⅰ)有一种节能的氯碱工业新工艺,将电解池与燃料电池相组合,相关流程如图所示(电极未标出):

回答下列有关问题:
(3)原电池的负极反应式为
(4)a、b、c的大小关系为:
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐3】人们应用原电池原理制作了多种电池,以满足不同的需要.以下每小题中的电池广泛使用于日常生活、生产和科学技术等方面,请根据题中提供的信息,填写空格.
(1)FeCl3溶液常用于腐蚀印刷电路铜板,发生2FeCl3+Cu═2FeCl2+CuCl2,若将此反应设计成原电池,则负极所用电极材料为____________ ,当线路中转移0.2mol电子时,则被腐蚀铜的质量为______________ g.
(2)将铝片和铜片用导线相连,一组插入浓硝酸中,一组插入烧碱溶液中,分别形成了原电池,在这两个原电池中,负极分别为____________________ .
A.铝片、铜片 B.铜片、铝片 C.铝片、铝片
(3)燃料电池是一种高效、环境友好的供电装置,如图是电解质为稀硫酸溶液的氢氧燃料电池原理示意图,回答下列问题:

①氢氧燃料电池的总反应化学方程式是:__________________ .
②电池工作一段时间后硫酸溶液的浓度___________ (填“增大”、“减小”或“不变”).
(1)FeCl3溶液常用于腐蚀印刷电路铜板,发生2FeCl3+Cu═2FeCl2+CuCl2,若将此反应设计成原电池,则负极所用电极材料为
(2)将铝片和铜片用导线相连,一组插入浓硝酸中,一组插入烧碱溶液中,分别形成了原电池,在这两个原电池中,负极分别为
A.铝片、铜片 B.铜片、铝片 C.铝片、铝片
(3)燃料电池是一种高效、环境友好的供电装置,如图是电解质为稀硫酸溶液的氢氧燃料电池原理示意图,回答下列问题:

①氢氧燃料电池的总反应化学方程式是:
②电池工作一段时间后硫酸溶液的浓度
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐1】图所示,是原电池的装置图。请回答:

(1)若C为稀H2SO4溶液,电流表指针发生偏转,B电极材料为Fe且做负极,则A电极上发生的电极反应式为________________________ ;反应进行一段时间后溶液C的pH将________ (填“升高”“降低”或“基本不变”)
(2)若需将反应:Cu+2Fe3+==Cu2++2Fe2+设计成如上图所示的原电池装置,则A(负极)极材料为________ ,B(正极)极材料为________ ,溶液C为________ 。
(3)若C为CuCl2溶液,Zn是________ 极,Cu极发生________ 反应,电极反应为________________________ 。反应过程溶液中c(Cu2+)________ (填“变大”“变小”或“不变”)。
(4)CO与H2反应还可制备CH3OH,CH3OH可作为燃料使用,用CH3OH和O2组合形成的质子交换膜燃料电池的结构示意图如下:

电池总反应为2CH3OH+3O2==2CO2+4H2O,则c电极是________ (填“正极”或“负极”),c电极的反应方程式为____________________________ 。若线路中转移2mol电子,则上述CH3OH燃料电池,消耗的O2在标准状况下的体积为________ L。

(1)若C为稀H2SO4溶液,电流表指针发生偏转,B电极材料为Fe且做负极,则A电极上发生的电极反应式为
(2)若需将反应:Cu+2Fe3+==Cu2++2Fe2+设计成如上图所示的原电池装置,则A(负极)极材料为
(3)若C为CuCl2溶液,Zn是
(4)CO与H2反应还可制备CH3OH,CH3OH可作为燃料使用,用CH3OH和O2组合形成的质子交换膜燃料电池的结构示意图如下:

电池总反应为2CH3OH+3O2==2CO2+4H2O,则c电极是
您最近一年使用:0次
【推荐2】根据下列要求回答下列问题。
(1)次磷酸钴[Co(H2PO2)2]广泛用于化学镀钴,以金属钴和次磷酸钠为原料,采用四室电渗析槽电解法制备,原理如图:

则Co的电极反应式为___________ ,A、B、C为离子交换膜,其中B为___________ 离子交换膜(填“阳”或“阴”)。
(2)我国科研人员研制出的可充电“NaCO2”电池,以钠箔和多壁碳纳米管(MWCNT)为电极材料,总反应方程式为4Na+3CO2 2Na2CO3+C.放电时该电池“吸入”CO2,其工作原理如图所示:
2Na2CO3+C.放电时该电池“吸入”CO2,其工作原理如图所示:

①放电时,正极的电极反应式为___________ 。
②若生成的Na2CO3和C全部沉积在正极表面,当正极增加的质量为28g时,转移电子的物质的量为___________ 。
③可选用高氯酸钠四甘醇二甲醚作电解液的理由是___________ 。
(1)次磷酸钴[Co(H2PO2)2]广泛用于化学镀钴,以金属钴和次磷酸钠为原料,采用四室电渗析槽电解法制备,原理如图:

则Co的电极反应式为
(2)我国科研人员研制出的可充电“NaCO2”电池,以钠箔和多壁碳纳米管(MWCNT)为电极材料,总反应方程式为4Na+3CO2
 2Na2CO3+C.放电时该电池“吸入”CO2,其工作原理如图所示:
2Na2CO3+C.放电时该电池“吸入”CO2,其工作原理如图所示:
①放电时,正极的电极反应式为
②若生成的Na2CO3和C全部沉积在正极表面,当正极增加的质量为28g时,转移电子的物质的量为
③可选用高氯酸钠四甘醇二甲醚作电解液的理由是
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐3】电化学在化学工业有着广泛的应用,
(1)工业冶炼铝的化学方程式是___________________________ ;
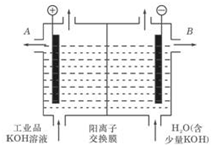
(2)工业级氢氧化钾的溶液中含有某些含氧酸根杂质,可用离子交换法膜法电解提纯。电解槽内装有阳离子交换膜(只允许阳离子通过),其工作原理如图所示。
①该电解槽的阳极反应式是________________________ ;
②除去杂质后的氢氧化钾溶液从液体出口__________ (填写“A”或“B”)导出。
(3)甲醇燃料电池由于其结构简单、能量转化率高、对环境无污染、可作为常规能源的替代品而越来越受到关注。其工作原理如右图,质子交换膜左右两侧的溶液均为1L 1.5 mol/L H2SO4 溶液。
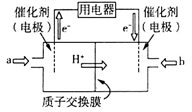
①通入气体a的电极是电池的________ (填“正”或“负”)极,其电极反应式为___________________________________ ;
②当电池中有2 mol e-发生转移时,左右两侧溶液的质量差值为_________ g。
(1)工业冶炼铝的化学方程式是
(2)工业级氢氧化钾的溶液中含有某些含氧酸根杂质,可用离子交换法膜法电解提纯。电解槽内装有阳离子交换膜(只允许阳离子通过),其工作原理如图所示。

①该电解槽的阳极反应式是
②除去杂质后的氢氧化钾溶液从液体出口
(3)甲醇燃料电池由于其结构简单、能量转化率高、对环境无污染、可作为常规能源的替代品而越来越受到关注。其工作原理如右图,质子交换膜左右两侧的溶液均为1L 1.5 mol/L H2SO4 溶液。

①通入气体a的电极是电池的
②当电池中有2 mol e-发生转移时,左右两侧溶液的质量差值为
您最近一年使用:0次



