把A、B、C、D四块金属片浸泡在稀硫酸中,用导线两两连接可以组成各种原电池。A、B连接时,A为负极;C、D连接时,电流由D到C;A、C连接时,C极产生大量气泡;B、D连接时,B极上产生大量气泡。则这4种金属的活动性顺序(由强到弱)为( )
| A.A>B>C>D | B.A>C>D>B |
| C.C>A>B>D | D.B>D>C>A |
更新时间:2017-04-05 20:15:09
|
【知识点】 利用原电池原理比较金属活动性强弱解读
相似题推荐
【推荐1】下列根据实验操作和现象所得出的结论合理的是
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向0.1mol/L的硅酸钠溶液中滴加稀盐酸 | 产生白色胶状沉淀 | 非金属性:Cl>Si |
| B | 等体积pH=3的HA和HB两种酸分别与足量的锌反应,排水法收集气体 | HA放出的氢气多且反应速率快 | 酸性:HA>HB |
| C | 向浓度均为0.1mol·L-1NaCl和NaI的混合溶液中滴加少量AgNO3溶液 | 出现黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
| D | 用导线将镁片和铝片相连后插入NaOH溶液中 | 铝片不断溶解,镁片上有气泡冒出 | 金属活动性:铝>镁 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】现有M、N、P、E 4种元素的单质,能发生以下反应:
①在水溶液中,M+N2+===M2++N ②P+2H2O(冷)===P(OH)2+H2↑ ③N、E相连浸入稀H2SO4中,电极反应为:N-2e-===N2+,2H++2e-===H2↑ 判断它们的还原性由强到弱的顺序是
①在水溶液中,M+N2+===M2++N ②P+2H2O(冷)===P(OH)2+H2↑ ③N、E相连浸入稀H2SO4中,电极反应为:N-2e-===N2+,2H++2e-===H2↑ 判断它们的还原性由强到弱的顺序是
| A.M、N、P、E | B.P、M、N、E |
| C.M、N、E、P | D.E、P、M、N |
您最近一年使用:0次

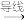 W;X、Z相连时,Z极上产生大量气泡;W、Y相连时,W极发生氧化反应。则这四种金属的活动性顺序是
W;X、Z相连时,Z极上产生大量气泡;W、Y相连时,W极发生氧化反应。则这四种金属的活动性顺序是

