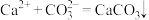下列说法正确的是
| A.粗盐的提纯时,加入沉淀剂过滤的滤液在坩埚中蒸发结晶、出现晶膜停止加热 |
| B.用碱式滴定管可以准确量取20.00 mLKMnO4溶液 |
| C.在未知溶液中滴加BaCl2溶液出现白色沉淀,加稀硝酸,沉淀不溶解,说明该未知溶液中存在SO42- |
| D.配制一定物质的量浓度的溶液时,容量瓶洗涤后未干燥,不影响所配溶液浓度 |
更新时间:2017-04-06 18:42:18
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】某合作学习小组讨论辨析下列说法,其中错误的是
A.金刚石、石墨和 互称为同素异形体 互称为同素异形体 |
| B.物质的摩尔体积主要取决于粒子大小和粒子的间距 |
| C.容量瓶和分液漏斗使用前都需要检查是否漏液 |
| D.焰色试验中有杂质铂丝可用稀硫酸洗净后在外焰上灼烧至与原来火焰颜色相同再实验 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】化学是以实验为基础的学科,下列有关实验操作正确的是
A.配制 溶液,应用托盘天平准确称取 溶液,应用托盘天平准确称取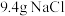 固体 固体 |
| B.中和反应反应热的测定实验中,测量反应前酸溶液的温度后立即测量碱溶液的温度,并记录数据 |
C.用碱式滴定管移取 溶液时,平视读数 溶液时,平视读数 |
| D.用标准氢氧化钠溶液滴定未知浓度的草酸时,滴定管的起始读数可以在0刻度以下 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】根据下列实验操作和实验现象所得结论正确的是
选项 | 实验操作 | 实验现象 | 结论 |
A | 向石蕊溶液中滴加氯水至足量 | 石蕊溶液先变红再褪色 | Cl2有酸性和漂白性 |
B | 向大豆油、煤油中分别加入足量NaOH溶液,充分加热 | 一种液体仍然分层,另一种液体不再分层 | 分层者为煤油,不分层者为大豆油 |
C | 向某溶液中加入足量盐酸 | 生成白色沉淀 | 该溶液中含有Ag+ |
D | 用容量瓶配制一定物质的量浓度的K2SO4溶液,定容后反复摇匀 | 液面低于刻度线 | 所配溶液浓度偏高 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】实验室需要配制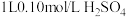 溶液,下列说法正确的是
溶液,下列说法正确的是
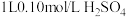 溶液,下列说法正确的是
溶液,下列说法正确的是A.可取 溶液溶解于 溶液溶解于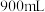 蒸馏水中 蒸馏水中 |
| B.配制过程中,定容时仰视刻度线会使所配制溶液浓度偏高 |
| C.配制过程中,使用未干燥的容量瓶会使所配制溶液浓度偏低 |
D.实验时取出 该溶液后,剩余溶液的浓度为 该溶液后,剩余溶液的浓度为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】《本草纲目》记载:“烧酒,其法用浓酒和糟入甑,蒸令气上,用器承滴露,”“凡酸坏之酒,皆可蒸烧”。这里用到的实验方法可以用于分离
| A.植物油和食盐水 | B.丁醇和乙醚 |
| C.硝酸钾和氯化钠 | D.碳酸钙和硫酸钾 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】中国传统文化博大精深。下列古文献所述没有涉及化学变化的是
| A.“凡石灰,经火焚炼为用” |
| B.“川东盐井,且有火井,以助煎熬,其火无灰” |
C.“丹砂( )烧之成水银,积变又还成丹砂” )烧之成水银,积变又还成丹砂” |
| D.“……欲去杂还纯,再入水煎炼……倾入盆中,经宿结成白雪” |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】离子检验的常用方法有三种
下列离子检验的方法不合理的是( )
| 检验方法 | 沉淀法 | 显色法 | 气体法 |
| 含义 | 反应中有沉淀产生或溶解 | 反应中有颜色变化 | 反应有气体产生 |
| A.CO32-—气体法 | B.Cl-—沉淀法 | C.Fe3+—气体法 | D.OH-—显色法 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列说法不正确 的是
| A.在实验室中,取用金属钠后,剩余的金属钠须放回原试剂瓶 |
| B.为防止硫酸亚铁溶液因氧化而变质,可在溶液中加入适量铁粉 |
| C.某溶液中滴入氯水后再滴入KSCN溶液,溶液变为血红色,则该溶液中一定含有Fe2+ |
D.某溶液加入适量稀硝酸酸化后,滴入硝酸钡溶液,无明显现象,滴入硝酸银溶液,产生白色沉淀,则该溶液中含有Clˉ,不含 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】资料显示:FeCl (亮黄色)只有在Cl-浓度较大的溶液中才能稳定存在,为了验证该事实,某实验小组取三份2mL黄色的工业盐酸分别做了一系列实验,记录如下:
(亮黄色)只有在Cl-浓度较大的溶液中才能稳定存在,为了验证该事实,某实验小组取三份2mL黄色的工业盐酸分别做了一系列实验,记录如下:
下列说法不正确的是
 (亮黄色)只有在Cl-浓度较大的溶液中才能稳定存在,为了验证该事实,某实验小组取三份2mL黄色的工业盐酸分别做了一系列实验,记录如下:
(亮黄色)只有在Cl-浓度较大的溶液中才能稳定存在,为了验证该事实,某实验小组取三份2mL黄色的工业盐酸分别做了一系列实验,记录如下:| 操作 | 现象 |
| 实验I:直接滴加2滴KSCN溶液 | 无明显变化 |
| 实验II:加10mL蒸馏水稀释,后滴入2滴浓KSCN溶液 | 稀释后溶液几乎变为无色,加KSCN溶液显红色 |
| 实验III:滴加2滴AgNO3饱和溶液 | 产生白色沉淀,溶液亮黄色消失 |
A.工业盐酸显黄色是因为其中混有FeCl |
| B.实验I中,未检测到Fe3+ |
| C.实验Ⅲ中,AgNO3溶液稀释了样品是溶液亮黄色消失的主要原因 |
D.通过上述实验,可以证明FeCl 只有在Cl-浓度较大的溶液中才能稳定存在 只有在Cl-浓度较大的溶液中才能稳定存在 |
您最近一年使用:0次



 、
、 、
、 及泥沙等杂质,某同学设计了一种制备精盐的实验方案,流程如图,下列说法正确的是
及泥沙等杂质,某同学设计了一种制备精盐的实验方案,流程如图,下列说法正确的是