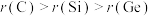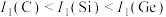短周期主族元素X、Y、Z、W的原子序数依次增大,X的原子半径比Y的小,Y原子最外层电子数是其内层电子总数的3倍,W原子的核电荷数等于X、Z原子的核电荷数之和,X和Z同主族。下列说法正确的是
| A.原子半径:r(W)>r(Z)>r(Y) |
| B.Z的最高价氧化物对应水化物的碱性比W的强 |
| C.化合物X2Y2和Z2Y2所含化学键类型完全相同 |
| D.工业上常用电解熔融W的氧化物制备W的单质 |
2017·江苏·一模 查看更多[10]
(已下线)BBWYhjhx1009.pdf湖南省衡阳市衡阳县第一中学2022届高三下学期第二次模考试化学试题湖南省张家界市第一中学2022届高三下学期期中考试化学试题四川省眉山市仁寿第一中学南校区2021-2022学年高三上学期入学考试化学试题河南省信阳市罗山县高级中学老校区2020届高三第七次模拟考试化学试题海南省海口第四中学2018-2019学年高一下学期期末(选考)化学试题【全国市级联考】广东省肇庆市2018届高三第三次模拟理科综合化学试题江苏省泰州中学2018届高三10月月考化学试题2017届辽宁省部分重点中学协作体高三考前模拟考试理综化学试卷2017届江苏省苏锡常镇四市高三教学情况调研(一)化学试卷
更新时间:2017-03-22 13:54:09
|
相似题推荐
单选题
|
较易
(0.85)
名校
【推荐1】下列四种元素的基态原子的电子排布式如下:①1s22s22p3 ②1s22s22p5 ③1s22s22p63s23p3 ④1s22s22p63s23p4,则下列有关的比较中正确的是
| A.原子半径:④>③>②>① |
| B.电负性:②>③>④>① |
| C.第一电离能:②>①>③>④ |
| D.最高正化合价:②>④>③=① |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列事实能说明非金属性Cl>S的是
| A.Cl2比S易与H2化合 | B.酸性HClO3>H2SO3 |
| C.酸性HCl>H2S | D.Cl、S的最高正价分别为+7、+6 |
您最近半年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】铍镁都是IIA族元素,分别位于第2、3周期,下列有关说法正确的是
| A.原子半径铍比镁的大 |
| B.铍的最高化合价为+3价 |
| C.单质与水的反应镁比铍的剧烈 |
| D.最高价氧化物对应的水化物的碱性铍比镁的强 |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】短周期主族元素离子a dD-都具有相同电子层结构,叙述正确的是
dD-都具有相同电子层结构,叙述正确的是
 dD-都具有相同电子层结构,叙述正确的是
dD-都具有相同电子层结构,叙述正确的是A.离子的还原性: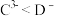 |
| B.原子序数d>c>b>a |
| C.离子半径C3->D->B+>A2+ |
| D.单质的还原性A>B>D>C |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】为了庆祝元素周期表诞生150周年,联合国宣布将2019年定为国际化学元素周期表年,元素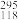 Og中文名为氡,是一种人工合成的稀有气体元素,下列正确的是( )
Og中文名为氡,是一种人工合成的稀有气体元素,下列正确的是( )
 Og中文名为氡,是一种人工合成的稀有气体元素,下列正确的是( )
Og中文名为氡,是一种人工合成的稀有气体元素,下列正确的是( )| A.核外电子数是118 | B.中子数是295 |
| C.质量数是177 | D.第六周期0族元素 |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】氯的原子序数是17,那么氯元素在元素周期表中的位置是
| A.第2周期ⅦA族 | B.第3周期ⅦA族 |
| C.第3周期ⅥA族 | D.第3周期ⅥA族 |
您最近半年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】短周期x、y、z、m、n五种主族元素,原子序数依次增大,x元素的某种原子可以在考古时用来测定文物年代。常温时,测得0.1mol/L y、m、n简单氢化物的水溶液pH分别为11、4、1。且z、m还可以与Na形成如图所以结构的化合物。以下有关说法错误的是
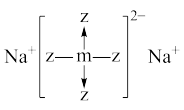
| A.原子半径:z<m<n |
| B.简单氢化物的沸点:x<y<z |
| C.电负性:z>y>x |
| D.x的最高价氧化物中各原子均满足8e-稳定结构 |
您最近半年使用:0次
单选题
|
较易
(0.85)
【推荐2】W、X、Y、Z是原子序数依次增大的短周期元素,W元素的一种同位素是最简单原子,X元素原子的最外层电子数是内层电子数的3倍,Y元素为其所在周期中原子半径最大的元素,Z元素的单质常温下为黄色固体,下列说法正确的是
| A.上述四种元素位于两个主族 |
B.四种元素的原子半径大小顺序: |
| C.含有上述四种元素的常见化合物的水溶液呈碱性 |
| D.W分别与X、Z形成的化合物中存在的化学键完全相同 |
您最近半年使用:0次
单选题
|
较易
(0.85)
【推荐3】短周期元素X、Y、Z、W的原子序数依次增大。X的气态氢化物能使湿润的红色石蕊试纸变蓝,Y是地壳中含量最高的元素,最外层电子数X+Z=Y,Y和W在元素周期表中相邻。下列说法正确的是
| A.Z2Y2的阴阳离子个数比为1∶1 | B.原子半径:Z>W |
| C.X、Y、Z、W中非金属性最强的是W | D.气态氢化物稳定性:W>Y |
您最近半年使用:0次