某小组探究元素周期律,甲根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图装置来一次性完成N、C、Si的非金属性强弱比较的研究;乙根据置换反应的规律,利用下图装置完成O元素的非金属性比S强的研究。回答:
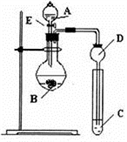
(1)图中A装置名称是______________ 。
(2)从以下所给物质中选出甲同学设计的实验所用到物质:
①稀HNO3溶液 ②稀盐酸 ③碳酸钙 ④Na2SiO3溶液 ⑤SiO2
试剂A与C分别为_________ (填序号);试管中发生反应的离子方程式为_______________ .有同学认为此实验不能说明N、C、S的非金属性强弱,你认为原因是_________________
(3)乙同学设计的实验所用到试剂A为________ ;如果C试剂为硫化氢的水溶液,则试管中可以观察到的现象为_______________

(1)图中A装置名称是
(2)从以下所给物质中选出甲同学设计的实验所用到物质:
①稀HNO3溶液 ②稀盐酸 ③碳酸钙 ④Na2SiO3溶液 ⑤SiO2
试剂A与C分别为
(3)乙同学设计的实验所用到试剂A为
16-17高一下·江西宜春·阶段练习 查看更多[4]
(已下线)练习13 元素周期律-2020-2021学年【补习教材·寒假作业】高一化学(人教版)【全国百强校】湖南省长沙市第一中学2017-2018学年高一下学期第一次检测化学试题(已下线)精做02 元素周期律——《大题精做》2017-2018学年高一化学人教必修22016-2017学年江西省奉新县第一中学高一下学期第一次月考化学试卷
更新时间:2017-04-10 19:36:36
|
相似题推荐
解答题-实验探究题
|
较难
(0.4)
【推荐1】某研究性学习小组设计了一组实验来探究元素周期律。甲同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图1装置来一次性完成N、C、Si三种非金属元素的非金属性强弱比较的实验研究;乙同学设计了如图2装置来验证卤族元素性质的递变规律。图2中,A、B、C三处分别是沾有NaBr溶液的棉花、湿润的淀粉KI试纸、湿润红纸。已知常温下浓盐酸与高锰酸钾能反应生成氯气。

(1)甲同学实验(如图1)中选用的三种物质名称分别为:______________________________ ;
(2)乙同学实验(如图2)中:A处反应的离子方程式为:_______________________________ ;
B处的实验现象为:___________________________ ;
该实验不能完全证明卤素性质的递变规律,请简述原因:__________________ 。

(1)甲同学实验(如图1)中选用的三种物质名称分别为:
(2)乙同学实验(如图2)中:A处反应的离子方程式为:
B处的实验现象为:
该实验不能完全证明卤素性质的递变规律,请简述原因:
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐2】为验证氯元素的非金属性比硫元素的非金属性强,某化学实验小组设计了如图实验,请回答下列问题:
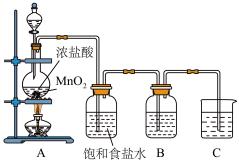
(1)装置B中盛放的试剂是___ (填选项),实验现象为___ ,化学反应方程式是______ 。
A.Na2S溶液 B.Na2SO3溶液 C.Na2SO4溶液
(2)装置C中盛放烧碱稀溶液,目的是______ 。反应的离子方程式是______ 。
(3)不能证明氯元素比硫元素非金属性强的依据为_____ 。(填序号)
①氯原子比硫原子更容易获得电子形成离子
②次氯酸的氧化性比稀硫酸强
③S2-比Cl-还原性强
④HCl比H2S酸性强
(4)若B瓶中盛放KI溶液和CCl4试剂,实验后,振荡、静置,会出现分层,下层呈紫红色的实验现象,若B瓶中通入标准状况下44.8L氯气全部参加反应,则转移的电子数目是_____ 。

(1)装置B中盛放的试剂是
A.Na2S溶液 B.Na2SO3溶液 C.Na2SO4溶液
(2)装置C中盛放烧碱稀溶液,目的是
(3)不能证明氯元素比硫元素非金属性强的依据为
①氯原子比硫原子更容易获得电子形成离子
②次氯酸的氧化性比稀硫酸强
③S2-比Cl-还原性强
④HCl比H2S酸性强
(4)若B瓶中盛放KI溶液和CCl4试剂,实验后,振荡、静置,会出现分层,下层呈紫红色的实验现象,若B瓶中通入标准状况下44.8L氯气全部参加反应,则转移的电子数目是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐3】某研究性学习小组设计了一组实验验证元素周期律。
Ⅰ.为了实验验证镁和铝的金属性强弱,学生甲和学生乙分别设计了两种不同的方法:
方案一:学生甲用水作试剂,比较镁和铝与水反应的情况
方案二:学生乙用稀盐酸作试剂,比较镁和铝与稀盐酸反应的情况
(1)以上两实验方案实验现象较为明显的是_____________ 。
(2)学生乙在实验中取了一段黑色的镁带,投入稀盐酸中,现象不十分明显,请分析原因_________________ 。
Ⅱ. (3) 向Na2S溶液中通入氯气出现黄色浑浊,可证明Cl的非金属性比S强,反应的离子方程式为_____________________________ 。
Ⅲ.利用如图装置可验证同主族元素非金属性的变化规律。

(4)仪器B的名称为__________ ,干燥管D的作用是__________________ 。
(5)若要证明非金属性: Cl>I,则A中加浓盐酸,B中加KMnO4(KMnO4与浓盐酸常温下反应生成氯气),C中加淀粉—碘化钾混合溶液,观察到C中溶液_____________________ (填现象),即可证明。从环境保护的观点考虑,此装置缺少尾气处理装置,可用____________ 溶液吸收尾气。
(6)若要证明非金属性: C>Si,则在A中加盐酸、B中加CaCO3、C中加Na2SiO3溶液。观察到C中溶液______________________ (填现象),即可证明。但有的同学认为盐酸具有挥发性,可进入C中干扰实验,应在两装置间添加装有__________________ 溶液的洗气瓶除去。
Ⅰ.为了实验验证镁和铝的金属性强弱,学生甲和学生乙分别设计了两种不同的方法:
方案一:学生甲用水作试剂,比较镁和铝与水反应的情况
方案二:学生乙用稀盐酸作试剂,比较镁和铝与稀盐酸反应的情况
(1)以上两实验方案实验现象较为明显的是
(2)学生乙在实验中取了一段黑色的镁带,投入稀盐酸中,现象不十分明显,请分析原因
Ⅱ. (3) 向Na2S溶液中通入氯气出现黄色浑浊,可证明Cl的非金属性比S强,反应的离子方程式为
Ⅲ.利用如图装置可验证同主族元素非金属性的变化规律。

(4)仪器B的名称为
(5)若要证明非金属性: Cl>I,则A中加浓盐酸,B中加KMnO4(KMnO4与浓盐酸常温下反应生成氯气),C中加淀粉—碘化钾混合溶液,观察到C中溶液
(6)若要证明非金属性: C>Si,则在A中加盐酸、B中加CaCO3、C中加Na2SiO3溶液。观察到C中溶液
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐1】某化学兴趣小组探究 溶液与
溶液与 溶液的反应。向
溶液的反应。向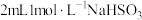 溶液
溶液 中逐滴加入
中逐滴加入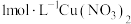 溶液,溶液变为绿色,静置
溶液,溶液变为绿色,静置 后,溶液变蓝,底部产生大量砖红色沉淀。
后,溶液变蓝,底部产生大量砖红色沉淀。
(1)测得 溶液
溶液 ,结合化学原理解释原因
,结合化学原理解释原因________________ 。
(2)甲同学认为 溶液与
溶液与 溶液发生了氧化还原反应。通过检验反应体系中是否含有
溶液发生了氧化还原反应。通过检验反应体系中是否含有 即可证明,检验
即可证明,检验 的方法是
的方法是________________ 。
(3)乙同学认为上述方法不能排除空气中 的干扰,应该进一步分析沉淀的成分。对反应产物中的砖红色沉淀提出以下假设:
的干扰,应该进一步分析沉淀的成分。对反应产物中的砖红色沉淀提出以下假设:
假设1:砖红色沉淀为 ;
;
假设2:砖红色沉淀为 ;
;
假设3:________________ ..
(4)查阅资料1: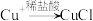 (白色难溶固体)
(白色难溶固体)
将砖红色沉淀过滤洗涤后,滴加 盐酸至过量,
盐酸至过量,________________ (填实验现象),可证明假设1成立,同时溶液变为蓝绿色,并伴有刺激性气味的气体生成。
(5)丙同学做对照实验时,向 中滴加
中滴加 盐酸至过量后,没有观察到溶液变蓝和生成气体的现象。因此,他认为砖红色沉淀中还可能含有其它成分,并设计实验进行证实。
盐酸至过量后,没有观察到溶液变蓝和生成气体的现象。因此,他认为砖红色沉淀中还可能含有其它成分,并设计实验进行证实。
①刺激性气味的气体可能是 或
或 ,在试管口用
,在试管口用蘸有碘水的淀粉试纸 检验,发现蓝色褪去,写出反应的离子方程式________________ 。
②向红色沉淀中加入过量氨水,发现沉淀溶解,溶液立即变蓝。 被空气氧化缓慢变蓝的原理
被空气氧化缓慢变蓝的原理________________ 。
③上述实验现象表明,砖红沉淀中除了含有 外,还含有
外,还含有________ 。(写出离子成分即可)
(6)丁同学通过如图装置证明了此条件下, 也能氧化
也能氧化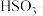 ,图中甲溶液是
,图中甲溶液是________ ,通过对比实验证明了此时空气中的 不是
不是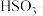 被氧化的主要原因,操作及现象是
被氧化的主要原因,操作及现象是________________ 。
 溶液与
溶液与 溶液的反应。向
溶液的反应。向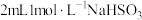 溶液
溶液 中逐滴加入
中逐滴加入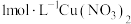 溶液,溶液变为绿色,静置
溶液,溶液变为绿色,静置 后,溶液变蓝,底部产生大量砖红色沉淀。
后,溶液变蓝,底部产生大量砖红色沉淀。(1)测得
 溶液
溶液 ,结合化学原理解释原因
,结合化学原理解释原因(2)甲同学认为
 溶液与
溶液与 溶液发生了氧化还原反应。通过检验反应体系中是否含有
溶液发生了氧化还原反应。通过检验反应体系中是否含有 即可证明,检验
即可证明,检验 的方法是
的方法是(3)乙同学认为上述方法不能排除空气中
 的干扰,应该进一步分析沉淀的成分。对反应产物中的砖红色沉淀提出以下假设:
的干扰,应该进一步分析沉淀的成分。对反应产物中的砖红色沉淀提出以下假设:假设1:砖红色沉淀为
 ;
;假设2:砖红色沉淀为
 ;
;假设3:
(4)查阅资料1:
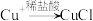 (白色难溶固体)
(白色难溶固体)将砖红色沉淀过滤洗涤后,滴加
 盐酸至过量,
盐酸至过量,(5)丙同学做对照实验时,向
 中滴加
中滴加 盐酸至过量后,没有观察到溶液变蓝和生成气体的现象。因此,他认为砖红色沉淀中还可能含有其它成分,并设计实验进行证实。
盐酸至过量后,没有观察到溶液变蓝和生成气体的现象。因此,他认为砖红色沉淀中还可能含有其它成分,并设计实验进行证实。①刺激性气味的气体可能是
 或
或 ,在试管口用
,在试管口用②向红色沉淀中加入过量氨水,发现沉淀溶解,溶液立即变蓝。
查阅资料2:
 被空气氧化缓慢变蓝的原理
被空气氧化缓慢变蓝的原理③上述实验现象表明,砖红沉淀中除了含有
 外,还含有
外,还含有(6)丁同学通过如图装置证明了此条件下,
 也能氧化
也能氧化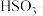 ,图中甲溶液是
,图中甲溶液是 不是
不是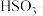 被氧化的主要原因,操作及现象是
被氧化的主要原因,操作及现象是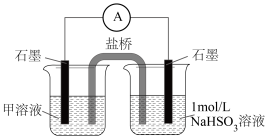
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐2】某研究小组探究SO2和Fe(NO3)3溶液的反应,其反应装置如下图所示:

已知:1.0 mol·L-1的Fe(NO3)3溶液的pH=1(即c(H+)=0.1 mol·L-1),回答下列问题:
(1)装置A中反应的化学方程式是_____________________________________________
(2)滴加浓硫酸之前应打开弹簧夹向装置中通入一段时间的N2,目的是________________________________
(3)装置B中产生了白色沉淀,其成分是___________ ,说明SO2具有___________ 性。
(4)分析B中产生白色沉淀的原因:
猜想1:SO2与Fe3+、酸性条件下NO3-都反应;
猜想2:___________________ ;
猜想3:在酸性条件下SO2与NO3—反应;
①按猜想2,装置B中反应的离子方程式是_____________________________________ ;
②按猜想3,只需将装置B中的Fe(NO3)3溶液替换为等体积的下列溶液,在相同条件下进行实验。应选择的试剂是________________ (填字母)。
A.1.5 mol·L-1Fe(NO3)2溶液
B.0.1 mol·L-1硝酸钠溶液
C.6.0 mol·L-1 NaNO3和0.2 mol·L-1盐酸等体积混合的溶液
D.3.0 mol·L-1 NaNO3和0.1 mol·L-1盐酸等体积混合的溶液

已知:1.0 mol·L-1的Fe(NO3)3溶液的pH=1(即c(H+)=0.1 mol·L-1),回答下列问题:
(1)装置A中反应的化学方程式是
(2)滴加浓硫酸之前应打开弹簧夹向装置中通入一段时间的N2,目的是
(3)装置B中产生了白色沉淀,其成分是
(4)分析B中产生白色沉淀的原因:
猜想1:SO2与Fe3+、酸性条件下NO3-都反应;
猜想2:
猜想3:在酸性条件下SO2与NO3—反应;
①按猜想2,装置B中反应的离子方程式是
②按猜想3,只需将装置B中的Fe(NO3)3溶液替换为等体积的下列溶液,在相同条件下进行实验。应选择的试剂是
A.1.5 mol·L-1Fe(NO3)2溶液
B.0.1 mol·L-1硝酸钠溶液
C.6.0 mol·L-1 NaNO3和0.2 mol·L-1盐酸等体积混合的溶液
D.3.0 mol·L-1 NaNO3和0.1 mol·L-1盐酸等体积混合的溶液
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐3】CaS微溶于水,常用于制发光漆,还用于医药工业、重金属处理及环保中。可用硫酸钙与焦炭高温反应制备,主反应 ,该反应过程中还可能产生
,该反应过程中还可能产生 、
、 、CaO等副产物。某兴趣小组为了探究该反应的总化学方程式,设计了如图所示的实验装置[图中所用试剂均为足量,假设产生的气体在相应的装置中完全反应,CO不与酸性
、CaO等副产物。某兴趣小组为了探究该反应的总化学方程式,设计了如图所示的实验装置[图中所用试剂均为足量,假设产生的气体在相应的装置中完全反应,CO不与酸性 溶液反应]
溶液反应]
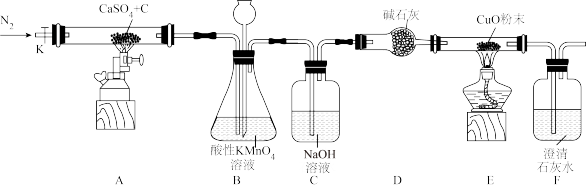
(1)仪器D的名称_______ ;实验开始前要通入 的目的是
的目的是_______ 。
(2)长颈斗的作用是_______ 。
(3)B中溶液颜色变浅,写出其中反应的离子方程式_______ 。
(4)能说明产物中有CO的实验现象是_______ 。
(5)取A中少量剩余固体溶于水,并不断搅拌一段时间后有淡黄色浑浊出现,请解释产生该现象的原因_______ 。
(6)如果实验前后B、C、E装置的质量变化分别为增重1.28g,增重0.44g,减轻0.64g,忽略装置中原有的 ,则硫酸钙与焦炭高温焙烧时发生的总化学方程式为
,则硫酸钙与焦炭高温焙烧时发生的总化学方程式为_______ ;
 ,该反应过程中还可能产生
,该反应过程中还可能产生 、
、 、CaO等副产物。某兴趣小组为了探究该反应的总化学方程式,设计了如图所示的实验装置[图中所用试剂均为足量,假设产生的气体在相应的装置中完全反应,CO不与酸性
、CaO等副产物。某兴趣小组为了探究该反应的总化学方程式,设计了如图所示的实验装置[图中所用试剂均为足量,假设产生的气体在相应的装置中完全反应,CO不与酸性 溶液反应]
溶液反应]
(1)仪器D的名称
 的目的是
的目的是(2)长颈斗的作用是
(3)B中溶液颜色变浅,写出其中反应的离子方程式
(4)能说明产物中有CO的实验现象是
(5)取A中少量剩余固体溶于水,并不断搅拌一段时间后有淡黄色浑浊出现,请解释产生该现象的原因
(6)如果实验前后B、C、E装置的质量变化分别为增重1.28g,增重0.44g,减轻0.64g,忽略装置中原有的
 ,则硫酸钙与焦炭高温焙烧时发生的总化学方程式为
,则硫酸钙与焦炭高温焙烧时发生的总化学方程式为
您最近一年使用:0次



