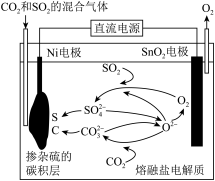
—种以Na2SO4为电解质的钠离子电池的总反应如下,下列有关说法正确的是
NaTi2(PO4)3+Zn+Na2SO4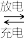 Na3Ti2(PO4)3+ZnSO4
Na3Ti2(PO4)3+ZnSO4
NaTi2(PO4)3+Zn+Na2SO4
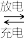 Na3Ti2(PO4)3+ZnSO4
Na3Ti2(PO4)3+ZnSO4| A.放电时,NaTi2(PO4)3发生氧化反应 | B.放电时,Na+向锌电极移动 |
C.充电时,阳极反应式为[Ti2(PO4)3]-+2e- [Ti2(PO4)3]3- [Ti2(PO4)3]3- | D.充电时,每转移0.2mol电子,理论上阴极增重6.5g |
更新时间:2017-05-15 14:06:02
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】肼(N2H4)空气燃料电池是一种环保碱性燃料电池,其电解质溶液是20%~30%的KOH溶液。电池总反应为N2H4+O2=N2↑+2H2O。下列关于该燃料电池工作时的说法正确的是( )
| A.溶液中阴离子物质的量基本不变 |
| B.正极的电极反应是N2H4+4OH--4e-=4H2O+N2↑ |
| C.正极的电极反应是O2+4H++4e-=2H2O |
| D.溶液中阴离子向正极移动 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】利用反应6NO2+8NH3=7N2+12H2O设计的电池装置如图所示,该装置既能有效消除氮氧化物的排放减轻环境污染,又能充分利用化学能。下列说法错误的是
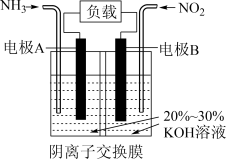
| A.电极B为正极,发生还原反应 |
| B.当有0.5molNO2被处理时,外电路中通过电子3mol |
| C.电池工作时,OH-从右向左迁移 |
| D.电极B的电极反应式为2NO2+8e-+4H2O=N2+8OH- |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】酒精检测仪可帮助执法交警测试驾驶员饮酒的多少,其工作原理示意图如下图所示。反应原理为:CH3CH2OH+O2=CH3COOH+H2O,被测者呼出气体中所含的酒精被输送到电池中反应产生微小电流,该电流经电子放大器放大后在液晶显示屏上显示其酒精含量。下列说法正确的是( )


| A.电解质溶液中的H+移向a电极 |
| B.b为正极,电极反应式为:O2+4H++4e-=2H2O |
| C.若有0.4 mol电子转移,则在标准状况下消耗4.48 L氧气 |
| D.呼出气体中酒精含量越高,微处理器中通过的电流越小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列有关原电池的说法正确的是( )
| A.将生铁投入稀盐酸中不能形成原电池 |
| B.镀锌铁放入稀硫酸中后,铁作负极 |
| C.铝片和镁片用导线连接后插入NaOH溶液中,Mg较活泼作负极 |
| D.铝片和铜片用导线连接后插入浓硝酸中,铜作负极 |
您最近一年使用:0次
【推荐3】下列实验操作所得的实验现象及结论均正确的是
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 将少量Na2SO3样品溶于水,滴加足量盐酸酸化的Ba(NO3)2溶液 | 有白色沉淀产生 | 说明Na2SO3已变质 |
| B | 镁、铝为电极,氢氧化钠为电解质的原电池装置 | 铝表面有气泡 | 金属活动性:Mg>Al |
| C | 将某气体通入品红溶液中 | 溶液褪色 | 该气体一定是SO2 |
| D | 将10mL2mol/L的KI溶液与1mL1mol/LFeCl3溶液混合 | 充分反应后,滴加数滴KSCN溶液,溶液颜色变红 | 该反应为可逆反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】钠硫电池以熔融金属钠、熔融硫和多硫化钠(Na2Sx)分别作为两个电极的反应物,固体Al2O3陶瓷(可传导Na+)为电解质,反应原理如图所示。下列说法正确的是
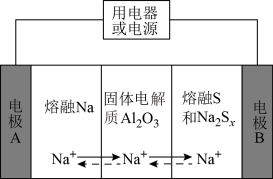

| A.放电时,电极A为正极 |
B.充电时,电极B与外接电源正极相连,电极反应式为S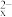 -2e-=xS -2e-=xS |
| C.当Na+由A极向B极移动时,能量转换方式为电能转化为化学能 |
| D.钠硫电池在常温下能正常工作 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】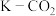 电池中活泼的钾负极容易产生枝晶状沉积物,导致正极催化剂活性不足与较高的充电过电位,容易引发电解液氧化分解,恶化电池性能。近日,我国科研团队通过对该电池正、负极同时改进,实现了稳定高效且可遵循环的
电池中活泼的钾负极容易产生枝晶状沉积物,导致正极催化剂活性不足与较高的充电过电位,容易引发电解液氧化分解,恶化电池性能。近日,我国科研团队通过对该电池正、负极同时改进,实现了稳定高效且可遵循环的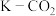 电池。电池总反应为
电池。电池总反应为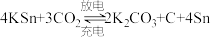 。
。

下列说法错误的是
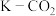 电池中活泼的钾负极容易产生枝晶状沉积物,导致正极催化剂活性不足与较高的充电过电位,容易引发电解液氧化分解,恶化电池性能。近日,我国科研团队通过对该电池正、负极同时改进,实现了稳定高效且可遵循环的
电池中活泼的钾负极容易产生枝晶状沉积物,导致正极催化剂活性不足与较高的充电过电位,容易引发电解液氧化分解,恶化电池性能。近日,我国科研团队通过对该电池正、负极同时改进,实现了稳定高效且可遵循环的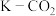 电池。电池总反应为
电池。电池总反应为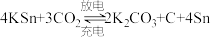 。
。
下列说法错误的是
A.活泼的钾负极替换成 合金是为了改善负极侧的枝晶问题 合金是为了改善负极侧的枝晶问题 |
B.电池的正极反应式为 |
| C.在碳纳米管正极表面引入羧酸根离子,可以使放电产物更易于可逆分解,降低充电过电位 |
D.充电时,每生成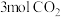 。阴极质量减少 。阴极质量减少 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】以NaCl溶液模拟海水,采用惰性电极处理有机废水的装置如图所示(以含 的溶液为例)。下列说法不正确的是
的溶液为例)。下列说法不正确的是

 的溶液为例)。下列说法不正确的是
的溶液为例)。下列说法不正确的是
A.负极反应为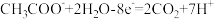 |
| B.隔膜1为阴离子交换膜,隔膜2为阳离子交换膜 |
| C.当电路中转移1mol电子时,模拟海水理论上最多可除盐58.5g |
| D.电池工作一段时间后,正、负极产生气体的物质的量之比为1:2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】铅蓄电池在现代生活中有广泛应用,其电极材料是Pb和PbO2,电解液是硫酸溶液。现用铅蓄电池电解硫酸钠溶液一段时间后,假设电解时温度不变且惰性电极,下列说法正确的是
| A.蓄电池放电时,每消耗0.1molPb,共生成0.1mol PbSO4 |
| B.电解硫酸钠溶液时的阳极反应式为:4OH--4e-=2H2O+O2↑ |
| C.电解后,硫酸钠溶液中有晶体析出,但c(Na2SO4)会变小 |
| D.蓄电池放电一段时间后其电解液中H2SO4的浓度、密度都变大 |
您最近一年使用:0次