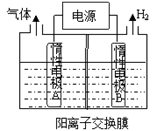
(I)利用如图装置电解制备LiOH,两电极区电解液分别为LiOH和LiCl溶液。
B极区电解液为__________ 溶液(填化学式),阳极电极反应式为_________________________ ,
电解过程中Li+向__________ 电极迁移(填“A”或“B”)。
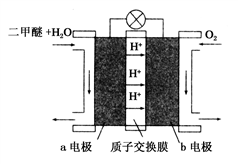
(Ⅱ)如图为绿色电源“二甲醚(CH3OCH3)燃料电池”的工作原理示意图.b电极是________ 极。
请写出负极的电极反应方程式:__________________
B极区电解液为
电解过程中Li+向

(Ⅱ)如图为绿色电源“二甲醚(CH3OCH3)燃料电池”的工作原理示意图.b电极是
请写出负极的电极反应方程式:

更新时间:2017-05-26 17:17:09
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)镍镉(Ni-Cd)电池是常用的二次电池,其总反应可以表示为:
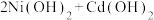 ,已知
,已知 和
和 均难溶于水但能溶于酸。
均难溶于水但能溶于酸。
①该电池的负极材料为____ 。
②该电池放电时,正极的电极反应式为____ 。
(2)用甲醇( )和
)和 组合形成的质子交换膜燃料电池的结构示意图如下图所示,已知该燃料电池的总反应
组合形成的质子交换膜燃料电池的结构示意图如下图所示,已知该燃料电池的总反应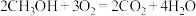 。
。

① 应从
应从_______ (填“a”或“b”)通入。
②电极c是燃料电池的_______ (填“正”或“负”)极,其电极反应式为_______ 。

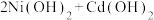 ,已知
,已知 和
和 均难溶于水但能溶于酸。
均难溶于水但能溶于酸。①该电池的负极材料为
②该电池放电时,正极的电极反应式为
(2)用甲醇(
 )和
)和 组合形成的质子交换膜燃料电池的结构示意图如下图所示,已知该燃料电池的总反应
组合形成的质子交换膜燃料电池的结构示意图如下图所示,已知该燃料电池的总反应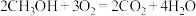 。
。
①
 应从
应从②电极c是燃料电池的
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】请分析下图装置。

⑴Fe电极是_____ (填“正”或“负”)极,其电极反应为________ ;
⑵Cu电极是_____ 电极,其电极反应为________________ 。
⑶若用浓硝酸做电解质溶液____ 做负极。

⑴Fe电极是
⑵Cu电极是
⑶若用浓硝酸做电解质溶液
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】2020年第七十五届联合国大会上,中国向世界郑重承诺在2030年前实现碳达峰,在2060年前实现碳中和。大力发展绿色能源、清洁能源是实现碳中和的最有效方法。
(1)原电池反应能够提供电能而不产生CO2气体,下图是某原电池装置图。
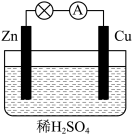
①Zn棒是原电池的___________ 极,发生___________ (填“氧化”或“还原”)反应。
②Cu棒上发生的电极反应是___________ 。
③溶液中H+向___________ (填“Zn”或“Cu”)电极定向移动。
(2)将上述装置中电解质稀H2SO4换为足量AgNO3溶液,灯泡也变亮,电流表指针偏转,无色溶液颜色没有变化。
①原电池的负极是___________ (填“Zn”或“Cu”),正极的电极反应是___________ 。
②若更换电解质时称量两个电极,质量恰好相等,放电一段时间后再称量两个电极,发现质量相差2.81g,则导线上通过的n(e-)=___________ mol。
(3)碱性锌锰电池是日常生活中常用电池,原电池反应是:Zn(①)+ 2MnO2 (②) +2H2O =Zn(OH)2(③)+2MnOOH(④)。该原电池的正极材料是___________ (填序号,下同),负极材料是___________ 。
(1)原电池反应能够提供电能而不产生CO2气体,下图是某原电池装置图。

①Zn棒是原电池的
②Cu棒上发生的电极反应是
③溶液中H+向
(2)将上述装置中电解质稀H2SO4换为足量AgNO3溶液,灯泡也变亮,电流表指针偏转,无色溶液颜色没有变化。
①原电池的负极是
②若更换电解质时称量两个电极,质量恰好相等,放电一段时间后再称量两个电极,发现质量相差2.81g,则导线上通过的n(e-)=
(3)碱性锌锰电池是日常生活中常用电池,原电池反应是:Zn(①)+ 2MnO2 (②) +2H2O =Zn(OH)2(③)+2MnOOH(④)。该原电池的正极材料是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】一次电池
(1)电池构成
(2)电池总反应与电极反应
碱性锌锰电池总反应式为Zn+2MnO2+H2O=2MnOOH+ZnO
①负极反应式是___________ ;
②正极反应式是___________ 。
(1)电池构成
| 酸性锌锰干电池 | 碱性锌锰干电池 | |
| 电极 | 负极: | 负极反应物: |
| 电解质溶液 |
碱性锌锰电池总反应式为Zn+2MnO2+H2O=2MnOOH+ZnO
①负极反应式是
②正极反应式是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
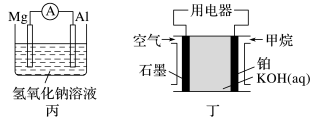
【推荐2】两位同学均想利用原电池反应检测金属的活动性顺序,两人均使用镁片和铝片作电极,甲同学将电极放入2mol/L H2SO4溶液A中,乙同学将电极放入6mol/L NaOH溶液B中,如图:

(1)原电池中的能量转化过程是将_______ 。
(2)A中正极的电极反应式为_______ ,电子的流向是由_______ (填“Al→Mg或Mg→Al”)。
(3)B中负极为_______ (填元素符号)。
(4)由此实验得出的下列结论中,正确的是_______(填字母)。
(5)两位同学继续用下图所示装置研究有关电化学的问题(甲、乙、丙三池中溶质足量),当闭合该装置的电键K时,观察到电流计的指针发生了偏转。
请回答下列问题:

①A电极的电极反应式为_______ 。
②一段时间后,丙池中F电极上出现的现象是_______ 。
③当乙池中C极质量减轻10.8 g时,甲池中B电极理论上消耗O2的体积为_______ mL(标准状况)。

(1)原电池中的能量转化过程是将
(2)A中正极的电极反应式为
(3)B中负极为
(4)由此实验得出的下列结论中,正确的是_______(填字母)。
| A.镁的金属性不一定比铝的金属性强 |
| B.该实验说明金属活动性顺序已过时,已没有实用价值 |
| C.该实验说明化学研究对象复杂,反应受条件影响较大,因此应具体问题具体分析 |
| D.上述实验证明了“直接利用金属活动性顺序判断原电池中的正负极”这种做法不可靠 |
请回答下列问题:

①A电极的电极反应式为
②一段时间后,丙池中F电极上出现的现象是
③当乙池中C极质量减轻10.8 g时,甲池中B电极理论上消耗O2的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】根据化学能转化为电能的相关知识,回答下列问题:
I.理论上讲,任何自发的氧化还原反应都可以设计成原电池。请利用反应“Cu+2Ag+=2Ag+Cu2+”设计一个化学电池(正极材料用碳棒),回答下列问题:
(1)该电池的负极材料是____ ,发生____ (填“氧化”或”还原”)反应,电解质溶液是____ 。
(2)正极上出现的现象是____ 。
II.为了探究原电池的工作原理,某化学学习小组设计了一组实验,其装置如图:
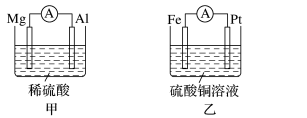
(3)丙装置中负极反应式为____ ,丁装置中负极反应式为____ 。
(4)电池的放电过程中,甲装置中溶液质量____ (填“增加”或“减少”);丁装置中溶液碱性____ (填“增强”或减弱”)。
(5)当甲装置导线中转移0.3mol电子时,正极生成气体____ L(标准状况下);假设开始时乙装置中两电极质量相等,导线中转移0.3mol电子时,两电极质量相差____ g。
I.理论上讲,任何自发的氧化还原反应都可以设计成原电池。请利用反应“Cu+2Ag+=2Ag+Cu2+”设计一个化学电池(正极材料用碳棒),回答下列问题:
(1)该电池的负极材料是
(2)正极上出现的现象是
II.为了探究原电池的工作原理,某化学学习小组设计了一组实验,其装置如图:


(3)丙装置中负极反应式为
(4)电池的放电过程中,甲装置中溶液质量
(5)当甲装置导线中转移0.3mol电子时,正极生成气体
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】储氢电池
(1)许多金属可固溶氢气,形成含氢的固溶体。在一定的温度和压力条件下,含氢的固溶体与氢气反应生成金属氢化物。
①正负极判断:氢做负极,金属不变价。
②电解质:碱性溶液。
(2)电极反应
总反应方程式:LaNi5H6+6NiOOH LaNi5+6Ni(OH)2
LaNi5+6Ni(OH)2
放电:
负极:___________ 。
正极:___________ 。
充电:
阴极:___________ 。
阳极:___________ 。
(1)许多金属可固溶氢气,形成含氢的固溶体。在一定的温度和压力条件下,含氢的固溶体与氢气反应生成金属氢化物。
①正负极判断:氢做负极,金属不变价。
②电解质:碱性溶液。
(2)电极反应
总反应方程式:LaNi5H6+6NiOOH
 LaNi5+6Ni(OH)2
LaNi5+6Ni(OH)2放电:
负极:
正极:
充电:
阴极:
阳极:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】原电池原理在生产生活中有着广泛的应用。
(1)食品保鲜常用的“双吸剂”是由还原铁粉、生石灰、氯化钠、炭粉按一定比例组成的混合物,可同时吸收水和氧气。“双吸剂”中CaO的主要作用是___________ ;在吸收氧气的过程中形成了原电池,则炭粉上发生的电极反应式为___________ 。
(2)电化学气敏传感器可用于监测大气环境中的SO2含量,其工作原理如图所示,电极a、b均为惰性电极。电极b是___________ 极(填“正”或“负”),请写出负极的电极反应式___________ ,放电时 向
向___________ 极(填“a”或“b”)迁移。

(3)铅蓄电池是一种广泛使用的二次电池,其放电时的反应方程式为: ,则其正极的电极反应式为
,则其正极的电极反应式为___________ ,当电路中通过2mol电子时负极质量增加___________ g。
(1)食品保鲜常用的“双吸剂”是由还原铁粉、生石灰、氯化钠、炭粉按一定比例组成的混合物,可同时吸收水和氧气。“双吸剂”中CaO的主要作用是
(2)电化学气敏传感器可用于监测大气环境中的SO2含量,其工作原理如图所示,电极a、b均为惰性电极。电极b是
 向
向
(3)铅蓄电池是一种广泛使用的二次电池,其放电时的反应方程式为:
 ,则其正极的电极反应式为
,则其正极的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】(1)高铁酸钾 不仅是一种理想的水处理剂,而且高铁电池的研制也在进行中。总反应式为
不仅是一种理想的水处理剂,而且高铁电池的研制也在进行中。总反应式为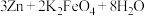
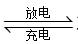
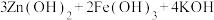 ,如图是高铁电池的模拟实验装置:
,如图是高铁电池的模拟实验装置:

①该电池盐桥中盛有饱和 溶液,此盐桥中氯离子向
溶液,此盐桥中氯离子向______ (填“左”或“右”)移动。
②该电池放电时正极的电极反应式为______ ;充电时每转移0.3mol电子,有______ mol 生成,正极附近溶液的碱性
生成,正极附近溶液的碱性______ (填“增强”,“不变”或“减弱”)。
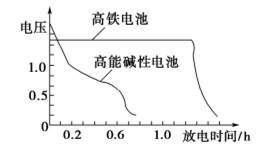
③上图为高铁电池和常用的高能碱性电池的放电曲线,由此可得出高铁电池的优点有_________________ 。
(2)“ ”电池可将
”电池可将 变废为宝。我国科研人员研制出的可充电“
变废为宝。我国科研人员研制出的可充电“ ”电池,以钠箔和多壁碳纳米管(MWCNT)为电极材料,总反应为
”电池,以钠箔和多壁碳纳米管(MWCNT)为电极材料,总反应为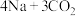

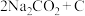 。放电时该电池“吸入”
。放电时该电池“吸入” ,其工作原理如图所示:
,其工作原理如图所示:
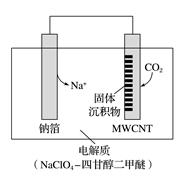
①充电时,正极的电极反应式为________________________________ 。
②放电时,若生成的 和
和 全部沉积在电极表面,当转移0.2mol
全部沉积在电极表面,当转移0.2mol 时,两极的质量差为
时,两极的质量差为______ 。
 不仅是一种理想的水处理剂,而且高铁电池的研制也在进行中。总反应式为
不仅是一种理想的水处理剂,而且高铁电池的研制也在进行中。总反应式为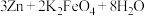

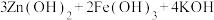 ,如图是高铁电池的模拟实验装置:
,如图是高铁电池的模拟实验装置:
①该电池盐桥中盛有饱和
 溶液,此盐桥中氯离子向
溶液,此盐桥中氯离子向②该电池放电时正极的电极反应式为
 生成,正极附近溶液的碱性
生成,正极附近溶液的碱性
③上图为高铁电池和常用的高能碱性电池的放电曲线,由此可得出高铁电池的优点有
(2)“
 ”电池可将
”电池可将 变废为宝。我国科研人员研制出的可充电“
变废为宝。我国科研人员研制出的可充电“ ”电池,以钠箔和多壁碳纳米管(MWCNT)为电极材料,总反应为
”电池,以钠箔和多壁碳纳米管(MWCNT)为电极材料,总反应为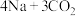

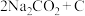 。放电时该电池“吸入”
。放电时该电池“吸入” ,其工作原理如图所示:
,其工作原理如图所示:
①充电时,正极的电极反应式为
②放电时,若生成的
 和
和 全部沉积在电极表面,当转移0.2mol
全部沉积在电极表面,当转移0.2mol 时,两极的质量差为
时,两极的质量差为
您最近一年使用:0次



