某课外小组分别用下图所示装置对原电池和电解原理进行实验探究.
请回答:
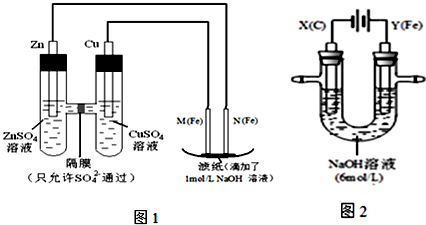
I.用图1所示装置进行第一组实验.
(1)在保证电极反应不变的情况下,不能替代Cu做电极的是______ (填字母序号).
A.铝 B.石墨 C.银 D.铂
(2)N极发生反应的电极反应式为_____________ .
(3)实验过程中,SO42-______ (填“从左向右”、“从右向左”或“不”)移动;滤纸上能观察到的现象有______________ .
II.用图2所示装置进行第二组实验.实验过程中,两极均有气体产生,Y极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清.查阅资料发现,高铁酸根(FeO42-)在溶液中呈紫红色.
(4)电解过程中,X极区溶液的pH______ (填“增大”、“减小”或“不变”).
(5)电解过程中,Y极发生的电极反应为_____________ 和4OH- - 4e-= 2H2O + O2↑
(6)若在X极收集到672mL气体,在Y极收集到168mL气体(均已折算为标准状况时气体体积),则Y电极(铁电极)质量减少______ g.
(7)在碱性锌电池中,用高铁酸钾作为正极材料,电池反应为:2K2FeO4+3Zn═Fe2O3+ZnO+2K2ZnO2 该电池正极发生的反应的电极反应式为__________ .

请回答:
I.用图1所示装置进行第一组实验.
(1)在保证电极反应不变的情况下,不能替代Cu做电极的是
A.铝 B.石墨 C.银 D.铂
(2)N极发生反应的电极反应式为
(3)实验过程中,SO42-
II.用图2所示装置进行第二组实验.实验过程中,两极均有气体产生,Y极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清.查阅资料发现,高铁酸根(FeO42-)在溶液中呈紫红色.
(4)电解过程中,X极区溶液的pH
(5)电解过程中,Y极发生的电极反应为
(6)若在X极收集到672mL气体,在Y极收集到168mL气体(均已折算为标准状况时气体体积),则Y电极(铁电极)质量减少
(7)在碱性锌电池中,用高铁酸钾作为正极材料,电池反应为:2K2FeO4+3Zn═Fe2O3+ZnO+2K2ZnO2 该电池正极发生的反应的电极反应式为
2014高三·全国·专题练习 查看更多[7]
(已下线)2014届高考化学二轮专题复习 电化学练习卷(已下线)2014高考名师推荐化学电解规律及电化学计算北京市2017届高三高考押题卷化学试题河南省南阳市第一中学校2016-2017学年高二下学期第三次月考化学试题河南省南阳市第一中学2016-2017学年高二下学期第三次月考化学试题2020届高考化学二轮复习大题精准训练 ——原电池、电解池填空题辽宁省沈阳市辽中区第一高级中学2020-2021学年高二下学期开学考试化学试题
更新时间:2017-06-17 16:00:44
|
相似题推荐
填空题
|
较难
(0.4)
名校
解题方法
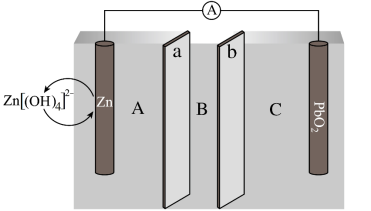
【推荐1】俄国科学家最近发明了一种Zn-PbO2电池,电解质为K2SO4、H2SO4和KOH,由a和b两种离子交换膜隔开,形成A、B、C三个电解质溶液区域,结构示意图如下:
回答下列问题:
(1)电池中,Zn为_______ 极,B区域的电解质为_______ (填“K2SO4”“H2SO4”或“KOH”)。
(2)电池反应的离子方程式为_______ 。
(3)阳离子交换膜为图中的_______ 膜(填“a”或“b”)。
(4)此电池中,消耗6.5gZn,理论上可产生的容量(电量)为_______ C(1mol电子的电量为1F,F=96500C/mol,结果保留整数)。

回答下列问题:
(1)电池中,Zn为
(2)电池反应的离子方程式为
(3)阳离子交换膜为图中的
(4)此电池中,消耗6.5gZn,理论上可产生的容量(电量)为
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐2】回答下列问题:
(1)双阴极微生物燃料电池处理NH -N废水的工作原理如图(a)所示,双阴极通过的电流相等,废水在电池中的运行模式如图(b)所示。
-N废水的工作原理如图(a)所示,双阴极通过的电流相等,废水在电池中的运行模式如图(b)所示。
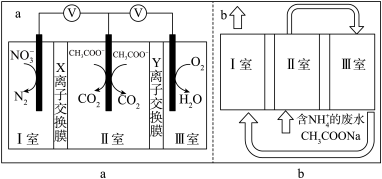
①Y离子交换膜为_______ (填“阳”或“阴”)离子交换膜。
②III室中除了O2→H2O,主要发生的反应还有_______ (用离子方程式表示)。
③生成3.5gN2,理论上需要消耗_______ gO2。
(2)西北工业大学的张健教授、德累斯顿工业大学的冯新亮院士等人报道了一种电催化半氢化策略,在室温条件下,水溶液介质中可选择性地将 还原为
还原为 ,其原理示意图如下:
,其原理示意图如下:

①阴极的电极反应式为:_______ 。
②同温同压下,相同时间内,若进口处气体物质的量为a ,出口处气体的总体积为进口处的x倍,则
,出口处气体的总体积为进口处的x倍,则 转化率为
转化率为_______ 。
(1)双阴极微生物燃料电池处理NH
 -N废水的工作原理如图(a)所示,双阴极通过的电流相等,废水在电池中的运行模式如图(b)所示。
-N废水的工作原理如图(a)所示,双阴极通过的电流相等,废水在电池中的运行模式如图(b)所示。
①Y离子交换膜为
②III室中除了O2→H2O,主要发生的反应还有
③生成3.5gN2,理论上需要消耗
(2)西北工业大学的张健教授、德累斯顿工业大学的冯新亮院士等人报道了一种电催化半氢化策略,在室温条件下,水溶液介质中可选择性地将
 还原为
还原为 ,其原理示意图如下:
,其原理示意图如下:
①阴极的电极反应式为:
②同温同压下,相同时间内,若进口处气体物质的量为a
 ,出口处气体的总体积为进口处的x倍,则
,出口处气体的总体积为进口处的x倍,则 转化率为
转化率为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐3】某研究小组用微生物电池模拟淡化海水,同时做电解实验,实验装置如下图所示,C、D是铂电极。
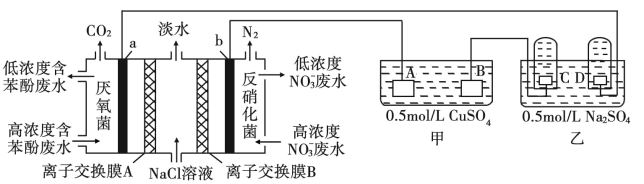
(1)若A、B是惰性电极
①写出D极的电极反应式_______ 。
②写出甲中总反应的离子方程式_______ 。
(2)若甲是铁片镀铜装置,A、B质量相同。当B和A的质量差为12.8g时,C极产生的气体在标准状况下的体积是_______ L。
(3)苯酚的分子式为 。
。
①离子交换膜A为_______ 离子交换膜(填“阴”或“阳”)。
②a极的电极反应式为_______ 。
③理论上每消除1mol苯酚,同时消除_______ mol  ;当电路中转移1mol电子时,模拟海水理论上除盐
;当电路中转移1mol电子时,模拟海水理论上除盐_______ g。

(1)若A、B是惰性电极
①写出D极的电极反应式
②写出甲中总反应的离子方程式
(2)若甲是铁片镀铜装置,A、B质量相同。当B和A的质量差为12.8g时,C极产生的气体在标准状况下的体积是
(3)苯酚的分子式为
 。
。①离子交换膜A为
②a极的电极反应式为
③理论上每消除1mol苯酚,同时消除
 ;当电路中转移1mol电子时,模拟海水理论上除盐
;当电路中转移1mol电子时,模拟海水理论上除盐
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐1】回答下列问题:
(1)根据氧化还原反应:Cu(s)+2Ag+(aq)=Cu2+(aq)+2Ag(s)设计原电池,若用铜、银做两个电极,开始两电极质量相等,当电路中转移0.01mol电子时两电极的质量差为____ g。
(2)某种燃料电池的工作原理示意如图所示,a、b均为惰性电极。
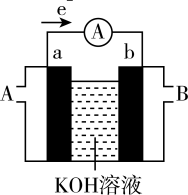
①假设使用的“燃料”是氢气(H2),则a极的电极反应式为____ 。若电池中氢气(H2)通入量为224mL(标准状况),且反应完全,则理论上通过电流表的电量为____ C。(已知一个电子所带电量为1.6×10−19C,NA约为6.02×1023mol−1)。
②假设使用的“燃料”是甲醇(CH3OH),则a极的电极反应式为____ ,如果消耗甲醇160g,假设化学能完全转化为电能,则转移电子的数目为____ (用NA表示)。
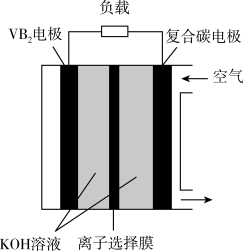
(3)一种高性能的碱性硼化钒(VB2)—空气电池如图所示,电池总反应为4VB2+11O2+20OH-+6H2O=8B(OH) +4VO
+4VO 。VB2电极发生的电极反应为
。VB2电极发生的电极反应为____ 。
(1)根据氧化还原反应:Cu(s)+2Ag+(aq)=Cu2+(aq)+2Ag(s)设计原电池,若用铜、银做两个电极,开始两电极质量相等,当电路中转移0.01mol电子时两电极的质量差为
(2)某种燃料电池的工作原理示意如图所示,a、b均为惰性电极。

①假设使用的“燃料”是氢气(H2),则a极的电极反应式为
②假设使用的“燃料”是甲醇(CH3OH),则a极的电极反应式为
(3)一种高性能的碱性硼化钒(VB2)—空气电池如图所示,电池总反应为4VB2+11O2+20OH-+6H2O=8B(OH)
 +4VO
+4VO 。VB2电极发生的电极反应为
。VB2电极发生的电极反应为
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】燃料电池在工业生产中有重要用途,肼燃料电池产物对环境无污染,能量高,有广泛的应用前景,其工作原理如图所示。回答下列问题
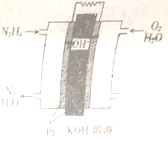
(1)该燃料电池中,负极通入的气体是_________ ,正极通入的气体是_________ .
(2)电池工作时,OH-向_____ 极移动,负极的电极反应式为_________ .
(3)肼在工业上常以氨和次氯酸钠为原料制得,其反应的化学方程式为2NH3+NaClO═N2H4+NaCl+H2O,该反应中每生成1molN2H4时,转移电子的物质的量为______ 。

(1)该燃料电池中,负极通入的气体是
(2)电池工作时,OH-向
(3)肼在工业上常以氨和次氯酸钠为原料制得,其反应的化学方程式为2NH3+NaClO═N2H4+NaCl+H2O,该反应中每生成1molN2H4时,转移电子的物质的量为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐3】已知废旧酸性干电池可通过酸浸、过滤等操作形成 、
、 的混合溶液,为了实现废旧普通氯化铵干电池中锌与
的混合溶液,为了实现废旧普通氯化铵干电池中锌与 的同时回收,某研究小组设计了如图实验探究装置:
的同时回收,某研究小组设计了如图实验探究装置:

回答下列问题:
(1)甲池是将_______ 能转化_______ 能的装置。
(2)乙池中石墨电极_______ 电子(填“得”或“失”),发生_______ 反应(填“氧化”或“还原”)。
(3)写出电池负极的电极反应式_______ 。
(4)写出乙池回收锌与 的总反应的离子方程式为
的总反应的离子方程式为_______ 。
(5)若消耗2.24L(标准状况) ,且无能量损失,电解池中回收制得19.5g单质Zn,计算乙池中电流效率
,且无能量损失,电解池中回收制得19.5g单质Zn,计算乙池中电流效率
_______ 。( 生成目标产物消耗的电子数/转移的电子总数×100%)。
生成目标产物消耗的电子数/转移的电子总数×100%)。
 、
、 的混合溶液,为了实现废旧普通氯化铵干电池中锌与
的混合溶液,为了实现废旧普通氯化铵干电池中锌与 的同时回收,某研究小组设计了如图实验探究装置:
的同时回收,某研究小组设计了如图实验探究装置:
回答下列问题:
(1)甲池是将
(2)乙池中石墨电极
(3)写出电池负极的电极反应式
(4)写出乙池回收锌与
 的总反应的离子方程式为
的总反应的离子方程式为(5)若消耗2.24L(标准状况)
 ,且无能量损失,电解池中回收制得19.5g单质Zn,计算乙池中电流效率
,且无能量损失,电解池中回收制得19.5g单质Zn,计算乙池中电流效率
 生成目标产物消耗的电子数/转移的电子总数×100%)。
生成目标产物消耗的电子数/转移的电子总数×100%)。
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐1】已知装置E是在石墨电极上镀银,回答下列问题:
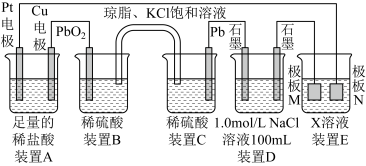
(1)装置A中Pt电极的名称为_______ (填“正极”、“负极”、“阴极”或“阳极”),装置A总反应的离子方程式为_______ 。
(2)装置B中电极上发生的电极反应为_______ ;盐桥中K+移向装置_______ (填“B”或“C”)。
(3)当装置D共收集到标况下5.6 L气体时,电路中通过的电子的物质的量为_______ mol。
(4)装置E中X为_______ ,极板M的材料为_______ 。

(1)装置A中Pt电极的名称为
(2)装置B中电极上发生的电极反应为
(3)当装置D共收集到标况下5.6 L气体时,电路中通过的电子的物质的量为
(4)装置E中X为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】氮是生命体的重要组成元素,自然界中氮的循环对于生命活动有重要意义。
(1)一种利用锂及其化合物的循环,将空气中的N2转化为NH3的过程如图所示。
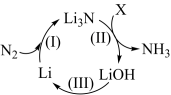
①X的化学式为___________ 。
②转化(Ⅲ)是电解熔融LiOH,该反应的化学方程式为___________ 。
(2)废水中氨氮(以NH3或NH 形式存在)含量过高,直接排放会造成水体富营养化。用NaClO可以将氨氮氧化去除,已知NH3比NH
形式存在)含量过高,直接排放会造成水体富营养化。用NaClO可以将氨氮氧化去除,已知NH3比NH 更易被氧化。NaClO除去水中氨氮的反应过程如下:
更易被氧化。NaClO除去水中氨氮的反应过程如下:
NaClO+H2O NaOH+HClO
NaOH+HClO
NH3+HClO=NH2Cl+H2O
2NH2Cl+HClO=N2↑+3HCl+H2O
①控制含氨氮废水的量和加入NaClO的量一定,测得反应相同时间,氨氮的去除率与溶液初始pH的关系如图-1所示。

(a)当pH<6时,氨氮去除率随溶液pH升高而升高的原因是:___________ 。
(b)当pH>10时,氨氮去除率随溶液pH升高而降低的原因是:___________ 。
②控制溶液的pH=7,测得反应相同时间,溶液中的氨氮、总氮(所有含氮微粒)的去除率随初始m(NaClO)∶m(NH3)的比例如图-2所示。当m(NaClO)∶m(NH3)>7.6,随m(NaClO)∶m(NH3)的增大,氨氮去除率始终接近100%,而总氮去除率逐渐降低的原因是___________ 。
③NaClO与NH3恰好完全反应时,反应的n(NaClO)∶n(NH3)的理论值是1.5.控制溶液的pH=7,测得反应相同时间,溶液中余氯含量与投入n(NaClO)∶n(NH3)的比值关系如图-3所示。水中的余氯的计算方法是向水中加入足量KI,生成的I2的物质的量看成是水中Cl2的物质的量。当n(NaClO)∶n(NH3)=1时,溶液中余氯含量较大的原因是___________ 。

(1)一种利用锂及其化合物的循环,将空气中的N2转化为NH3的过程如图所示。

①X的化学式为
②转化(Ⅲ)是电解熔融LiOH,该反应的化学方程式为
(2)废水中氨氮(以NH3或NH
 形式存在)含量过高,直接排放会造成水体富营养化。用NaClO可以将氨氮氧化去除,已知NH3比NH
形式存在)含量过高,直接排放会造成水体富营养化。用NaClO可以将氨氮氧化去除,已知NH3比NH 更易被氧化。NaClO除去水中氨氮的反应过程如下:
更易被氧化。NaClO除去水中氨氮的反应过程如下:NaClO+H2O
 NaOH+HClO
NaOH+HClONH3+HClO=NH2Cl+H2O
2NH2Cl+HClO=N2↑+3HCl+H2O
①控制含氨氮废水的量和加入NaClO的量一定,测得反应相同时间,氨氮的去除率与溶液初始pH的关系如图-1所示。

(a)当pH<6时,氨氮去除率随溶液pH升高而升高的原因是:
(b)当pH>10时,氨氮去除率随溶液pH升高而降低的原因是:
②控制溶液的pH=7,测得反应相同时间,溶液中的氨氮、总氮(所有含氮微粒)的去除率随初始m(NaClO)∶m(NH3)的比例如图-2所示。当m(NaClO)∶m(NH3)>7.6,随m(NaClO)∶m(NH3)的增大,氨氮去除率始终接近100%,而总氮去除率逐渐降低的原因是
③NaClO与NH3恰好完全反应时,反应的n(NaClO)∶n(NH3)的理论值是1.5.控制溶液的pH=7,测得反应相同时间,溶液中余氯含量与投入n(NaClO)∶n(NH3)的比值关系如图-3所示。水中的余氯的计算方法是向水中加入足量KI,生成的I2的物质的量看成是水中Cl2的物质的量。当n(NaClO)∶n(NH3)=1时,溶液中余氯含量较大的原因是

您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐3】海水中锂的提取
随着锂电池的广泛应用,锂已成为重要的战略资源,被称为白色石油。据估计,海水中锂的总含量为陆地锂总含量的5000倍以上,但海水中锂的质量浓度仅为0.1-0.2ppm,从海水提取锂首先需要对低浓度的Li+进行选择性富集。Li+能够嵌入某些氧化物并在一定条件下脱出,据此可以进行Li+的富集。
(1)以Li2CO3和MnO2为原料,充分混合后在720°C下煅烧3h,冷至室温后即可得到复合氧化物LiMn2O4(LMO)。用1molL-1的HCl在60°C处理LMO,将其中所有Li+置换后得到HMO,HMO可以和Li+反应再生成LMO,然后LMO与酸作用脱出Li+从而实现Li+富集。如此,可以循环处理。
①写出合成LiMn2O4的方程式_____ 。
②用酸处理LMO时,除离子交换反应之外,也会发生一个副反应,该副反应导致固体中Mn的平均氧化态有所升高,写出副反应对应的化学方程式。这一副反应对再生后的HMO的锂富集性能有何影响_____ ?
(2)利用电化学富集锂也是有效的方法之一、某电化学系统如图所示,其包含两个电池单元,中间区域置有具有一维孔道结构的λ-MnO2,该孔道可以容纳合适的阳离子进出。MnO2电极通过阳离子交换膜与两个电化学池中的对电极隔开,腔室1和2中的电解质分别为0.5M的Na2SO4.和0.1M的LiOH.该电化学系统的工作步骤如下:

i.向MnO2所在腔室通入海水,启动电源1,使海水中的Li+进入MnO2结构而形成LixMn2O4;
ii.关闭电源1和海水通道,启动电源2,同时向电极2上通入空气,使LixMn2O4中的Li+脱出进入腔室2。
①为衡量MnO2对Li+的富集效果,将0.50M的LiC1溶液通入MnO2(4.8mg)所在腔室,启动电源1,使电流恒定在5.0mA,累计工作325s后发现MnO2的电极电势快速下降,计算所得LixMn2O4中的x_____ 。
②写出上述过程中发生腔室2中阴极和阳极上的电极反应_____ 。
随着锂电池的广泛应用,锂已成为重要的战略资源,被称为白色石油。据估计,海水中锂的总含量为陆地锂总含量的5000倍以上,但海水中锂的质量浓度仅为0.1-0.2ppm,从海水提取锂首先需要对低浓度的Li+进行选择性富集。Li+能够嵌入某些氧化物并在一定条件下脱出,据此可以进行Li+的富集。
(1)以Li2CO3和MnO2为原料,充分混合后在720°C下煅烧3h,冷至室温后即可得到复合氧化物LiMn2O4(LMO)。用1molL-1的HCl在60°C处理LMO,将其中所有Li+置换后得到HMO,HMO可以和Li+反应再生成LMO,然后LMO与酸作用脱出Li+从而实现Li+富集。如此,可以循环处理。
①写出合成LiMn2O4的方程式
②用酸处理LMO时,除离子交换反应之外,也会发生一个副反应,该副反应导致固体中Mn的平均氧化态有所升高,写出副反应对应的化学方程式。这一副反应对再生后的HMO的锂富集性能有何影响
(2)利用电化学富集锂也是有效的方法之一、某电化学系统如图所示,其包含两个电池单元,中间区域置有具有一维孔道结构的λ-MnO2,该孔道可以容纳合适的阳离子进出。MnO2电极通过阳离子交换膜与两个电化学池中的对电极隔开,腔室1和2中的电解质分别为0.5M的Na2SO4.和0.1M的LiOH.该电化学系统的工作步骤如下:

i.向MnO2所在腔室通入海水,启动电源1,使海水中的Li+进入MnO2结构而形成LixMn2O4;
ii.关闭电源1和海水通道,启动电源2,同时向电极2上通入空气,使LixMn2O4中的Li+脱出进入腔室2。
①为衡量MnO2对Li+的富集效果,将0.50M的LiC1溶液通入MnO2(4.8mg)所在腔室,启动电源1,使电流恒定在5.0mA,累计工作325s后发现MnO2的电极电势快速下降,计算所得LixMn2O4中的x
②写出上述过程中发生腔室2中阴极和阳极上的电极反应
您最近一年使用:0次
【推荐1】I.探究原电池和电解池原理,对生产生活具有重要的意义。
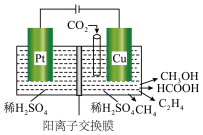
(1)近年来,有研究人员用 通过电催化生成多种燃料,其工作原理如图所示。请写出
通过电催化生成多种燃料,其工作原理如图所示。请写出 电极上产生
电极上产生 的电极反应式:
的电极反应式:___________ 。
(2)以惰性电极电解 溶液,通电一段时间后,加入0.1mol
溶液,通电一段时间后,加入0.1mol 可使溶液复原,则电路中转移电子为
可使溶液复原,则电路中转移电子为___________ mol。
(3)在直流电源作用下,双极膜中间层中的 解离为
解离为 和
和 。某技术人员利用双极膜(膜
。某技术人员利用双极膜(膜 、膜
、膜 )和离子交换膜高效制备
)和离子交换膜高效制备 和
和 ,工作原理如图所示:
,工作原理如图所示:
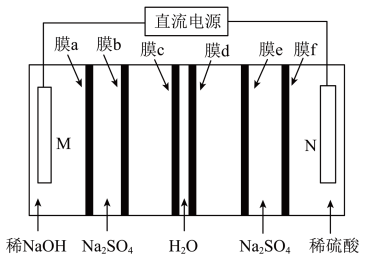
①膜 、
、 、
、 、
、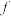 需选用阳离子交换膜的是
需选用阳离子交换膜的是___________
②当电路中转移2mol 时,整套装置将制得
时,整套装置将制得___________ mol
Ⅱ.利用电化学方法可以将CO₂有效地转化为 ,装置如图所示。
,装置如图所示。
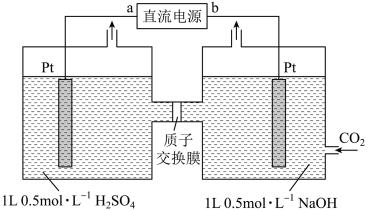
(4)若以铅蓄电池为直流电源,则铅蓄电池中 极的电极反应式为
极的电极反应式为___________ 。
(5)装置工作时,阴极除有 生成外,还可能生成副产物,降低电解效率。
生成外,还可能生成副产物,降低电解效率。
已知:
①副产物可能是___________ (写出一种即可)。
②标准状况下,当阳极生成氧气的体积为224mL时,测得整个阴极区内的 ,电解效率为
,电解效率为___________ (忽略电解前后溶液的体积变化)。
Ⅲ.利用新型镁—锂双离子二次电池(甲池)作电源同时电解乙池和丙池。
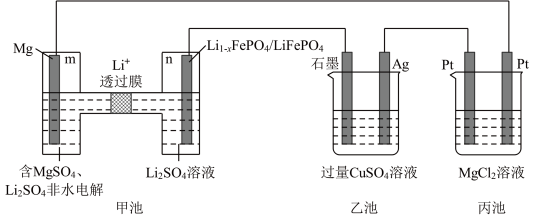
(6)放电时, 向
向___________ (填“ 极”或“
极”或“ 极”)移动;甲池中正极的电极反应式为
极”)移动;甲池中正极的电极反应式为___________ 。
(7)电解一段时间后,乙池中溶液的 将
将___________ (填“增大”、“减小”或“不变”)。
(8)丙池发生电解反应的总离子方程式为___________ 。
(1)近年来,有研究人员用
 通过电催化生成多种燃料,其工作原理如图所示。请写出
通过电催化生成多种燃料,其工作原理如图所示。请写出 电极上产生
电极上产生 的电极反应式:
的电极反应式:
(2)以惰性电极电解
 溶液,通电一段时间后,加入0.1mol
溶液,通电一段时间后,加入0.1mol 可使溶液复原,则电路中转移电子为
可使溶液复原,则电路中转移电子为(3)在直流电源作用下,双极膜中间层中的
 解离为
解离为 和
和 。某技术人员利用双极膜(膜
。某技术人员利用双极膜(膜 、膜
、膜 )和离子交换膜高效制备
)和离子交换膜高效制备 和
和 ,工作原理如图所示:
,工作原理如图所示:
①膜
 、
、 、
、 、
、 需选用阳离子交换膜的是
需选用阳离子交换膜的是②当电路中转移2mol
 时,整套装置将制得
时,整套装置将制得
Ⅱ.利用电化学方法可以将CO₂有效地转化为
 ,装置如图所示。
,装置如图所示。
(4)若以铅蓄电池为直流电源,则铅蓄电池中
 极的电极反应式为
极的电极反应式为(5)装置工作时,阴极除有
 生成外,还可能生成副产物,降低电解效率。
生成外,还可能生成副产物,降低电解效率。已知:

①副产物可能是
②标准状况下,当阳极生成氧气的体积为224mL时,测得整个阴极区内的
 ,电解效率为
,电解效率为Ⅲ.利用新型镁—锂双离子二次电池(甲池)作电源同时电解乙池和丙池。

(6)放电时,
 向
向 极”或“
极”或“ 极”)移动;甲池中正极的电极反应式为
极”)移动;甲池中正极的电极反应式为(7)电解一段时间后,乙池中溶液的
 将
将(8)丙池发生电解反应的总离子方程式为
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐2】电浮选凝聚法是工业上采用的一种污水处理方法:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3沉淀。Fe(OH)3有吸附性,可吸附污物而沉积下来,具有净化水的作用。阴极产生的气泡把污水中悬浮物带到水面形成浮渣层,除去浮渣层,即起到了浮选净化的作用。某科研小组用电浮选凝聚法处理污水,设计装置示意图,如图所示。
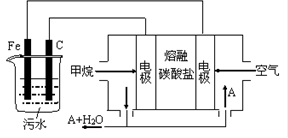
(1)实验时若污水中离子浓度较小,导电能力较差,产生气泡速率缓慢,无法使悬浮物形成浮渣。此时,可向污水中加入适量的____________ 。
a.Na2SO4 b.H2SO4 c.NaOH d.CH3COOH e.NaCl
(2)除污过程中污水池中阳离子将移向____ 极(填:“正”或“负”或“阴”或“阳”)。
(3)电解池阳极发生了两个电极反应,电极反应式是
Ⅰ. Fe-2e-=Fe2+ Ⅱ.______________________________________ 。
(4)以上电解过程是以上图右侧的燃料电池为电源,该燃料电池是以熔融碳酸盐为电解质,CH4为燃料,空气为氧化剂,稀土金属材料做电极。
①负极的电极反应是____________________________________________ ;
②为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定,电池工作时必须有部分A物质参加循环。A物质的电子式为__________ 。
(5)实验过程中,若在阴极产生了44.8 L(标准状况)气体,则熔融盐燃料电池消耗CH4(标准状况)_________ L。

(1)实验时若污水中离子浓度较小,导电能力较差,产生气泡速率缓慢,无法使悬浮物形成浮渣。此时,可向污水中加入适量的
a.Na2SO4 b.H2SO4 c.NaOH d.CH3COOH e.NaCl
(2)除污过程中污水池中阳离子将移向
(3)电解池阳极发生了两个电极反应,电极反应式是
Ⅰ. Fe-2e-=Fe2+ Ⅱ.
(4)以上电解过程是以上图右侧的燃料电池为电源,该燃料电池是以熔融碳酸盐为电解质,CH4为燃料,空气为氧化剂,稀土金属材料做电极。
①负极的电极反应是
②为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定,电池工作时必须有部分A物质参加循环。A物质的电子式为
(5)实验过程中,若在阴极产生了44.8 L(标准状况)气体,则熔融盐燃料电池消耗CH4(标准状况)
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】右图是一个化学过程的示意图。已知甲池的总反应式为:
2CH3OH+3O2+4KOH 2K2CO3+6H2O
2K2CO3+6H2O
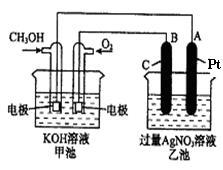
(1)请回答图中甲、乙两池的有关问题:甲池是_______________ 装置,B(石墨)电极的名称是____________ 。
(2)写出电极反应式:通入O2的电极的反应式__________ 。A(Pt)电极的反应式为_____________ ,
(3)乙池中反应的化学方程式为_______________________________ 。
(4)若乙池溶液体积为500mL,且忽略电解过程中溶液体积的变化,当乙池中A极的质量增加5.40g时:
①甲池中理论上消耗O2体积为______________ (标准状况下);
②乙池中所得溶液的pH=____________________ 。
2CH3OH+3O2+4KOH
 2K2CO3+6H2O
2K2CO3+6H2O
(1)请回答图中甲、乙两池的有关问题:甲池是
(2)写出电极反应式:通入O2的电极的反应式
(3)乙池中反应的化学方程式为
(4)若乙池溶液体积为500mL,且忽略电解过程中溶液体积的变化,当乙池中A极的质量增加5.40g时:
①甲池中理论上消耗O2体积为
②乙池中所得溶液的pH=
您最近一年使用:0次



