下列依据热化学方程式得出的结论正确的是
| A.已知2H2(g)+O2(g)=2H2O(g) △H=-483.6 kJ·mol-1,则氢气的燃烧热(△H)为-241.8 kJ·mol-1 |
| B.已知NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H=-57.3 kJ·mol-1,则含40.0g NaOH的稀溶液与稀醋酸完全中和,放出小于57.3kJ的热量 |
| C.已知2C(s)+2O2(g)=2CO2(g)△H = a;2C(s)+O2(g)=2CO(g);△H= b,则a>b |
| D.已知C (石墨,s)=C (金刚石,s) △H>0,则金刚石比石墨稳定 |
更新时间:2016-07-25 09:21:39
|
相似题推荐
未知-未知
|
适中
(0.65)
【推荐1】下列说法正确的是
| A.1mol酸与1mol碱完全反应放出的热量就是中和热 |
| B.燃烧热随化学方程式的化学计量数的改变而改变 |
| C.强酸强碱中和热的热化学方程式可表示为:H+(aq)+OHˉ(aq)═H2O(l)△H=57.3 kJ/mol |
| D.反应物总能量大于生成物总能量,则反应的△H<0 |
您最近一年使用:0次
未知-未知
|
适中
(0.65)
【推荐1】煤的气化是实施节能环保的一项重要措施。通常在高温下将煤转化为水煤气,再将水煤气作为气体燃料。有关热化学方程式如下:
①C(s)+H2O(g)=CO(g)+H2(g) ΔH1=131.3 kJ·mol-1
②2CO(g)+O2(g)=2CO2(g) ΔH2=-566.0 kJ·mol-1
③2H2(g)+O2(g)=2H2O(g) ΔH3=-483.6 kJ·mol-1
下列有关说法正确的是
①C(s)+H2O(g)=CO(g)+H2(g) ΔH1=131.3 kJ·mol-1
②2CO(g)+O2(g)=2CO2(g) ΔH2=-566.0 kJ·mol-1
③2H2(g)+O2(g)=2H2O(g) ΔH3=-483.6 kJ·mol-1
下列有关说法正确的是
| A.水煤气只能用作燃料 |
| B.水煤气是一种二次能源,比煤直接燃烧污染小 |
| C.等质量的CO和H2完全燃烧时,前者放热多 |
| D.由反应③可以确定H2的燃烧热ΔH=-241.8 kJ·mol-1 |
您最近一年使用:0次
未知-未知
|
适中
(0.65)
【推荐2】已知:①2H2(g)+O2(g)= 2H2O(g) ΔH=-483.6 kJ·mol-1
②H2(g) + S(g) = H2S(g) ΔH=-20.1 kJ·mol-1 。下列判断一定正确的是
②H2(g) + S(g) = H2S(g) ΔH=-20.1 kJ·mol-1 。下列判断一定正确的是
| A.1 mol氢气完全燃烧生成H2O(g)吸收241.8 kJ热量 |
| B.水蒸气和硫化氢的能量相差221.7 kJ |
| C.由①②知,水的热稳定性小于硫化氢 |
| D.反应②中改用固态硫,1 mol H2完全反应放热将小于20.1 kJ |
您最近一年使用:0次
未知-未知
|
适中
(0.64)
【推荐3】在101kPa 25℃时,1.0g乙烷气体完全燃烧生成液态水时放出热量52.0kJ,则乙烷燃烧的热化学方程式为( )
A.C2H6(g)+ O2(g)═2CO2(g)+3H2O(l)△H=﹣1560kJ•mol﹣1 O2(g)═2CO2(g)+3H2O(l)△H=﹣1560kJ•mol﹣1 |
| B.2C2H6(g)+7O2(g)═4CO2(g)+6H2O(g)△H=﹣1560kJ•mol﹣1 |
| C.2C2H6(g)+7O2(g)═4CO2(g)+6H2O(l)△H=+3120 kJ•mol﹣1 |
D.C2H6(g)+ O2(g)═2CO2(g)+3H2O(l)△H=﹣52.0kJ•mol﹣1 O2(g)═2CO2(g)+3H2O(l)△H=﹣52.0kJ•mol﹣1 |
您最近一年使用:0次
未知-未知
|
适中
(0.65)
【推荐1】在1100℃,一定容积的密闭容器中发生反应:FeO(s)+CO(g) Fe(s)+CO2(g) △H=a kJ/mol(a >0),下列有关该反应的说法正确的是
Fe(s)+CO2(g) △H=a kJ/mol(a >0),下列有关该反应的说法正确的是
 Fe(s)+CO2(g) △H=a kJ/mol(a >0),下列有关该反应的说法正确的是
Fe(s)+CO2(g) △H=a kJ/mol(a >0),下列有关该反应的说法正确的是| A.若生成1 mol Fe,则吸收的热量小于a kJ |
| B.若升高温度,正反应速率加快,逆反应速率加快,则化学平衡正向移动 |
| C.若增大压强反应向正反应方向进行 |
| D.若容器内压强不随时间变化,则可以判断该反应已达到化学平衡状态 |
您最近一年使用:0次


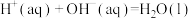
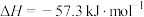 ,则
,则

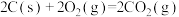
 ;
;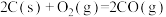
 ;则
;则
 (白磷,s)
(白磷,s) (红磷,s)
(红磷,s)

 ,则氢气燃烧热
,则氢气燃烧热


