计算后填空:
(1)在标准状况下,448 mL某气体的质量为0.64 g,这种气体的相对分子质量为______ 。
(2)某氯化铁与氯化钠的混合液,已知c(Fe3+)=0.2 mol·L-1,c(Cl-)=1 mol·L-1。则c(Na+)为______ 。
(3)19 g某二价金属的氯化物RCl2中含有0.4 mol的Cl-,则R的相对原子质量为_______ 。
(4)V L Fe2(SO4)3溶液中含Fe3+ m g,则溶液中SO42-的物质的量浓度为_____ mol·L-1。
(5)在无土栽培中,配制1 L含5 mol NH4Cl、1.6 mol KCl、2.4 mol K2SO4的某营养液,若用KCl、NH4Cl、(NH4)2SO4配制,则需KCl、NH4Cl的物质的量分别为______ 、______ 。
(6)如图所示, 分别向密闭容器内可移动活塞的两边充入空气(已知空气体积占整个容器容积的1/4)、H2和O2的混合气体,在标准状况下,若将H2、O2的混合气体点燃引爆,活塞先左弹,恢复原温度后,活塞右滑停留于容器的中央。则原来H2、O2的体积之比可能为
分别向密闭容器内可移动活塞的两边充入空气(已知空气体积占整个容器容积的1/4)、H2和O2的混合气体,在标准状况下,若将H2、O2的混合气体点燃引爆,活塞先左弹,恢复原温度后,活塞右滑停留于容器的中央。则原来H2、O2的体积之比可能为________ 。
(1)在标准状况下,448 mL某气体的质量为0.64 g,这种气体的相对分子质量为
(2)某氯化铁与氯化钠的混合液,已知c(Fe3+)=0.2 mol·L-1,c(Cl-)=1 mol·L-1。则c(Na+)为
(3)19 g某二价金属的氯化物RCl2中含有0.4 mol的Cl-,则R的相对原子质量为
(4)V L Fe2(SO4)3溶液中含Fe3+ m g,则溶液中SO42-的物质的量浓度为
(5)在无土栽培中,配制1 L含5 mol NH4Cl、1.6 mol KCl、2.4 mol K2SO4的某营养液,若用KCl、NH4Cl、(NH4)2SO4配制,则需KCl、NH4Cl的物质的量分别为
(6)如图所示,
 分别向密闭容器内可移动活塞的两边充入空气(已知空气体积占整个容器容积的1/4)、H2和O2的混合气体,在标准状况下,若将H2、O2的混合气体点燃引爆,活塞先左弹,恢复原温度后,活塞右滑停留于容器的中央。则原来H2、O2的体积之比可能为
分别向密闭容器内可移动活塞的两边充入空气(已知空气体积占整个容器容积的1/4)、H2和O2的混合气体,在标准状况下,若将H2、O2的混合气体点燃引爆,活塞先左弹,恢复原温度后,活塞右滑停留于容器的中央。则原来H2、O2的体积之比可能为
16-17高一上·河南周口·阶段练习 查看更多[6]
河南省温县第一高级中学2021-2022学年高三上学期12月月考化学试题安徽省霍邱县第二中学2021届高三上学期开学考试化学试题(已下线)2019年7月7日 《每日一题》 2020年高考一轮复习-每周一测人教版2017届高三单元精练检测一化学试题苏教版2017届高三单元精练检测一化学试题2016-2017学年河南省郸城中学高一上第一次考试化学卷
更新时间:2020-09-24 21:19:56
|
相似题推荐
计算题
|
较难
(0.4)
解题方法
【推荐1】将一定质量的镁铝合金样品全部溶于100mL某浓度的盐酸中。向所得溶液中滴加5.0mol/L的NaOH溶液,生成沉淀质量与加入的NaOH溶液体积关系如图所示。

(1)19.4g沉淀中含有Al(OH)3的质量为____________ ;
(2)盐酸的物质的量浓度为____________ .

(1)19.4g沉淀中含有Al(OH)3的质量为
(2)盐酸的物质的量浓度为
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
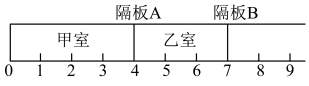
【推荐2】如图所示,一密闭容器被无摩擦、可滑动的两隔板A、B分成甲、乙两室。标准状况下,在乙室充入8.4g N2,甲室充入8.8g H2和O2的混合气体。
(1)甲室中H2与O2的质量比为_____________ ,甲室中原子个数约为 ____________ 个。
(2)维持温度不变,将隔板A固定在“3”处,将隔板B固定在“5”处,此时甲、乙两室中气体的压强比P(甲):P(乙)=______________ 。
(3)用电火花处理甲室中的气体使其充分反应,反应后恢复至标准状况。甲室与乙室此时的体积比为_____ 。
(1)甲室中H2与O2的质量比为
(2)维持温度不变,将隔板A固定在“3”处,将隔板B固定在“5”处,此时甲、乙两室中气体的压强比P(甲):P(乙)=
(3)用电火花处理甲室中的气体使其充分反应,反应后恢复至标准状况。甲室与乙室此时的体积比为
您最近一年使用:0次
计算题
|
较难
(0.4)
【推荐1】现有标准状况下V L 气体AB3,它的摩尔质量为M g·mol-1。则:
(1)该气体所含原子总数为________________ 个(列出计算式即可,下同)。
(2)该气体的质量为_____________ g。
(3)该气体溶于1L水中(不考虑反应),其溶液中溶质的质量分数为______________ 。
(4)该气体溶于水后形成1 L溶液,其溶液的物质的量浓度为_______________ mol·L-1。
(5)该气体溶于1L水中(不考虑反应),若所得溶液的密度为ρg·mL-1,则溶液的物质的量浓度为_____________________ mol·L-1
(1)该气体所含原子总数为
(2)该气体的质量为
(3)该气体溶于1L水中(不考虑反应),其溶液中溶质的质量分数为
(4)该气体溶于水后形成1 L溶液,其溶液的物质的量浓度为
(5)该气体溶于1L水中(不考虑反应),若所得溶液的密度为ρg·mL-1,则溶液的物质的量浓度为
您最近一年使用:0次
计算题
|
较难
(0.4)
名校
【推荐2】(1) 3.01×1023个CO2分子中含_____________ mol氧原子,在标准状况下其体积为____ L,0.4 molOH-的中有 ______ 个电子。
(2)实验中需取0.1mol CuSO4配制溶液,若用CuSO4 • 5H2O替代,则应称取CuSO4 • 5H2O的质最为___ g。
(3)同温同压下,等质量的N2和CO2所含分子数比为_____ ,体积比为________ 。
(4)某气体在标准状况下的密度为1.25g/L,则28g该气体所含有的分子数为_____________ 。
(5)在标准状况下22.4L由氮气和氧气组成的混合气体,其质量为30g,则其中氧气的质量为____ g。
(6)用98%的浓硫酸(ρ=1.84 g/cm3)配制1 mol/L的稀硫酸l00mL,配制过程中需量取浓硫酸____ mL。
(2)实验中需取0.1mol CuSO4配制溶液,若用CuSO4 • 5H2O替代,则应称取CuSO4 • 5H2O的质最为
(3)同温同压下,等质量的N2和CO2所含分子数比为
(4)某气体在标准状况下的密度为1.25g/L,则28g该气体所含有的分子数为
(5)在标准状况下22.4L由氮气和氧气组成的混合气体,其质量为30g,则其中氧气的质量为
(6)用98%的浓硫酸(ρ=1.84 g/cm3)配制1 mol/L的稀硫酸l00mL,配制过程中需量取浓硫酸
您最近一年使用:0次



