根据下列两个热化学方程式,回答下列问题:
2H2(g)+O2(g)=2H2O(1) ΔH=-571.6 kJ·mol-1
C3H8(g)+5O2(g)=3CO2(g)+4H2O(l) ΔH=-2 220 kJ·mol-1
(1)H2的燃烧热为_______ ,C3H8的燃烧热为_______ 。
(2)1 mol H2和2 mol C3H8组成的混合气体完全燃烧释放的热量为__________ 。
(3)现有H2和C3H8的混合气体共5 mol,完全燃烧时放热3 847kJ,则在混合气体中H2和C3H8的体积比是_______ 。
2H2(g)+O2(g)=2H2O(1) ΔH=-571.6 kJ·mol-1
C3H8(g)+5O2(g)=3CO2(g)+4H2O(l) ΔH=-2 220 kJ·mol-1
(1)H2的燃烧热为
(2)1 mol H2和2 mol C3H8组成的混合气体完全燃烧释放的热量为
(3)现有H2和C3H8的混合气体共5 mol,完全燃烧时放热3 847kJ,则在混合气体中H2和C3H8的体积比是
2017高二·全国·课时练习 查看更多[10]
(已下线)1.2 燃烧热 能源高中化学人教版 选修四 第一章 化学反应与能量 第二节 燃烧热 能源甘肃省岷县二中2018-2019学年高二上学期第一次月考化学试题(已下线)2019年8月29日《每日一题》人教选修4—— 燃烧热的计算福建省漳州市平和县第一中学2019-2020学年高二上学期第一次月考化学试题宁夏贺兰县景博中学2019-2020学年高二上学期第一次月考化学试题(已下线)第一章 化学反应与能量(基础过关)-2020-2021学年高二化学单元测试定心卷(人教版选修4)内蒙古自治区通辽市科左后旗甘旗卡第二高级中学2020-2021学年高二上学期期中考试化学试题新疆新和县实验中学2021-2022学年高二上学期第一次月考化学试题云南省文山州广南县第二中学校2021-2022学年高二上学期12月考试化学试题
更新时间:2017-11-27 08:01:08
|
相似题推荐
计算题
|
适中
(0.65)
名校
【推荐1】已知:2H2(g)+O2(g)=2 H2O(l) △H= -571.6 kJ·mol-1
H2(g)+1/2O2(g)=H2O(g) ΔH= -241.8 kJ/mol
C3H4(g)+4O2(g) = 3CO2(g) +2H2O(g) △H= -2100.0 kJ·mol-1
根据上面两个热化学方程式回答下列问题:
(1) H2的燃烧热为________________ ;
(2)1mol H2和2mol C3H4 组成的混合气体完全燃烧生成液态水时释放的热量为___ ;
(3)现有H2和C3H4的混合气体共5mol,完全燃烧生成CO2和气态水时,则放出热量(Q)的取值范围是____ ;若生成CO2和H2O的物质的量相等,则放出的热量是_____ 。
H2(g)+1/2O2(g)=H2O(g) ΔH= -241.8 kJ/mol
C3H4(g)+4O2(g) = 3CO2(g) +2H2O(g) △H= -2100.0 kJ·mol-1
根据上面两个热化学方程式回答下列问题:
(1) H2的燃烧热为
(2)1mol H2和2mol C3H4 组成的混合气体完全燃烧生成液态水时释放的热量为
(3)现有H2和C3H4的混合气体共5mol,完全燃烧生成CO2和气态水时,则放出热量(Q)的取值范围是
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】用化学用语完成以下各题:
(1)硫化氢在水中的电离方程式___ 。
(2)已知通常状况下,1.6g甲烷完全燃烧放出89.03kJ的热量,表示甲烷燃烧热的热化学方程式为___ 。
(3)用CO可以合成甲醇。已知:
CH3OH(g)+ O2(g)=CO2(g)+2H2O(l) ΔH=-764.6kJ·mol-1
O2(g)=CO2(g)+2H2O(l) ΔH=-764.6kJ·mol-1
CO(g)+ O2(g)=CO2(g) ΔH=-283.0kJ·mol-1
O2(g)=CO2(g) ΔH=-283.0kJ·mol-1
H2(g)+ O2(g)=H2O(l) ΔH=-285.8kJ·mol-1
O2(g)=H2O(l) ΔH=-285.8kJ·mol-1
则CO(g)与H2(g)合成CH3OH(g)的热化学方程式为___ 。
(4)油酸甘油酯(相对分子质量884)在体内代谢时可发生如下反应:C57H104O6(s)+80O2(g)=57CO2(g)+52H2O(l)
已知燃烧1kg该化合物释放出热量3.8×104kJ,油酸甘油酯的燃烧热为___ 。
(1)硫化氢在水中的电离方程式
(2)已知通常状况下,1.6g甲烷完全燃烧放出89.03kJ的热量,表示甲烷燃烧热的热化学方程式为
(3)用CO可以合成甲醇。已知:
CH3OH(g)+
 O2(g)=CO2(g)+2H2O(l) ΔH=-764.6kJ·mol-1
O2(g)=CO2(g)+2H2O(l) ΔH=-764.6kJ·mol-1CO(g)+
 O2(g)=CO2(g) ΔH=-283.0kJ·mol-1
O2(g)=CO2(g) ΔH=-283.0kJ·mol-1H2(g)+
 O2(g)=H2O(l) ΔH=-285.8kJ·mol-1
O2(g)=H2O(l) ΔH=-285.8kJ·mol-1则CO(g)与H2(g)合成CH3OH(g)的热化学方程式为
(4)油酸甘油酯(相对分子质量884)在体内代谢时可发生如下反应:C57H104O6(s)+80O2(g)=57CO2(g)+52H2O(l)
已知燃烧1kg该化合物释放出热量3.8×104kJ,油酸甘油酯的燃烧热为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】已知下列热化学方程式:
① H2(g) + O2(g) = H2O(l) △H = -285.8 kJ / mol
O2(g) = H2O(l) △H = -285.8 kJ / mol
② C(s) + O2(g) = CO2(g) △H = -393.5 kJ / mol
③ C(s) + H2O(g) =CO(g) + H2(g) △H= +131.5 kJ/mol
请回答:
(1)上述反应中属于放热反应的是_________ (填序号,下同),属于吸热反应的是_________ 。
(2)1 mol H2完全燃烧生成液态水,放出的热量为________________ 。
(3)碳的燃烧热△H=_______________ 。
(4)在25℃、101kPa下, 1g甲烷完全燃烧生成CO2和液态H2O,放出55 kJ的热量,写出表示甲烷燃烧热的热化学方程式__________________________________ 。
① H2(g) +
 O2(g) = H2O(l) △H = -285.8 kJ / mol
O2(g) = H2O(l) △H = -285.8 kJ / mol② C(s) + O2(g) = CO2(g) △H = -393.5 kJ / mol
③ C(s) + H2O(g) =CO(g) + H2(g) △H= +131.5 kJ/mol
请回答:
(1)上述反应中属于放热反应的是
(2)1 mol H2完全燃烧生成液态水,放出的热量为
(3)碳的燃烧热△H=
(4)在25℃、101kPa下, 1g甲烷完全燃烧生成CO2和液态H2O,放出55 kJ的热量,写出表示甲烷燃烧热的热化学方程式
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】已知:
2H2(g) + O2(g) =2H2O( l) ΔH= -571.6 kJ·mol-1
CO(g) + O2(g) = CO2(g) △H= -283 kJ·mol-1
O2(g) = CO2(g) △H= -283 kJ·mol-1
某H2和CO的混合气体完全燃烧时放出113.76 kJ热量,同时生成3.6 g液态水,求原混合气体中
H2和CO的物质的量_______ 。
2H2(g) + O2(g) =2H2O( l) ΔH= -571.6 kJ·mol-1
CO(g) +
 O2(g) = CO2(g) △H= -283 kJ·mol-1
O2(g) = CO2(g) △H= -283 kJ·mol-1某H2和CO的混合气体完全燃烧时放出113.76 kJ热量,同时生成3.6 g液态水,求原混合气体中
H2和CO的物质的量
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】根据下列叙述写出相应的热化学方程式:
(1)已知8 g固体硫完全燃烧时放出74.2 kJ的热量,该反应的热化学方程式是___________ 。
(2)在25℃、101 kPa下,已知SiH4气体在氧气中完全燃烧后恢复至原状态,平均每转移1 mol电子放出热量190.0 kJ,该反应的热化学方程式是___________ 。
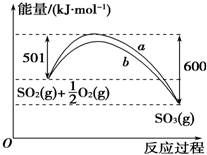
(3)下图a曲线是SO2生成SO3反应过程中能量变化的曲线图。该反应的热化学方程式为___________ 。___________ ,1 mol H2完全反应生成NH3所放出的热量为___________ 。
(5)已知:N2(g)+2O2(g)=2NO2(g) △H=+67.7 kJ·mol-1
N2H4(g)+O2(g)=N2(g)+2H2O(g) △H=-534 kJ·mol-1
则肼(N2H4)与NO2完全反应的热化学方程式为___________ 。
(1)已知8 g固体硫完全燃烧时放出74.2 kJ的热量,该反应的热化学方程式是
(2)在25℃、101 kPa下,已知SiH4气体在氧气中完全燃烧后恢复至原状态,平均每转移1 mol电子放出热量190.0 kJ,该反应的热化学方程式是
(3)下图a曲线是SO2生成SO3反应过程中能量变化的曲线图。该反应的热化学方程式为
(5)已知:N2(g)+2O2(g)=2NO2(g) △H=+67.7 kJ·mol-1
N2H4(g)+O2(g)=N2(g)+2H2O(g) △H=-534 kJ·mol-1
则肼(N2H4)与NO2完全反应的热化学方程式为
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】常见的氮氧化物有一氧化氮、二氧化氮、一氧化二氮(N2O)、五氧化二氮(N2O5)等。
(1)在一定条件下,氮气与氧气反应生成1 mol一氧化氮气体,吸收90 kJ的热。该反应的热化学方程式为:N2(g)+O2(g)=2NO(g) ΔH=___________ kJ·mol−1
(2)在2 L密闭容器内,800℃时反应2NO(g)+O2(g) 2NO2(g)体系中,n(NO)随时间变化如下表:
2NO2(g)体系中,n(NO)随时间变化如下表:
①用NO表示0~2s内该反应的平均速率v(NO)=___________ mol·L−1·s−1。
②下列措施能够使该反应速率加快的是___________ 。
a.降低温度 b.使用催化剂 c.减小压强
③若上述反应在恒容的密闭容器中进行,下列叙述中能说明该反应已达平衡状态的是___________ 。
a.混合气体的颜色保持不变
b.c(NO)∶c(O2)=2∶1
c.每消耗1 mol O2的同时生成2 mol NO2
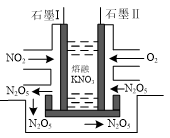
(3)NO2、O2和熔融KNO3可制作燃料电池,其原理如图所示。该电池在放电过程中石墨I电极上生成可循环使用的氧化物N2O5。
①放电时,该电池的负极是___________ (填“石墨Ⅰ”或“石墨Ⅱ”)。
②若电路中有1 mol电子转移,则理论上石墨Ⅱ处需消耗标准状况下的O2___________ L。
(1)在一定条件下,氮气与氧气反应生成1 mol一氧化氮气体,吸收90 kJ的热。该反应的热化学方程式为:N2(g)+O2(g)=2NO(g) ΔH=
(2)在2 L密闭容器内,800℃时反应2NO(g)+O2(g)
 2NO2(g)体系中,n(NO)随时间变化如下表:
2NO2(g)体系中,n(NO)随时间变化如下表:| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
②下列措施能够使该反应速率加快的是
a.降低温度 b.使用催化剂 c.减小压强
③若上述反应在恒容的密闭容器中进行,下列叙述中能说明该反应已达平衡状态的是
a.混合气体的颜色保持不变
b.c(NO)∶c(O2)=2∶1
c.每消耗1 mol O2的同时生成2 mol NO2
(3)NO2、O2和熔融KNO3可制作燃料电池,其原理如图所示。该电池在放电过程中石墨I电极上生成可循环使用的氧化物N2O5。
①放电时,该电池的负极是
②若电路中有1 mol电子转移,则理论上石墨Ⅱ处需消耗标准状况下的O2
您最近一年使用:0次



