下表是部分短周期元素的原子半径及主要化合价:
下列判断正确的是
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.112 | 0.101 | 0.066 |
| 主要化合价 | +2 | +3 | +2 | +6、 -2 | -2 |
| A.T的氢化物的沸点比R的氢化物的沸点低 |
| B.失电子能力:L<Q |
| C.L与R所对应的离子的核外电子排布相同 |
| D.M与T形成的化合物能与NaOH溶液反应 |
更新时间:2017-09-06 15:01:43
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】下图是部分短周期元素的原子序数与其某种常见化合价的关系图,若用原子序数代表所对应的元素,则下列说法正确的是
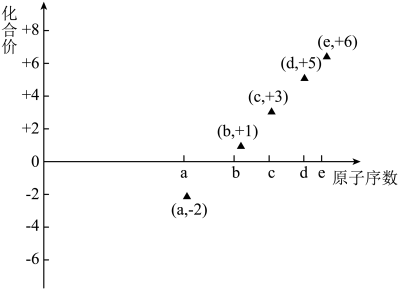

| A.31d和33d属于同种核素 |
| B.气态氢化物的稳定性:a>d>e |
| C.b、c的最高价氧化物对应水化物可以反应 |
| D.a和b形成的化合物不可能含共价键 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】下列说法正确的是
①HF、HCl、HBr、HI的热稳定性和还原性均依次减弱
②1H和2H是不同的核素,它们的质子数相等
③17O2和18O2互为同分异构体
④第三周期非金属含氧酸的酸性从左到右依次增强
⑤1.12L16O2和1.12L18O2均含0.1NA个氧原子
⑥元素周期律是元素原子核外电子排布周期性变化的结果
①HF、HCl、HBr、HI的热稳定性和还原性均依次减弱
②1H和2H是不同的核素,它们的质子数相等
③17O2和18O2互为同分异构体
④第三周期非金属含氧酸的酸性从左到右依次增强
⑤1.12L16O2和1.12L18O2均含0.1NA个氧原子
⑥元素周期律是元素原子核外电子排布周期性变化的结果
| A.②⑥ | B.②④ | C.①④ | D.③⑤ |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐3】短周期主族元素X、Y、Z、W的原子序数依次增大,K、L、M均是由这些元素组成的氧化物,甲、乙分别是元素Y、W的单质,甲是常见的固体,乙是常见的气体。K是红棕色气体,丙的浓溶液具有强氧化性,上述物质的转化关系如图所示。下列说法错误的是( )
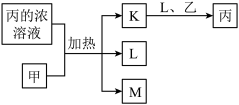

A.X、Y、Z三种元素的第一电离能: |
| B.X分别与Y、Z、W形成的分子中均可能含有非极性共价键 |
| C.Z元素的最高价含氧酸的酸性在同周期和同主族元素中均最强 |
D.若固体 是由直线形的 是由直线形的 和平面三角形的 和平面三角形的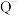 组成,则 组成,则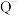 与丙溶液中的溶质阴离子相同 与丙溶液中的溶质阴离子相同 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】X、Y、Z、R为原子序数依次增大的短周期主族元素,其最外层电子数之和等于19。X与Y位于不同周期,Y和Z相邻,Z原子的最外层电子数是X原子内层电子总数的3倍。下列说法正确的是
| A.非金属性:Y>R | B.对应单质的熔点:X<R |
| C.最简单氢化物的稳定性:R>Z | D.与X同主族的元素都是金属元素 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】下列结论正确 的是( )
①粒子半径:K+>Al3+>S2->Cl-
②氢化物的酸性:HCl>HBr>HI
③离子的还原性:S2->Cl->Br->I-
④氧化性:Cl2>S>Se>Te
⑤酸性:H2SO4>H3PO4>H2CO3>HClO
⑥非金属性:O>N>P>Si
①粒子半径:K+>Al3+>S2->Cl-
②氢化物的酸性:HCl>HBr>HI
③离子的还原性:S2->Cl->Br->I-
④氧化性:Cl2>S>Se>Te
⑤酸性:H2SO4>H3PO4>H2CO3>HClO
⑥非金属性:O>N>P>Si
| A.①④⑤ | B.③⑥ | C.④⑤⑥ | D.②④⑤⑥ |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】短周期主族元素X、Y、Z、W原子序数依次增大,X原子的核外有7个电子,在周期表中Y位于ⅡA族,Y、Z原子的最外层电子数之和等于W原子的最外层电子数,W的氢化物热稳定性在同周期元素中最强。下列说法正确的是
| A.原子半径:r(X)<r(Y)<r(Z)<r(W) |
| B.元素Y、W的简单离子具有相同的电子层结构 |
| C.Z的最高价氧化物对应水化物的酸性比X的强 |
| D.由X与Y两种元素组成的简单化合物是离子化合物 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】短周期主族元素W、X、Y、Z的原子半径依次增大,且X、Y原子序数之和是W、Z原子序数之和的2 倍,m、n、p、r是由这些元素组成的元化合物,甲、乙是其中两种元素对应的单质,n 与乙均是淡黄色固体。上述物质的转化关系如图所示(部分反应物或生成物省略)。下列说法错误的是
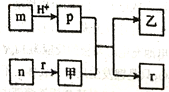

| A.热稳定性: p<r |
| B.X 与Y组成的化合物一定有漂白性 |
| C.含Y 元素的盐溶液可能显酸性、中性或碱性 |
| D.Z 与W、X、Y 可形成离子化合物 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐3】短周期元素W、X、Y、Z的原子序数依次增大,其中Z为金属且Z的原子序数为W的2倍。n、p、q是由这些元素组成的二元化合物,常温下n为气体。m、r、s分别是Z、W、X的单质,t的水溶液显碱性且焰色反应呈黄色,上述物质间的转化关系如图所示。下列说法正确的是
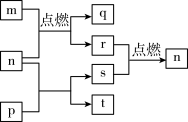

| A.离子半径:Z>X |
| B.2.4 gm在足量的n中充分燃烧,固体质量增加1.6 g |
| C.最简单气态氢化物的稳定性:W>X |
| D.n+p→s+t的过程中,有离子键、共价键的断裂,也有离子键、共价键的形成 |
您最近一年使用:0次



