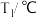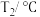某研究小组将V1 mL 0.50 mol/L H2SO4溶液和V2 mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验装置和实验结果如下图所示(实验中始终保持V1+V2=50 mL)。回答下列问题:
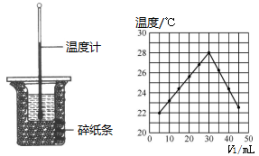
(1)如图所示实验装置中有一个明显的 错误________ 。
(2)为了减少实验误差,实验过程中将NaOH溶液_______ (选填“一次”或“分多次”)倒入盛有稀硫酸的小烧杯中。溶液混 合后,准确读取混合溶液的______ ,记为终止温度。
(3)研究小组做该实验时环境温度_____ 22 ℃(填“高于”、“低于”或“等于”),判断的依据是_____________ 。
(4)由题干及图形可知,V1︰V2=____________ 时,酸碱恰好完全中和,此反应所用NaOH溶液的浓度应为___________ mol/L。
(5)若通过实验测定及有关计算知此反应共放出a kJ的热量,请写出此反应的热化学方程式:_____________________________________________________________________

(1)如图所示实验装置中有一个明显的 错误
(2)为了减少实验误差,实验过程中将NaOH溶液
(3)研究小组做该实验时环境温度
(4)由题干及图形可知,V1︰V2=
(5)若通过实验测定及有关计算知此反应共放出a kJ的热量,请写出此反应的热化学方程式:
更新时间:2017-10-14 21:50:23
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】现有A、B、C、D、E、F六种短周期主族元素,它们的原子序数依次增大,D与E的氢化物分子构型都是V型。A、B的最外层电子数之和与C的最外层电子数相等,A分别与B、C、D形成电子总数相等的分子。
(1)C的元素符号是______ ;元素F在周期表中的位置_____________ 。
(2)B与D一般情况下可形成两种常见气态化合物,假若现在科学家制出另一种直线型气态化合物B2D2分子,且各原子最外层都满足8电子结构,则B2D2电子式为_________ ,其固体时的晶体类型是____________ 。
(3)最近意大利罗马大学的FuNvio Cacace等人获得了极具理论研究意义的C4气态分子。C4分子结构如图所示,已知断裂1molC—C吸收167kJ的热量,生成1mol C≡C放出942kJ热量。试写出由C4气态分子变成C2气态分子的热化学方程式:_____________________________________________ 。
(4)某盐x (C2A6F2)的性质与CA4F类似,是离子化合物,其水溶液因分步水解而呈弱酸性。
①盐x显酸性原因(用离子方程式表示)____________________________ 。
②写出足量金属镁加入盐x的溶液中产生H2的化学方程式_____________________________________________
(1)C的元素符号是
(2)B与D一般情况下可形成两种常见气态化合物,假若现在科学家制出另一种直线型气态化合物B2D2分子,且各原子最外层都满足8电子结构,则B2D2电子式为
(3)最近意大利罗马大学的FuNvio Cacace等人获得了极具理论研究意义的C4气态分子。C4分子结构如图所示,已知断裂1molC—C吸收167kJ的热量,生成1mol C≡C放出942kJ热量。试写出由C4气态分子变成C2气态分子的热化学方程式:

(4)某盐x (C2A6F2)的性质与CA4F类似,是离子化合物,其水溶液因分步水解而呈弱酸性。
①盐x显酸性原因(用离子方程式表示)
②写出足量金属镁加入盐x的溶液中产生H2的化学方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】分别取25 mL 0.50 mol/L硫酸与50 mL 0.55 mol/L NaOH溶液进行中和反应。某学习小组用简易量热计测得有关数据如下表:
(1)反应前酸和碱稀溶液的密度近似为1.0g/cm3,反应后溶液的比热容近似为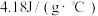 ,实验中反应释放的热量为
,实验中反应释放的热量为___________ J。
(2)根据测量结果,写出生成 对应的热化学反应方程式
对应的热化学反应方程式___________ 。
| 实验序号 | 起始温度t1/℃ | 终止温度t2/℃ | |
| 硫酸 | 氢氧化钠 | 混合溶液 | |
| 1 | 20.0 | 20.2 | 24.0 |
| 2 | 20.2 | 20.4 | 24.4 |
| 3 | 20.5 | 20.6 | 26.0 |
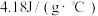 ,实验中反应释放的热量为
,实验中反应释放的热量为(2)根据测量结果,写出生成
 对应的热化学反应方程式
对应的热化学反应方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】砷(As)是第VA族元素,它在自然界中的含量不高,但人类认识它的历史很长,砷的某些化合物具有独特的性质与用途,如 在医药、电子等领域有重要应用,我国科学家研究发现砒霜(
在医药、电子等领域有重要应用,我国科学家研究发现砒霜( )可用来治疗早期幼粒白血病。
)可用来治疗早期幼粒白血病。
(1) 中砷的化合价为
中砷的化合价为___________ ,从物质化学性质角度看, 不可能是
不可能是___________ (填“酸”“碱”或“两”)性氧化物。
(2)某化工厂利用含硫化砷(As2S3)的废料制取 (微溶于水)的流程如下。
(微溶于水)的流程如下。
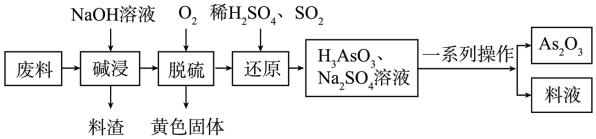
①写出两种能提高“碱浸”速率的方法:___________ 。
②碱浸液中溶质主要为 、
、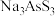 ,脱硫后以
,脱硫后以 的形式存在,写出
的形式存在,写出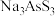 与
与 反应的化学方程式:
反应的化学方程式:___________ 。还原后砷以 形式存在,则通入
形式存在,则通入 的反应中,氧化剂与还原剂的物质的量之比为
的反应中,氧化剂与还原剂的物质的量之比为___________ 。
③还原后加热溶液, 分解为
分解为 ,结晶得到粗
,结晶得到粗 。
。 在不同温度和不同浓度硫酸中的溶解度度(S)曲线如下图所示。
在不同温度和不同浓度硫酸中的溶解度度(S)曲线如下图所示。
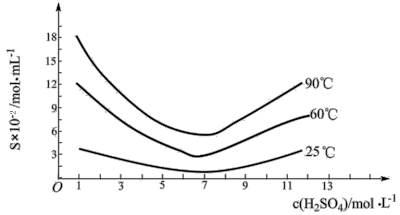
为了提高粗 的沉淀率,“结晶”过程进行的操作是蒸发浓缩,冷却结晶,过滤,洗涤,在此过程中应控制的条件为
的沉淀率,“结晶”过程进行的操作是蒸发浓缩,冷却结晶,过滤,洗涤,在此过程中应控制的条件为___________ 。
④在工业生产中,最后一步所得滤液可循环使用,其目的是___________ 。
(3)砷元素广泛存在于自然界,砷与其化合物被运用在农药、除草剂、杀虫剂等。砷的常见氧化物有 和
和 ,其中
,其中 热稳定性差。根据下图写出
热稳定性差。根据下图写出 分解为
分解为 的热化学方程式
的热化学方程式___________ 。

 在医药、电子等领域有重要应用,我国科学家研究发现砒霜(
在医药、电子等领域有重要应用,我国科学家研究发现砒霜( )可用来治疗早期幼粒白血病。
)可用来治疗早期幼粒白血病。(1)
 中砷的化合价为
中砷的化合价为 不可能是
不可能是(2)某化工厂利用含硫化砷(As2S3)的废料制取
 (微溶于水)的流程如下。
(微溶于水)的流程如下。
①写出两种能提高“碱浸”速率的方法:
②碱浸液中溶质主要为
 、
、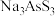 ,脱硫后以
,脱硫后以 的形式存在,写出
的形式存在,写出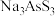 与
与 反应的化学方程式:
反应的化学方程式: 形式存在,则通入
形式存在,则通入 的反应中,氧化剂与还原剂的物质的量之比为
的反应中,氧化剂与还原剂的物质的量之比为③还原后加热溶液,
 分解为
分解为 ,结晶得到粗
,结晶得到粗 。
。 在不同温度和不同浓度硫酸中的溶解度度(S)曲线如下图所示。
在不同温度和不同浓度硫酸中的溶解度度(S)曲线如下图所示。
为了提高粗
 的沉淀率,“结晶”过程进行的操作是蒸发浓缩,冷却结晶,过滤,洗涤,在此过程中应控制的条件为
的沉淀率,“结晶”过程进行的操作是蒸发浓缩,冷却结晶,过滤,洗涤,在此过程中应控制的条件为④在工业生产中,最后一步所得滤液可循环使用,其目的是
(3)砷元素广泛存在于自然界,砷与其化合物被运用在农药、除草剂、杀虫剂等。砷的常见氧化物有
 和
和 ,其中
,其中 热稳定性差。根据下图写出
热稳定性差。根据下图写出 分解为
分解为 的热化学方程式
的热化学方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】某化学兴趣小组用0.50mol∙L-1硫酸溶液和0.50mol∙L-1NaOH溶液要进行中和反应反应热的测定。
(1)若实验中大约需要使用240mLNaOH溶液,至少需要称取NaOH固体_____ g。
(2)实验桌上备有大小两个烧杯、胶头滴管、玻璃搅拌器、0.50mol∙L-1硫酸溶液、0.50mol∙L-1氢氧化钠溶液,实验尚缺少的玻璃用品是_____ 。
(3)用50mLNaOH溶液和30mL硫酸溶液进行实验,实验数据如表所示。
①请填写表中的空白:_____ 。
已知: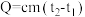 ,反应后溶液的比热容c为
,反应后溶液的比热容c为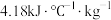 ,各物质的密度均为
,各物质的密度均为 。
。
②根据实验结果写出氢氧化钠溶液与盐酸反应的热化学方程式:_____ (取小数点后一位)。
(4)若用同浓度醋酸代替硫酸做实验,则所测焓变_____ (填“偏大”、“偏小”或“不变”)。
(5)上述实验所测中和热数值与-57.3kJ∙mol-1,产生偏差的原因可能是_____ 。
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
(1)若实验中大约需要使用240mLNaOH溶液,至少需要称取NaOH固体
(2)实验桌上备有大小两个烧杯、胶头滴管、玻璃搅拌器、0.50mol∙L-1硫酸溶液、0.50mol∙L-1氢氧化钠溶液,实验尚缺少的玻璃用品是
(3)用50mLNaOH溶液和30mL硫酸溶液进行实验,实验数据如表所示。
①请填写表中的空白:
| 温度 实验次数 | 起始温度t1/℃ | 终止温度t2/℃ | 温度差平均值(t2-t1)/℃ | ||
| H2SO4溶液 | NaOH溶液 | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 30.1 | _____ |
| 2 | 27.0 | 27.4 | 27.2 | 33.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 | |
| 4 | 26.4 | 26.2 | 26.3 | 30.4 | |
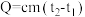 ,反应后溶液的比热容c为
,反应后溶液的比热容c为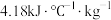 ,各物质的密度均为
,各物质的密度均为 。
。②根据实验结果写出氢氧化钠溶液与盐酸反应的热化学方程式:
(4)若用同浓度醋酸代替硫酸做实验,则所测焓变
(5)上述实验所测中和热数值与-57.3kJ∙mol-1,产生偏差的原因可能是
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】某小组学生用如图所示简易量热计进行中和反应反应热的测定。近似处理实验所用酸、碱溶液的密度为1.0 g∙cm-3、比热容为4.2J/(g∙℃),忽略量热计的比热容。
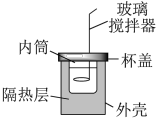
【药品】:50mL 0.50mol/L 盐酸、50mL 0.55mol/L NaOH溶液、50mL 0.55mol/L KOH溶液。
【实验数据】学生甲进行的三次实验数据如下表所示:
(1)从实验装置上看,还缺少的仪器名称是___________ 。
(2)学生甲实测数据处理
①∆t=___________ ℃。
②放出的热量Q甲___________ kJ(保留一位数)。
③Q甲kJ比该反应理论上放热为Q kJ略微偏小,其原因可能是___________ (写一条)。
(3)学生乙选用KOH溶液,其他均与学生甲同,且操作规范,预测实验放出热量的数值Q乙___________ Q甲(填“<”或“=”或“>”)。
(4)写出上面实验理论上生成1mol H2O时,中和反应的反应热的热化学方程式为(用含Q的代数式表示)___________ 。
(5)TiO2转化为TiCl4有直接氯化法和碳氯化法。1000 ℃时反应的热化学方程式及其平衡常数如下:
(i)直接氯化:TiO2(s)+2Cl2(g)=TiCl4(g)+O2(g) ΔH1=+172 kJ·mol-1,Kp1=1.0×10-2
(ii)碳氯化:TiO2(s)+2Cl2(g)+2C(s)=TiCl4(g)+2CO(g) ΔH2=-51 kJ·mol-1,Kp2=1.2×1012Pa
①反应2C(s)+O2(g)=2CO(g)的ΔH为___________ kJ·mol-1,Kp=___________ Pa。
②碳氯化的反应趋势远大于直接氯化,其原因是___________ 。
③数据显示在200 ℃平衡时TiO2几乎完全转化为TiCl4,但实际生产中反应温度却远高于此温度,其原因是___________ 。
④TiO2碳氯化是一个“气-固-固”反应,有利于TiO2-C“固-固”接触的措施是___________ 。

【药品】:50mL 0.50mol/L 盐酸、50mL 0.55mol/L NaOH溶液、50mL 0.55mol/L KOH溶液。
【实验数据】学生甲进行的三次实验数据如下表所示:
| 实验次数 | 反应前体系的温度/℃ | 反应后体系温度/℃ | 温度差平均值/℃ | ||
| 50mL 0.50mol/L盐酸 | 50mL 0.55mol/L NaOH溶液 | 平均值 | |||
| 1 | 24.9 | 25.1 | 28.4 | ∆t | |
| 2 | 25.1 | 25.0 | 26.3 | ||
| 3 | 25.0 | 25.0 | 28.4 | ||
(1)从实验装置上看,还缺少的仪器名称是
(2)学生甲实测数据处理
①∆t=
②放出的热量Q甲
③Q甲kJ比该反应理论上放热为Q kJ略微偏小,其原因可能是
(3)学生乙选用KOH溶液,其他均与学生甲同,且操作规范,预测实验放出热量的数值Q乙
(4)写出上面实验理论上生成1mol H2O时,中和反应的反应热的热化学方程式为(用含Q的代数式表示)
(5)TiO2转化为TiCl4有直接氯化法和碳氯化法。1000 ℃时反应的热化学方程式及其平衡常数如下:
(i)直接氯化:TiO2(s)+2Cl2(g)=TiCl4(g)+O2(g) ΔH1=+172 kJ·mol-1,Kp1=1.0×10-2
(ii)碳氯化:TiO2(s)+2Cl2(g)+2C(s)=TiCl4(g)+2CO(g) ΔH2=-51 kJ·mol-1,Kp2=1.2×1012Pa
①反应2C(s)+O2(g)=2CO(g)的ΔH为
②碳氯化的反应趋势远大于直接氯化,其原因是
③数据显示在200 ℃平衡时TiO2几乎完全转化为TiCl4,但实际生产中反应温度却远高于此温度,其原因是
④TiO2碳氯化是一个“气-固-固”反应,有利于TiO2-C“固-固”接触的措施是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】50mL0.50mol·L-1盐酸与50mL0.55mol·L-1 NaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
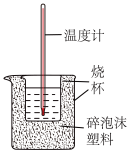
(1)图中尚缺少一种玻璃仪器是_______ 。
(2)烧杯间填满碎泡沫塑料的作用是_______ 。
(3)大烧杯上如不盖硬纸板,求得的中和热ΔH_______ (填“偏大”或“偏小”或“无影响”)。
(4)实验中改用60mL 0.50mol·L-1盐酸跟50mL 0.55mol·L-1 NaOH溶液进行反应,与上述实验相比,所放出的热量_______ (填“相等”或“不相等”),所求中和热_______ (填“相等”或“不相等”),简述理由:_______ 。
(5)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热数值会_______ ;用50mL 0.50mol·L-1 NaOH溶液进行上述实验,测得的中和热数值会_______ 。(填“偏大”、“偏小”或“无影响”)

(1)图中尚缺少一种玻璃仪器是
(2)烧杯间填满碎泡沫塑料的作用是
(3)大烧杯上如不盖硬纸板,求得的中和热ΔH
(4)实验中改用60mL 0.50mol·L-1盐酸跟50mL 0.55mol·L-1 NaOH溶液进行反应,与上述实验相比,所放出的热量
(5)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热数值会
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】通过测定反应过程中所放出的热量可计算中和热。50mL 0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在图示的装置中进行中和反应。回答下列问题:
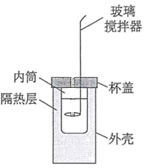
(1)从实验装置上看,图中尚缺少的一种玻璃仪器是___________ 。
(2)如果改用铜质搅拌器,求得的中和热ΔH___________ (填“偏 大”,“偏小”或“无影响”,下同);若将NaOH溶液分多次加入到盐酸中求得的中和热ΔH ___________ 。
(3)实验中改用60mL 0.50mol/L盐酸跟50mL 0.55mol/LNaOH溶液进行反应,与上述实验相比,所求中和热___________ (填“相等”“不相等”),简述理由:___________ 。
(4)若两溶液的密度都是1g/mL,中和后所得溶液的比热容c=4.18J/(g·℃),三次平行操作测得终止温度与起始温度差(t2-t1)分别为:①3.2℃②2.2℃③3.0℃,写出表示盐酸与NaOH溶液反应的中和热的热化学方程式___________ 。(小数点后保留一位小数)

(1)从实验装置上看,图中尚缺少的一种玻璃仪器是
(2)如果改用铜质搅拌器,求得的中和热ΔH
(3)实验中改用60mL 0.50mol/L盐酸跟50mL 0.55mol/LNaOH溶液进行反应,与上述实验相比,所求中和热
(4)若两溶液的密度都是1g/mL,中和后所得溶液的比热容c=4.18J/(g·℃),三次平行操作测得终止温度与起始温度差(t2-t1)分别为:①3.2℃②2.2℃③3.0℃,写出表示盐酸与NaOH溶液反应的中和热的热化学方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】如图是某实验小组改进的中和反应反应热测定实验装置。在塑料瓶中事先加入 盐酸,然后通过注射器注入
盐酸,然后通过注射器注入 溶液,通过测定反应过程中所放出的热量可计算反应热。回答下列问题:
溶液,通过测定反应过程中所放出的热量可计算反应热。回答下列问题:
(1)塑料瓶外泡沫板的作用是_____ 。
(2)实验小组按课本装置和改进后的装置分别进行实验,测得实验数据如下:
根据改进后装置的实验数据计算中和热
_____ (计算结果保留两位小数,近似认为盐酸和 溶液的密度都是
溶液的密度都是 ,中和后溶液的比热容
,中和后溶液的比热容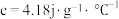 )。
)。
(3)如果用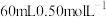 盐酸与
盐酸与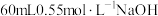 溶液进行反应,与上述实验相比,所放出的热量
溶液进行反应,与上述实验相比,所放出的热量_____ (填“相等”或“不相等”)。
 盐酸,然后通过注射器注入
盐酸,然后通过注射器注入 溶液,通过测定反应过程中所放出的热量可计算反应热。回答下列问题:
溶液,通过测定反应过程中所放出的热量可计算反应热。回答下列问题:(1)塑料瓶外泡沫板的作用是
(2)实验小组按课本装置和改进后的装置分别进行实验,测得实验数据如下:
实验次数 | 起始温度 | 终止温度 | 温度差 | |||||||
|
| 平均值 | 改进前 | 改进后 | 改进前 | 改进后 | ||||
| 改进前 | 改进后 | 改进前 | 改进后 | 改进前 | 改进后 | |||||
| 1 | 19.1 | 19.0 | 21.1 | 21.2 | 20.1 | 20.2 | 23.4 | 23.6 | 3.3 | 3.4 |
| 2 | 19.0 | 19.2 | 21.0 | 20.8 | 20.0 | 20.0 | 23.2 | 23.5 | 3.2 | 3.5 |
| 3 | 19.2 | 19.2 | 21.2 | 21.0 | 20.2 | 21.0 | 23.6 | 23.4 | 3.4 | 3.3 |

 溶液的密度都是
溶液的密度都是 ,中和后溶液的比热容
,中和后溶液的比热容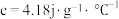 )。
)。(3)如果用
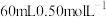 盐酸与
盐酸与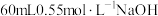 溶液进行反应,与上述实验相比,所放出的热量
溶液进行反应,与上述实验相比,所放出的热量
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】回答下列问题:
(1)用50mL0.50mol•L-1的盐酸与50mL0.55mol•L-1的NaOH溶液在如图1所示的装置中进行中和反应,通过测定反应过程中放出的热量可计算中和反应反应热。回答下列问题:
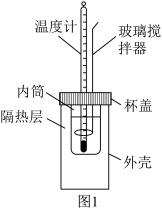
①若将杯盖改为薄铁板,求得的反应热将____ (填“偏大”“偏小”或“不变”)。
②若通过测定计算出产生的热量为1.42kJ,请写出该反应的热化学方程式:____ 。
(2)在温度t℃时,某溶液中c(H+)=10-amol•L-1,c(OH-)=10-bmol•L-1,已知a+b=12,则t____ 25℃(填“大于”“小于”或“等于”)。
(3)常温下,向某Ba(OH)2溶液中逐滴加入pH=x的盐酸,测得混合溶液的部分pH如表所示:
x=____ 。Ba(OH)2溶液的物质的量浓度为____ 。
(4)常温下,向100mLpH=2的硫酸与硫酸钠的混合溶液中,加入300mL上述Ba(OH)2溶液,沉淀正好达最大量,此时溶液的pH____ 7(填“大于”“小于”或“等于”);原混合溶液中硫酸钠的物质的量浓度为____ 。
(1)用50mL0.50mol•L-1的盐酸与50mL0.55mol•L-1的NaOH溶液在如图1所示的装置中进行中和反应,通过测定反应过程中放出的热量可计算中和反应反应热。回答下列问题:

①若将杯盖改为薄铁板,求得的反应热将
②若通过测定计算出产生的热量为1.42kJ,请写出该反应的热化学方程式:
(2)在温度t℃时,某溶液中c(H+)=10-amol•L-1,c(OH-)=10-bmol•L-1,已知a+b=12,则t
(3)常温下,向某Ba(OH)2溶液中逐滴加入pH=x的盐酸,测得混合溶液的部分pH如表所示:
| 序号 | 氢氧化钡溶液的体积/mL | 盐酸的体积/mL | 溶液的pH |
| ① | 22.00 | 0.00 | 12 |
| ② | 22.00 | 18.00 | 11 |
| ③ | 22.00 | 22.00 | 7 |
x=
(4)常温下,向100mLpH=2的硫酸与硫酸钠的混合溶液中,加入300mL上述Ba(OH)2溶液,沉淀正好达最大量,此时溶液的pH
您最近一年使用:0次