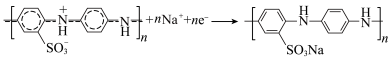某同学做如下实验:
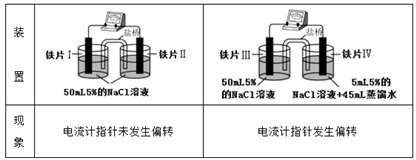
已知K3[Fe(CN)6]遇Fe2+生成深蓝色沉淀,则下列说法正确的是

已知K3[Fe(CN)6]遇Fe2+生成深蓝色沉淀,则下列说法正确的是
| A.“电流计指针未发生偏转”,说明铁片I、铁片II均未被腐蚀 |
| B.用K3[Fe(CN)6]溶液检验铁片III、IV附近溶液,可判断电池的正、负极 |
| C.铁片I、III所处的电解质溶液浓度相同,二者的腐蚀速率相等 |
| D.铁片IV的电极反应式为Fe-3e-=Fe3+ |
更新时间:2016-04-27 19:24:41
|
【知识点】 原电池
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】以N2和H2为反应物、溶有A的稀盐酸为电解质溶液,可制成能固氮的新型燃料电池,原理如图所示。下列说法不正确的是


| A.b电极为负极,发生氧化反应 |
B.a电极发生的反应为N2+8H++6e﹣=2NH |
| C.A溶液中所含溶质为NH4Cl |
| D.当反应消耗1molN2时,则消耗的H2为67.2L |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】某全固态薄膜锂离子电池截面结构如图3,电极A为非晶硅薄膜,充电时Li+得电子成为Li嵌入该薄膜材料,同时电极B中 失电子转化为
失电子转化为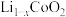 ,集流体起导电作用。下列说法
,集流体起导电作用。下列说法不 正确的是

 失电子转化为
失电子转化为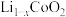 ,集流体起导电作用。下列说法
,集流体起导电作用。下列说法
| A.充电时,集流体A与外接电源的负极相连 |
B.放电时,电极B为正极,反应可表示为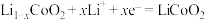 |
| C.放电时,外电路通过a mol电子,内电路中有a mol Li+通过LiPON薄膜电解质从正极迁移到负极 |
D.导电介质不可能为 溶液 溶液 |
您最近一年使用:0次

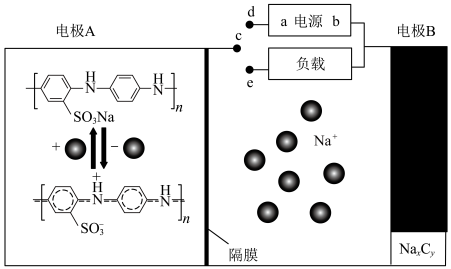
 连接
连接 时,
时, 透过隔膜进入电极
透过隔膜进入电极 室
室 极的电势比
极的电势比 极低
极低 时,每转移
时,每转移 ,两电极质量变化相差
,两电极质量变化相差