下图是一个电化学过程的示意图:

请回答下列问题:
(1)图中甲池是__________ (填“原电池”、“原解池”、“原镀池”),乙池中A电极的名称是__________ (填“正极”、“负极”、“阴极”或“阳极”)
(2)写出甲池中甲醇发生反应的电极反应式:______________________________________________
(3)当乙池中B极质量增加10.8克,理论上甲池中消耗O2的体积为:_______ L(标准状况),此时丙池中D极析出3.2g某金属,则丙池中的某盐溶液可能是__________ (填字母,下同)
a.MgSO4溶液 b.CuSO4溶液 c.NaCl溶液 d.AgNO3溶液
(4)若丙中电极不变,将其溶液换成NaCl溶液,一段时间后,丙中溶液的pH将_________ (填“增大”、“减小”或“不变”);甲中溶液的pH将_________ (填“增大”、“减小”或“不变”)。

请回答下列问题:
(1)图中甲池是
(2)写出甲池中甲醇发生反应的电极反应式:
(3)当乙池中B极质量增加10.8克,理论上甲池中消耗O2的体积为:
a.MgSO4溶液 b.CuSO4溶液 c.NaCl溶液 d.AgNO3溶液
(4)若丙中电极不变,将其溶液换成NaCl溶液,一段时间后,丙中溶液的pH将
更新时间:2017-11-07 11:14:16
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】探究铁比铬活泼时,可以将二者组成原电池(装置如图所示),在 电极上发生的反应为
电极上发生的反应为_______ ,溶液变为_______ 色;电子经过导线转移至 电极上,溶液中的
电极上,溶液中的 在
在 电极上获得电子,发生的还原反应为
电极上获得电子,发生的还原反应为_______ ,在 电极上有许多
电极上有许多_______ 产生。故能证明铁比铬活泼的实验现象是_______ 。

 电极上发生的反应为
电极上发生的反应为 电极上,溶液中的
电极上,溶液中的 在
在 电极上获得电子,发生的还原反应为
电极上获得电子,发生的还原反应为 电极上有许多
电极上有许多
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】金属铬和氢气在工业上都有重要的用途。
已知:铬能与稀硫酸反应,生成氢气和硫酸亚铬(CrSO4)。

(1)铜和铬构成的原电池装置如图1所示,其中盛有稀硫酸的烧杯中出现的现象为_______ 。盐桥中装的是琼脂-饱和KCl溶液,下列关于该原电池的说法正确的是_____ (填序号)。
A.盐桥的作用是使整个装置构成通路并保持溶液呈电中性,凡是有盐桥的原电池,盐桥中均可以盛装琼脂-饱和KCl溶液
B.理论上1 mol Cr溶解,盐桥中将有2 mol Cl-进入左烧杯中,2 mol K+进入右烧杯中
C.在原电池反应中H+得电子发生氧化反应
D.电子从铬极通过导线到铜极,又通过盐桥转移到左烧杯中
(2)铜和铬构成的另一原电池装置如图2所示,铜电极上不再有图1装置中铜电极上出现的现象,铬电极上产生大量气泡,且气体遇空气呈红棕色。写出该原电池正极的电极反应式:_____________________________________ 。
已知:铬能与稀硫酸反应,生成氢气和硫酸亚铬(CrSO4)。

(1)铜和铬构成的原电池装置如图1所示,其中盛有稀硫酸的烧杯中出现的现象为
A.盐桥的作用是使整个装置构成通路并保持溶液呈电中性,凡是有盐桥的原电池,盐桥中均可以盛装琼脂-饱和KCl溶液
B.理论上1 mol Cr溶解,盐桥中将有2 mol Cl-进入左烧杯中,2 mol K+进入右烧杯中
C.在原电池反应中H+得电子发生氧化反应
D.电子从铬极通过导线到铜极,又通过盐桥转移到左烧杯中
(2)铜和铬构成的另一原电池装置如图2所示,铜电极上不再有图1装置中铜电极上出现的现象,铬电极上产生大量气泡,且气体遇空气呈红棕色。写出该原电池正极的电极反应式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
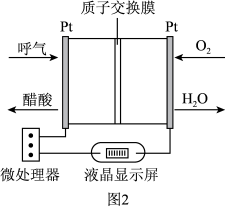
【推荐1】利用反应6NO2+8NH3=7N2+12H2O构成电池的方法,即能实现有效消除氮氧化物的排放,减轻环境污染,又能充分利用化学能,装置如图1所示,回答问题:

(1)电流从_______ (填“左”或“右”)侧电极经过负载后流向另一电极;电极A发生_______ 反应(填“氧化”或“还原”)。
(2)为使电池持续放电,离子交换膜需选用_______ (填“阴”或“阳”)离子交换膜。
(3)A电极上的电极反应式为:_______ 。
(4)当有4.48 L NO2(标准状况)被处理时,转移电子的物质的量为_______ 。
(5)负载可以测定电流大小,从而确定气体含量,酒驾测定工作原理与其相似。仔细阅读图2,写出酒驾测定中电池的总反应式:_______ 。

(1)电流从
(2)为使电池持续放电,离子交换膜需选用
(3)A电极上的电极反应式为:
(4)当有4.48 L NO2(标准状况)被处理时,转移电子的物质的量为
(5)负载可以测定电流大小,从而确定气体含量,酒驾测定工作原理与其相似。仔细阅读图2,写出酒驾测定中电池的总反应式:

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】电化学技术是有效解决CO、SO2、NOx等大气污染的重要方法。
I。某兴趣小组以SO2为原料,采用电化学方法制取硫酸,装置如下:

(1)电解质溶液中H+离子向___________ (填“A极”或“B极”)移动。
(2)请写出负极电极反应式___________ 。
(3)用该原电池做电源,石墨做电极电解2LAgNO3和KNO3混合溶液,通电一段时间,两极均产生4.48L(标准状况)气体,假设电解前后溶液体积不变,则电解后溶液中H+的浓度为___________ ,析出银的物质的量___________ 。
II。该兴趣小组又以NO为原料,采用电化学方法制取NH4NO3溶液,装置如下:

(4)阳极与阴极消耗NO物质的量之比为___________ ,物质A可为___________ 。
I。某兴趣小组以SO2为原料,采用电化学方法制取硫酸,装置如下:

(1)电解质溶液中H+离子向
(2)请写出负极电极反应式
(3)用该原电池做电源,石墨做电极电解2LAgNO3和KNO3混合溶液,通电一段时间,两极均产生4.48L(标准状况)气体,假设电解前后溶液体积不变,则电解后溶液中H+的浓度为
II。该兴趣小组又以NO为原料,采用电化学方法制取NH4NO3溶液,装置如下:

(4)阳极与阴极消耗NO物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】电化学手段对于研究物质性质以及工业生产中都有重要价值。
I.某实验小组利用原电池装置对FeCl3与Na2SO3的反应进行探究。
(1)取少量FeCl3溶液电极附近的混合液,加入铁氰化钾溶液,产生蓝色沉淀,证明FeCl3转化成_______ (化学式)。
(2)检验另一电极产物的实验操作及现象是_____ 。
(3)负极的电极反应式为_____ 。
II.工业上用Na2SO4溶液吸收工业烟气中的低浓度SO2形成吸收液后,再采用阳离子膜电解法,控制电压,电解吸收液可制成产品S和O2。工作原理示意图如图:

阴极区和阳极区的pH随时间的变化关系如图:

(4)阳极反应的电极反应物是______ 。结合电极反应式,说明阴极区pH升高的原因_______ 。(写出一条即可)
I.某实验小组利用原电池装置对FeCl3与Na2SO3的反应进行探究。
| 装置 | 实验现象 |
 1mol/LFeCl3溶液(pH≈1) 1mol/LNa2SO3溶液(pH≈9) | 灵敏电流计指针发生偏转 |
(2)检验另一电极产物的实验操作及现象是
(3)负极的电极反应式为
II.工业上用Na2SO4溶液吸收工业烟气中的低浓度SO2形成吸收液后,再采用阳离子膜电解法,控制电压,电解吸收液可制成产品S和O2。工作原理示意图如图:

阴极区和阳极区的pH随时间的变化关系如图:

(4)阳极反应的电极反应物是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】现有一套电化学装置,如下图所示,E 为沾有 Na2SO4溶液的滤纸,并加入几滴酚酞。A、B分别为Pt片,压在滤纸两端,R、S为电源的电极。M、N是用多微孔的 Ni 制成的电极材料,它在碱性溶液中可以视为惰性电极。G为电流计,K为开关。C、D和电解池中都充满浓KOH溶液。若在滤纸中央点上一滴紫色的 KMnO4溶液,断开K,接通外电源一段时间后,C、D中有气体产生。
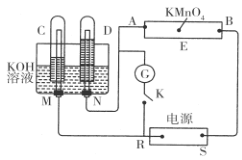
(1)S为________ (填“正”或“负”)极。
(2)A极附近溶液的现象是______________ , B 极附近发生的电极反应式为___________ 。
(3)滤纸上的紫色点向______ (填“A”或“B”)方移动。
(4)当 C、D里的气体产生到一定量时,切断外电源并接通开关K,经过一段时间,C、D中气体逐渐减少,D中的电极为________ (填“正”或“负”)极,电极反应式为___________________________ 。

(1)S为
(2)A极附近溶液的现象是
(3)滤纸上的紫色点向
(4)当 C、D里的气体产生到一定量时,切断外电源并接通开关K,经过一段时间,C、D中气体逐渐减少,D中的电极为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】电解装置如图所示:
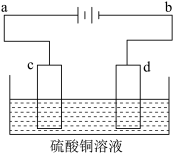
(1)当用惰性电极电解时,c为____________ 极,电极反应________ d为____________ 极,电极反应______________ ,电解总反应的化学方程____________________
(2)①若用此装置进行铁上镀铜则c为__________ (填铁或铜)d为___________ (填铁或铜)电解液浓度_____________ (增大,减小或不变)
②电镀一段时间后对电极进行称量发现两极质量差为16克,则电路中转移的电子___________ mol.
(3)若用此装置进行粗铜的电解精炼。则要求粗铜板是图中电极________ (填图中的字母);若粗铜中还含有Au、Ag、Fe,则Fe以_______ (填离子符号)形式进入溶液,c电极发生的反应______________ ,________________ 。

(1)当用惰性电极电解时,c为
(2)①若用此装置进行铁上镀铜则c为
②电镀一段时间后对电极进行称量发现两极质量差为16克,则电路中转移的电子
(3)若用此装置进行粗铜的电解精炼。则要求粗铜板是图中电极
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】电解原理在化学工业中有广泛应用。如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。
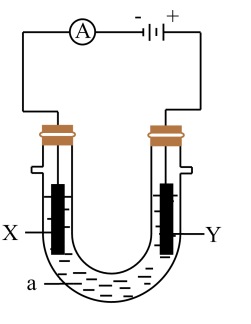
请回答以下问题:
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则:Y电极上的电极反应式为_______ ,检验该电极反应产物的方法是_______ 。
(2)如要用电解方法精炼粗铜,则:X电极的材料是_______ ,电极反应式是_______ 。电解液a可以选用_______ 。

请回答以下问题:
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则:Y电极上的电极反应式为
(2)如要用电解方法精炼粗铜,则:X电极的材料是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】目前流通的第五套人民币硬币材料分别为:1元硬币为铜芯镀镍合金,5角硬币为铜芯镀铜合金,1角硬币为硬铝合金。请回答:(题目中的百分含量均为质量分数)
(1)钢是含碳量为0.03%~2%的______ (填物质类别名称)。
(2)下图所示的装置中,甲、乙、丙三个烧杯分别盛放足量的溶液,电极及溶液如下表所示:

通电后电极a上可产生能使湿润的碘化钾淀粉试纸变蓝的气体。
①上述装置中M极为直流电源的______ 极(填“正”或“负”),电极b上发生的电极反应式为______ 。
②若在钢币上镀铜,应选择______ 烧杯(填“乙”或“丙”),当电极a上生成标准状况下气体2240 mL时,理论上可在电极______ (填字母)上镀铜______ g。
(3)工业上以铝土矿(主要成分Al2O3·nH2O,含少量的氧化铁和石英等杂质)为原料生产铝。为除去铝土矿样品中氧化铁和石英杂质,要将粉碎、筛选后的铝土矿样品溶解在足量的氢氧化钠溶液中处理,请写出有关反应的离子方程式______ 。
(4)已知硬铝中含Cu:2.2%~5%、Mg:0.2%~3%、Mn:0.3%~1.5%、Si:0.5%,其余是Al。1角硬币单枚质量为2.20克,若想制得1角硬币1百万枚,理论上至少需要含Al2O3 90%的铝土矿约______ 吨(小数点后保留一位数字)。
(1)钢是含碳量为0.03%~2%的
(2)下图所示的装置中,甲、乙、丙三个烧杯分别盛放足量的溶液,电极及溶液如下表所示:

| 电极 | a | b | c | d | e | f |
| 石墨 | 石墨 | 铜 | 钢 | 钢 | 铜 | |
| 溶液 | NaCl溶液 | CuSO4溶液 | CuSO4溶液 | |||
①上述装置中M极为直流电源的
②若在钢币上镀铜,应选择
(3)工业上以铝土矿(主要成分Al2O3·nH2O,含少量的氧化铁和石英等杂质)为原料生产铝。为除去铝土矿样品中氧化铁和石英杂质,要将粉碎、筛选后的铝土矿样品溶解在足量的氢氧化钠溶液中处理,请写出有关反应的离子方程式
(4)已知硬铝中含Cu:2.2%~5%、Mg:0.2%~3%、Mn:0.3%~1.5%、Si:0.5%,其余是Al。1角硬币单枚质量为2.20克,若想制得1角硬币1百万枚,理论上至少需要含Al2O3 90%的铝土矿约
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】铁是用途最广泛的金属材料之一,但生铁易生锈,请讨论电化学实验中有关铁的性质。
(1)某原电池装置如图所示,右侧烧杯中的电极反应为_________ ,左侧烧杯中的c(Cl-)________ (填“增大”“减小”或“不变”)。

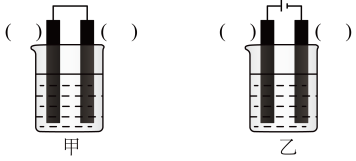
(2)已知下图甲、乙两池的总反应式均为Fe+H2SO4=FeSO4+H2↑,且在同侧电极(指均在“左电极”或“右电极”)产生H2。请在两池上标出电极材料(填“Fe”或“C”)。________
(3)用高铁酸盐设计的高铁电池是一种新型可充电电池,电解质溶液为KOH溶液,放电时的总反应式为3Zn+2K2FeO4+8H2O=3Zn(OH)2+2Fe(OH)3+4KOH。
①写出正极电极反应式________________ 。
②用高铁电池做电源,以铁为阳极,以铜作阴极,对足量KOH溶液进行电解,当电池中有0.2molK2FeO4反应时,则在电解池中生成H2________ L。(标准状况)
(1)某原电池装置如图所示,右侧烧杯中的电极反应为

(2)已知下图甲、乙两池的总反应式均为Fe+H2SO4=FeSO4+H2↑,且在同侧电极(指均在“左电极”或“右电极”)产生H2。请在两池上标出电极材料(填“Fe”或“C”)。

(3)用高铁酸盐设计的高铁电池是一种新型可充电电池,电解质溶液为KOH溶液,放电时的总反应式为3Zn+2K2FeO4+8H2O=3Zn(OH)2+2Fe(OH)3+4KOH。
①写出正极电极反应式
②用高铁电池做电源,以铁为阳极,以铜作阴极,对足量KOH溶液进行电解,当电池中有0.2molK2FeO4反应时,则在电解池中生成H2
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】如图所示三套实验装置,分别回答下列问题。

(1)装置1为铁的吸氧腐蚀实验。一段时间后,向插入铁钉的玻璃筒内滴入NaOH溶液,即可观察到铁钉附近的溶液有沉淀,表明铁被________ (填“氧化”或“还原”); 向插入石墨棒的玻璃筒内滴入酚酞溶液,可观察到石墨棒附近的溶液变红,该电极反应式为_______________________ 。
(2)装置2中的石墨是________ 极(填“正”或“负”),该电极反应式为_______________________________ 。
(3)装置3中甲烧杯盛放100 mL 0.2 mol·L-1的NaCl溶液,乙烧杯盛放100 mL0.5 mol·L-1的CuSO4溶液。反应一段时间后,停止通电。向甲烧杯中滴入几滴酚酞,观察到石墨电极附近首先变红。
①电源的M端为________ 极;甲烧杯中铁电极的电极反应式为_________________ 。
②乙烧杯中电解反应的离子方程式为_________________________________ 。
③停止电解,取出Cu电极,洗涤、干燥、称量,电极增重0.64 g,甲烧杯中产生的气体标准状况下的体积为________ mL。

(1)装置1为铁的吸氧腐蚀实验。一段时间后,向插入铁钉的玻璃筒内滴入NaOH溶液,即可观察到铁钉附近的溶液有沉淀,表明铁被
(2)装置2中的石墨是
(3)装置3中甲烧杯盛放100 mL 0.2 mol·L-1的NaCl溶液,乙烧杯盛放100 mL0.5 mol·L-1的CuSO4溶液。反应一段时间后,停止通电。向甲烧杯中滴入几滴酚酞,观察到石墨电极附近首先变红。
①电源的M端为
②乙烧杯中电解反应的离子方程式为
③停止电解,取出Cu电极,洗涤、干燥、称量,电极增重0.64 g,甲烧杯中产生的气体标准状况下的体积为
您最近一年使用:0次

 溶液,其充、放电按下式进行:
溶液,其充、放电按下式进行: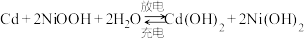 。
。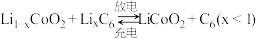 。则:
。则:

