现要配制0.01 mol·L-1的KMnO4溶液,下列操作导致所配溶液浓度偏高的是( )
| A.称量时,左盘高,右盘低 | B.定容时俯视容量瓶刻度线 |
| C.砝码破损 | D.摇匀后见液面下降,再加水至刻度线 |
17-18高一上·北京·阶段练习 查看更多[2]
更新时间:2017-11-09 19:16:46
|
【知识点】 配制一定物质的量浓度的溶液实验的误差分析解读
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】配制500 mL 0.100 mol·L-1的NaCl溶液,部分实验操作示意图如图。下列说法正确的是
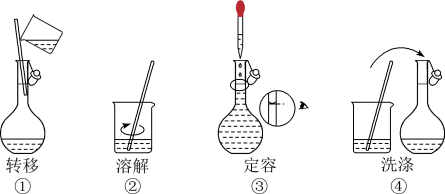

| A.定容时,仰视容量瓶的刻度线,使配得的NaCl溶液浓度偏低 |
| B.容量瓶需用自来水、蒸馏水洗涤,干燥后才可用 |
| C.实验中需用到的仪器有:托盘天平、250 mL容量瓶、烧杯、玻璃棒、胶头滴管等 |
| D.上述实验操作步骤的正确顺序为①②④③ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法不正确的是
| A.配制一定物质的量浓度溶液时,定容时俯视容量瓶的刻度线,会造成所配溶液的物质的量浓度偏高 |
| B.将质量分数为a%,物质的量浓度为c1mol/L的稀H2SO4溶液蒸发掉一定量的水,使之质量分数为2a%,此时物质的量浓度为c2mol/L,则c1和c2的数值关系是c2>2c1 |
C.将标准状况下的aLHCl气体溶于100mL水中,得到的盐酸溶液密度为bg/mL,则盐酸溶液的物质的量浓度为 mol/L mol/L |
D.VLFe2(SO4)3溶液中含Fe3+ag,则溶液中 的物质的量浓度为 的物质的量浓度为 mol/L mol/L |
您最近一年使用:0次



