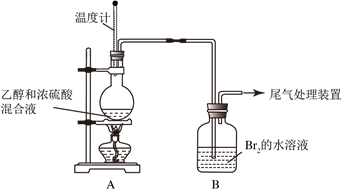
用乙醇与浓硫酸的混合液在加热的条件下可以发生消去反应,某实验小组的同学在实验室用如下图所示装置验证消去反应的产物。(气密性已检验,部分夹持装置略)。
实验操作和选项:
(1)烧瓶内发生的有机反应化学方程式是____________________________________ ,烧瓶内产生刺激性气味的气体的无机反应化学方程式是____________________________________ 。
(2)溶液“渐渐变黑”说明浓硫酸具有_________ 性。
(3)甲同学认为若 中溶液褪色,即可证明烧瓶中发生了消去反应,根据甲同学的观点,使
中溶液褪色,即可证明烧瓶中发生了消去反应,根据甲同学的观点,使 中溶液褪色反应的化学方程式是
中溶液褪色反应的化学方程式是____________________________________ 。
(4)乙同学却认为即使 中溶液褪色,也不能证明烧瓶中发生了消去反应。于是提出了两种改进方案①在
中溶液褪色,也不能证明烧瓶中发生了消去反应。于是提出了两种改进方案①在 、
、 间增加一个装有某种试剂的洗气瓶,该试剂为
间增加一个装有某种试剂的洗气瓶,该试剂为___________________________________ 。
②在 、
、 间增加一个盛有浓硫酸的洗气瓶,并将
间增加一个盛有浓硫酸的洗气瓶,并将 中的
中的 的水溶液改为
的水溶液改为 的
的 溶液,即可排除干扰,据实验现象可证明烧瓶中发生了消去反应。
溶液,即可排除干扰,据实验现象可证明烧瓶中发生了消去反应。
则乙同学认为 中使
中使 的水溶液褪色,产生干扰的原因(用化学方程式解释)
的水溶液褪色,产生干扰的原因(用化学方程式解释)_________ ,由方案②可知___________ 不能使 的四氯化碳溶液褪色。
的四氯化碳溶液褪色。

实验操作和选项:
| 操作 | 现象 |
点燃酒精灯加热至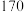 ℃ ℃ | Ⅰ: 中烧瓶内液体渐渐变黑 中烧瓶内液体渐渐变黑Ⅱ:  内气泡连续冒出,溶液逐渐褪色 内气泡连续冒出,溶液逐渐褪色 |
| …… | |
| 实验完毕,清洗烧瓶 | Ⅲ: 中烧瓶内附着少量黑色颗粒状物,有刺激性气味逸出 中烧瓶内附着少量黑色颗粒状物,有刺激性气味逸出 |
(2)溶液“渐渐变黑”说明浓硫酸具有
(3)甲同学认为若
 中溶液褪色,即可证明烧瓶中发生了消去反应,根据甲同学的观点,使
中溶液褪色,即可证明烧瓶中发生了消去反应,根据甲同学的观点,使 中溶液褪色反应的化学方程式是
中溶液褪色反应的化学方程式是(4)乙同学却认为即使
 中溶液褪色,也不能证明烧瓶中发生了消去反应。于是提出了两种改进方案①在
中溶液褪色,也不能证明烧瓶中发生了消去反应。于是提出了两种改进方案①在 、
、 间增加一个装有某种试剂的洗气瓶,该试剂为
间增加一个装有某种试剂的洗气瓶,该试剂为②在
 、
、 间增加一个盛有浓硫酸的洗气瓶,并将
间增加一个盛有浓硫酸的洗气瓶,并将 中的
中的 的水溶液改为
的水溶液改为 的
的 溶液,即可排除干扰,据实验现象可证明烧瓶中发生了消去反应。
溶液,即可排除干扰,据实验现象可证明烧瓶中发生了消去反应。则乙同学认为
 中使
中使 的水溶液褪色,产生干扰的原因(用化学方程式解释)
的水溶液褪色,产生干扰的原因(用化学方程式解释) 的四氯化碳溶液褪色。
的四氯化碳溶液褪色。
更新时间:2017-11-09 11:05:00
|
相似题推荐
解答题-有机推断题
|
适中
(0.65)
解题方法
【推荐1】B.《有机化学基础》
Ⅰ双酚A (也称BPA)常用来生产防碎塑料聚碳酸酯。BPA的结构简式如右下图所示。

(1)双酚A中的含氧官能团为___________ (填名称)。
(2)下列关于双酚A的叙述中,不正确的是____________ (填标号)。
a.遇FeCl3溶液变色
b.可以发生还原反应
c.1 mol双酚A最多可与2 mol Br2反应
d.可与NaOH溶液反应
(3)双酚A的一种合成路线如下图所示:
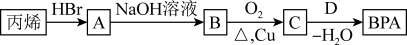
①丙烯→A的反应类型是______________ 。
②B→C的化学方程式是_______________ 。
Ⅱ甲苯和溴乙烷混合物可通过如下流程进行分离。

请填写下列空白:
(4)X的结构简式为___________ ;
(5)操作①能否用分液__________ ,理由是______________ 。
(6)写出甲苯与溴乙烷的混合物中加入试剂A时发生反应的化学方程式:_____________ 。
(7)如果Y为乙烯,则试剂B为_________ ,“一定条件”是指___________ 。
Ⅰ双酚A (也称BPA)常用来生产防碎塑料聚碳酸酯。BPA的结构简式如右下图所示。

(1)双酚A中的含氧官能团为
(2)下列关于双酚A的叙述中,不正确的是
a.遇FeCl3溶液变色
b.可以发生还原反应
c.1 mol双酚A最多可与2 mol Br2反应
d.可与NaOH溶液反应
(3)双酚A的一种合成路线如下图所示:

①丙烯→A的反应类型是
②B→C的化学方程式是
Ⅱ甲苯和溴乙烷混合物可通过如下流程进行分离。

请填写下列空白:
(4)X的结构简式为
(5)操作①能否用分液
(6)写出甲苯与溴乙烷的混合物中加入试剂A时发生反应的化学方程式:
(7)如果Y为乙烯,则试剂B为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】某化学兴趣小组用如下图1所示装置进行探究实验,以验证产物中有乙烯生成且乙烯具有不饱和性。当温度迅速上升后,可观察到试管中溴水褪色,烧瓶中浓H2SO4与乙醇的混合液体变为棕黑色。
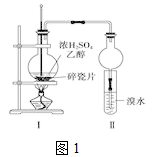

(1)写出该实验中生成乙烯的化学方程式_______________________ 。
(2)甲同学认为:考虑到该混合液体反应的复杂性,溴水褪色的现象不能证明反应中有乙烯生成且乙烯具有不饱和性,其理由正确的是___________________ 。
a.乙烯与溴水易发生取代反应
b.使溴水褪色的反应,未必是加成反应
c.使溴水褪色的物质,未必是乙烯
(3)乙同学经过细致观察后试管中另一实验现象后,证明反应中有乙烯生成,请简述这种这一实验现象___________________________ 。
(4)丙同学对上述实验装置进行了改进,在Ⅰ和Ⅱ之间增加上图2装置以除去乙醇蒸气和SO2,则A中的试剂是_____________ ,B中的试剂为__________________ 。


(1)写出该实验中生成乙烯的化学方程式
(2)甲同学认为:考虑到该混合液体反应的复杂性,溴水褪色的现象不能证明反应中有乙烯生成且乙烯具有不饱和性,其理由正确的是
a.乙烯与溴水易发生取代反应
b.使溴水褪色的反应,未必是加成反应
c.使溴水褪色的物质,未必是乙烯
(3)乙同学经过细致观察后试管中另一实验现象后,证明反应中有乙烯生成,请简述这种这一实验现象
(4)丙同学对上述实验装置进行了改进,在Ⅰ和Ⅱ之间增加上图2装置以除去乙醇蒸气和SO2,则A中的试剂是
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
真题
名校
【推荐3】乙醇是一种重要的化工原料,由乙醇为原料衍生出的部分化工产品如下图所示:
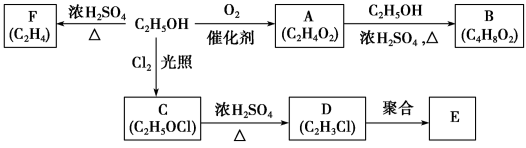
回答下列问题:
(1)A的结构简式为___________________ 。
(2)B的化学名称是____________________ 。
(3)由乙醇生产C的化学反应类型为____________________ 。
(4)E是一种常见的塑料,其化学名称是_________________________ 。
(5)由乙醇生成F的化学方程式为_______________________________ 。

回答下列问题:
(1)A的结构简式为
(2)B的化学名称是
(3)由乙醇生产C的化学反应类型为
(4)E是一种常见的塑料,其化学名称是
(5)由乙醇生成F的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】高铁酸钾(K2FeO4,极易溶于水,溶液呈紫红色)是一种绿色净水剂,易溶于水。某小组在实验室条件下制备K2FeO4并探究其性质。回答下列问题:
实验(一)制备K2FeO4。___________ ,装置B的作用是___________ ,盛装的试剂为 ___________ 。
(2)装置C中生成K2FeO4的化学方程式为___________
实验(二)探究K₂FeO4的性质。
(3)R溶液为______ (填“稀硫酸”或“盐酸”),写出装置a中的离子方程式:____________ ,不选择另一种酸的主要原因是____________ .
(4)设计一种方案检验从d口逸出的气体:______ 。
ll.探究K₂FeO4在酸性条件下的氧化性。
(5)向K₂FeO4溶液中滴加少量用稀硫酸酸化后的MnSO4溶液,溶液呈紫红色。______ (填“能”或“不能”)证明氧化性:  >MnSO4,原因是
>MnSO4,原因是____________ (用文字说明)。
实验(一)制备K2FeO4。

(2)装置C中生成K2FeO4的化学方程式为
实验(二)探究K₂FeO4的性质。
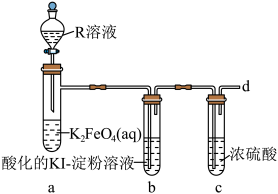
(3)R溶液为
(4)设计一种方案检验从d口逸出的气体:
ll.探究K₂FeO4在酸性条件下的氧化性。
(5)向K₂FeO4溶液中滴加少量用稀硫酸酸化后的MnSO4溶液,溶液呈紫红色。
 >MnSO4,原因是
>MnSO4,原因是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】Ⅰ.氨的制备
氨在化工生产领域有广泛应用,历史上曾有三位科学家在合成氨领域获得诺贝尔化学奖。

(1)实验室常用铵盐与强碱反应制取氨气,可选择装置___________ (填“A”或“B”),反应的化学方程式为___________ 。
(2)制备干燥的 时,发生、净化、收集和尾气处理装置的接口顺序为
时,发生、净化、收集和尾气处理装置的接口顺序为___________ (按气流方向填写小写字母)
(3)检验某溶液中存在 的操作及现象为
的操作及现象为___________ 。
(4)工业上在一定温度和催化剂条件下,可用 消除
消除 污染,生成两种对环境无害的物质,请写出
污染,生成两种对环境无害的物质,请写出 与
与 反应的化学方程式
反应的化学方程式___________ 。
Ⅱ.某实验小组研究 与溶液的反应,实验如下:
与溶液的反应,实验如下:
实验中所取镁粉质量均为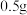 ,分别加入到选取的实验试剂中。
,分别加入到选取的实验试剂中。
资料:a. 溶液呈中性;b.Cl-对该反应几乎无影响。
溶液呈中性;b.Cl-对该反应几乎无影响。
(5)甲同学认为实验2比实验1反应剧烈的原因是 溶液中
溶液中 大,与Mg反应快。乙同学通过实验3证明甲同学的说法不合理。
大,与Mg反应快。乙同学通过实验3证明甲同学的说法不合理。
试剂X是___________ 。
(6)为进一步探究实验2反应剧烈的原因,进行实验4:
依据上述实验,可以得出Mg能与 反应生成
反应生成 ,乙同学认为该方案不严谨,需要补充的实验方案是
,乙同学认为该方案不严谨,需要补充的实验方案是___________ 。
实验总结:通过上述实验,该小组同学得出Mg能与 反应生成
反应生成 的结论。
的结论。
氨在化工生产领域有广泛应用,历史上曾有三位科学家在合成氨领域获得诺贝尔化学奖。

(1)实验室常用铵盐与强碱反应制取氨气,可选择装置
(2)制备干燥的
 时,发生、净化、收集和尾气处理装置的接口顺序为
时,发生、净化、收集和尾气处理装置的接口顺序为(3)检验某溶液中存在
 的操作及现象为
的操作及现象为(4)工业上在一定温度和催化剂条件下,可用
 消除
消除 污染,生成两种对环境无害的物质,请写出
污染,生成两种对环境无害的物质,请写出 与
与 反应的化学方程式
反应的化学方程式Ⅱ.某实验小组研究
 与溶液的反应,实验如下:
与溶液的反应,实验如下:实验中所取镁粉质量均为
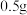 ,分别加入到选取的实验试剂中。
,分别加入到选取的实验试剂中。资料:a.
 溶液呈中性;b.Cl-对该反应几乎无影响。
溶液呈中性;b.Cl-对该反应几乎无影响。| 实验 | 实验试剂 | 实验现象 |
| 1 |  蒸馏水 蒸馏水 | 反应缓慢,有少量气泡产生(经检验为H2) |
| 2 | 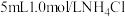 溶液 溶液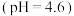 | 剧烈反应,产生刺激性气味气体和灰白色难溶固体 |
 溶液中
溶液中 大,与Mg反应快。乙同学通过实验3证明甲同学的说法不合理。
大,与Mg反应快。乙同学通过实验3证明甲同学的说法不合理。| 实验 | 实验装置 | 现象 |
| 3 | 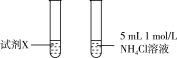 | 两试管反应剧烈程度相当 |
(6)为进一步探究实验2反应剧烈的原因,进行实验4:
| 实验 | 实验试剂 | 实验现象 |
| 4 | 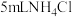 乙醇溶液 乙醇溶液 | 有无色无味气体产生(经检验为 ) ) |
 反应生成
反应生成 ,乙同学认为该方案不严谨,需要补充的实验方案是
,乙同学认为该方案不严谨,需要补充的实验方案是实验总结:通过上述实验,该小组同学得出Mg能与
 反应生成
反应生成 的结论。
的结论。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】某化学小组以铜为阳极、石墨为阴极,研究在不同的电解质溶液中铜被氧化的价态及产物。实验装置如图所示(电源装置略去)。

资料:i.Cu2O为砖红色,CuCl为白色,CuOH为黄色且易分解
ii.[Cu(NH3)2]+为无色,在空气中易被氧化为深蓝色[Cu(NH3)4]2+
iii.25 ℃时,Ksp(CuCl)=1.2×10-6,Ksp(CuOH)= 1.2×10-14
实验记录如下:
(1)I中铜电极的电极反应式是___________ 。
(2)II中沉淀由黄色变为砖红色的化学方程式是___________ 。
(3)将III中所得白色沉淀过滤,充分洗涤,进行下列实验,证实该沉淀为CuCl。

①证明III中所得白色沉淀中有Cu+的证据是___________ 。
②步骤iii的操作是___________ 。
(4)III中下端白色沉淀最终变为砖红色的原因是:白色沉淀为CuCl,___________ ,CuOH不稳定易分解为砖红色的Cu2O。
(5)IV中Cu未被氧化的原因是________ 。
(6)综上,铜被氧化的价态及产物与________ 有关。

资料:i.Cu2O为砖红色,CuCl为白色,CuOH为黄色且易分解
ii.[Cu(NH3)2]+为无色,在空气中易被氧化为深蓝色[Cu(NH3)4]2+
iii.25 ℃时,Ksp(CuCl)=1.2×10-6,Ksp(CuOH)= 1.2×10-14
实验记录如下:
| 实验 | 电解质溶液(3 mol/L) | 现象 | |
| 铜电极附近 | 石墨电极 | ||
| I | H2SO4 | 溶液变蓝 | 产生无色气泡,一段时间后有少量红色金属析出 |
| II | NaOH | 出现黄色浑浊,很快变为砖红色 | 产生无色气泡 |
| III | NaCl | 出现白色浑浊,浑浊向下扩散,一段时间后,下端白色沉淀变黄,最终为砖红色 | 产生无色气泡 |
| IV | KI | 迅速产生棕褐色的物质,滴入1 滴淀粉溶液, 立即变为蓝色;取出铜电极洗净检验,无变化 | 产生无色气泡 |
(2)II中沉淀由黄色变为砖红色的化学方程式是
(3)将III中所得白色沉淀过滤,充分洗涤,进行下列实验,证实该沉淀为CuCl。

①证明III中所得白色沉淀中有Cu+的证据是
②步骤iii的操作是
(4)III中下端白色沉淀最终变为砖红色的原因是:白色沉淀为CuCl,
(5)IV中Cu未被氧化的原因是
(6)综上,铜被氧化的价态及产物与
您最近一年使用:0次



