化学反应过程中,不仅有物质的变化,同时还伴随有能量的变化。
(1)已知几种化学键的键能如表所示:
则反应Cl2(g)+ 3F2(g) 2ClF3(g) 的△H=
2ClF3(g) 的△H=_____________ kJ·mol—1 。
(2)如图是乙烷、二甲醚燃烧过程中的能量变化图。
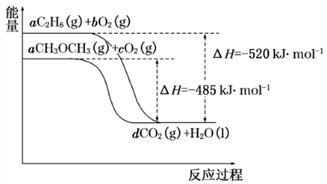
请回答下列问题:
①乙烷的燃烧热ΔH=____ kJ·mol-1。
②等物质的量的液态乙烷比气态乙烷完全燃烧生成稳定的氧化物时放出的热量__ (填“多”或“少”)。
③根据题图写出二甲醚完全燃烧时的热化学方程式_____________ 。
(3)实验室用50mL 0.50mol·L﹣1HCl与50mL 0.55mol·L﹣1NaOH溶液测定中和热。
①若改用60mL HCl进行实验,与原实验相比,所放出的热量____ (填“相等”或“不相等”,忽略实验本身误差,下同),所求中和热_____ (填“相等”或“不相等”,)。
②若用相同浓度和体积的氨水代替NaOH溶液进行上述实验,所求中和热数值会___ (填“偏大”“偏小”或“无影响”)。
(1)已知几种化学键的键能如表所示:
| 化学键 | Cl—Cl | F—F | Cl—F |
| 键能/ kJ·mol—1 | 242 | 159 | 172 |
则反应Cl2(g)+ 3F2(g)
 2ClF3(g) 的△H=
2ClF3(g) 的△H=(2)如图是乙烷、二甲醚燃烧过程中的能量变化图。

请回答下列问题:
①乙烷的燃烧热ΔH=
②等物质的量的液态乙烷比气态乙烷完全燃烧生成稳定的氧化物时放出的热量
③根据题图写出二甲醚完全燃烧时的热化学方程式
(3)实验室用50mL 0.50mol·L﹣1HCl与50mL 0.55mol·L﹣1NaOH溶液测定中和热。
①若改用60mL HCl进行实验,与原实验相比,所放出的热量
②若用相同浓度和体积的氨水代替NaOH溶液进行上述实验,所求中和热数值会
更新时间:2017-12-12 23:47:57
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】回答下列问题。
(1)室温下,NaY溶液的pH=8,c(Na+)-c(Y-)=___________ 。
(2)稀溶液中,1molH2SO4与NaOH完全反应时,放出114.6kJ热量,写出表示中和热的热化学方程式___________ 。
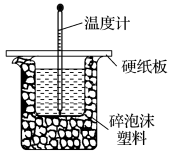
(3)实验室用50mL0.50mol·L-1的盐酸与50mL某浓度的NaOH溶液在如图所示装置中反应,通过测定反应过程中所放出的热量可计算中和热。如果用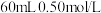 的盐酸与
的盐酸与 的溶液进行反应,与上述实验相比,所放出的热量
的溶液进行反应,与上述实验相比,所放出的热量___________ (填“相等、不相等”),所求中和热___________ (填“相等、不相等”)。该装置有明显的错误,其中一处是缺少一种玻璃仪器,该仪器的名称为___________ 。
(1)室温下,NaY溶液的pH=8,c(Na+)-c(Y-)=
(2)稀溶液中,1molH2SO4与NaOH完全反应时,放出114.6kJ热量,写出表示中和热的热化学方程式
(3)实验室用50mL0.50mol·L-1的盐酸与50mL某浓度的NaOH溶液在如图所示装置中反应,通过测定反应过程中所放出的热量可计算中和热。如果用
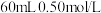 的盐酸与
的盐酸与 的溶液进行反应,与上述实验相比,所放出的热量
的溶液进行反应,与上述实验相比,所放出的热量
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】已知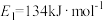 、
、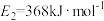 ,请参考题中图表,按要求填空:
,请参考题中图表,按要求填空:
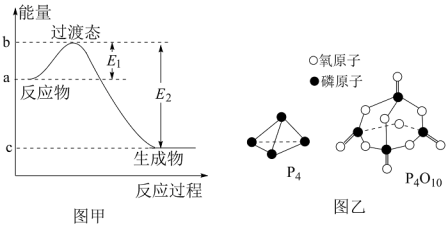
(1)图甲是1mol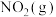 和1mol
和1mol 反应生成
反应生成 和
和 过程中的能量变化示意图。若在反应体系中加入催化剂,反应速率加快,
过程中的能量变化示意图。若在反应体系中加入催化剂,反应速率加快,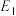 的变化是
的变化是___________ (填“增大”、“减小”或“不变”,下同), 的变化是
的变化是___________ , 和
和 反应的热化学方程式为
反应的热化学方程式为___________ 。
(2)已知25℃、101kPa下,1mol水蒸发为水蒸气需要吸热44.01kJ。
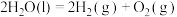
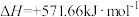

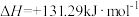
则反应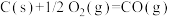 的反应热
的反应热 =
=___________ 。
(3)下表所示是部分化学键的键能参数:
已知白磷燃烧反应的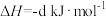 ,白磷及其完全燃烧生成的产物的结构如图乙所示。表中x=
,白磷及其完全燃烧生成的产物的结构如图乙所示。表中x=___________ 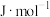 (用含a、b、c、d的代数式表示)。
(用含a、b、c、d的代数式表示)。
(4)某学生想通过测定中和反应过程中所放出的热量来计算中和反应的焓变。他将50mL0.5mol/L的盐酸与50mL0.55mol/L的 溶液在如图所示的装置中进行中和反应。
溶液在如图所示的装置中进行中和反应。
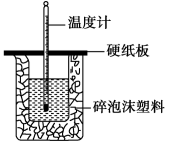
请回答下列问题:
①从实验装置上看,图中有多处错误,其中一处错误是缺少了一种玻璃仪器______ ;
②大烧杯上如不盖硬纸板,则求得的中和反应的 =
=_______ (填“偏大”、“偏小”、“无影响”);
③实验中改用20mL0.50mol/L的盐酸跟20mL0.55mol/L的 溶液进行反应,与上述实验相比,所放出的热量
溶液进行反应,与上述实验相比,所放出的热量___________ (填“相等”或“不相等”),所求中和反应的
___________ (填“相等”或“不相等”)。
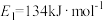 、
、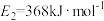 ,请参考题中图表,按要求填空:
,请参考题中图表,按要求填空:
(1)图甲是1mol
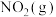 和1mol
和1mol 反应生成
反应生成 和
和 过程中的能量变化示意图。若在反应体系中加入催化剂,反应速率加快,
过程中的能量变化示意图。若在反应体系中加入催化剂,反应速率加快,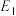 的变化是
的变化是 的变化是
的变化是 和
和 反应的热化学方程式为
反应的热化学方程式为(2)已知25℃、101kPa下,1mol水蒸发为水蒸气需要吸热44.01kJ。
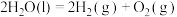
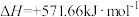

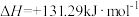
则反应
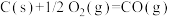 的反应热
的反应热 =
=(3)下表所示是部分化学键的键能参数:
| 化学键 |  |  |  | 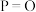 |
| 键能 | a | b | c | x |
已知白磷燃烧反应的
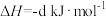 ,白磷及其完全燃烧生成的产物的结构如图乙所示。表中x=
,白磷及其完全燃烧生成的产物的结构如图乙所示。表中x=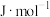 (用含a、b、c、d的代数式表示)。
(用含a、b、c、d的代数式表示)。(4)某学生想通过测定中和反应过程中所放出的热量来计算中和反应的焓变。他将50mL0.5mol/L的盐酸与50mL0.55mol/L的
 溶液在如图所示的装置中进行中和反应。
溶液在如图所示的装置中进行中和反应。
请回答下列问题:
①从实验装置上看,图中有多处错误,其中一处错误是缺少了一种玻璃仪器
②大烧杯上如不盖硬纸板,则求得的中和反应的
 =
=③实验中改用20mL0.50mol/L的盐酸跟20mL0.55mol/L的
 溶液进行反应,与上述实验相比,所放出的热量
溶液进行反应,与上述实验相比,所放出的热量
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】回答下列问题:
(1)已知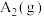 和
和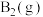 反应生成1mol
反应生成1mol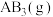 过程中能量变化如图所示。根据下列已知键能数据计算A—B键键能为
过程中能量变化如图所示。根据下列已知键能数据计算A—B键键能为_______ kJ/mol。
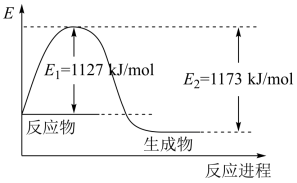
(2)在如图所示的装置中进行中和反应。通过测定反应过程中放出的热量可计算中和反应的反应热。
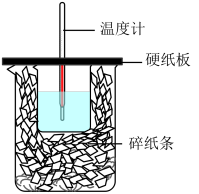
①从实验装置上看,图中缺少的一种玻璃仪器是_______ 。烧杯间填满碎纸条的作用是_______ 。若大烧杯上不盖硬纸板,求得的中和反应反应热
_______ (填“偏大”“偏小”或“无影响”)。
②甲同学用50mL 盐酸与50mL
盐酸与50mL NaOH溶液进行中和反应,通过计算得到
NaOH溶液进行中和反应,通过计算得到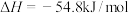 ,该结果与
,该结果与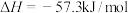 有偏差,产生此偏差的原因可能是
有偏差,产生此偏差的原因可能是_______ (填字母)。
A.用温度计测量盐酸起始温度后直接测量NaOH溶液的温度
B.一次性把NaOH溶液倒入盛有盐酸的小烧杯中
C.实验装置保温、隔热效果差
③若改用60mL 盐酸与60mL
盐酸与60mL NaOH溶液进行反应,与②中实验相比,所放出的热量
NaOH溶液进行反应,与②中实验相比,所放出的热量_______ (填“相等”或“不相等”);若用50mL
 溶液代替盐酸进行②中实验,测得反应前后温度的变化值
溶液代替盐酸进行②中实验,测得反应前后温度的变化值_______ (填“偏大”“偏小”或“不受影响”)。
(1)已知
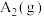 和
和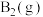 反应生成1mol
反应生成1mol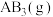 过程中能量变化如图所示。根据下列已知键能数据计算A—B键键能为
过程中能量变化如图所示。根据下列已知键能数据计算A—B键键能为
| 化学键 |  | B—B |
| 键能(kJ/mol) | 946 | 436 |

①从实验装置上看,图中缺少的一种玻璃仪器是

②甲同学用50mL
 盐酸与50mL
盐酸与50mL NaOH溶液进行中和反应,通过计算得到
NaOH溶液进行中和反应,通过计算得到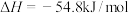 ,该结果与
,该结果与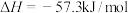 有偏差,产生此偏差的原因可能是
有偏差,产生此偏差的原因可能是A.用温度计测量盐酸起始温度后直接测量NaOH溶液的温度
B.一次性把NaOH溶液倒入盛有盐酸的小烧杯中
C.实验装置保温、隔热效果差
③若改用60mL
 盐酸与60mL
盐酸与60mL NaOH溶液进行反应,与②中实验相比,所放出的热量
NaOH溶液进行反应,与②中实验相比,所放出的热量
 溶液代替盐酸进行②中实验,测得反应前后温度的变化值
溶液代替盐酸进行②中实验,测得反应前后温度的变化值
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】已知:
①C(s)+H2O(g) CO(g)+H2(g) △H=a kJ▪mol-1
CO(g)+H2(g) △H=a kJ▪mol-1
②2C(s)+O2(g)= 2CO(g) △H=-220 kJ▪mol-1
③2CO(g)+O2(g)= 2CO2(g) △H=-566 kJ▪mol-1
化学键的键能参数如下表所示:
回答下列问题:
(1)对于密闭容器中进行的反应①,温度升高,活化能________ (填“增大”“减小”或“不变”)。
(2)CO(g)的燃烧热△H=________ kJ▪mol-1。
(3)反应①中a的值是___________ (填字母代号)。
A.-332 B.-118 C.+350 D.+130
(4)写出表示C(s)燃烧热的热化学方程式:________________________________________ 。
①C(s)+H2O(g)
 CO(g)+H2(g) △H=a kJ▪mol-1
CO(g)+H2(g) △H=a kJ▪mol-1②2C(s)+O2(g)= 2CO(g) △H=-220 kJ▪mol-1
③2CO(g)+O2(g)= 2CO2(g) △H=-566 kJ▪mol-1
化学键的键能参数如下表所示:
| 化学键 | H-H | O-H | O=O |
| 键能/(kJ▪mol-1) | 436 | 462 | 496 |
回答下列问题:
(1)对于密闭容器中进行的反应①,温度升高,活化能
(2)CO(g)的燃烧热△H=
(3)反应①中a的值是
A.-332 B.-118 C.+350 D.+130
(4)写出表示C(s)燃烧热的热化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】已知下列热化学方程式:
①H2(g)+ O2(g)=H2O(
O2(g)=H2O(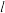 ); △H=﹣285kJ/mol
); △H=﹣285kJ/mol
②H2(g)+ O2(g)=H2O(g); △H=﹣241.8kJ/mol
O2(g)=H2O(g); △H=﹣241.8kJ/mol
③C(s)+ O2(g)=CO(g); △H=﹣110.4kJ/mol
O2(g)=CO(g); △H=﹣110.4kJ/mol
④C(s)+ O2(g)=CO2(g); △H=﹣393.5kJ/mol
回答下列各问:
(1)上述反应中属于放热反应的是_________________________________ ;
(2)C的燃烧热为_________________ kJ/mol;
(3)燃烧10g H2生成液态水,放出的热量为_____________________ kJ;
①H2(g)+
 O2(g)=H2O(
O2(g)=H2O( ); △H=﹣285kJ/mol
); △H=﹣285kJ/mol ②H2(g)+
 O2(g)=H2O(g); △H=﹣241.8kJ/mol
O2(g)=H2O(g); △H=﹣241.8kJ/mol③C(s)+
 O2(g)=CO(g); △H=﹣110.4kJ/mol
O2(g)=CO(g); △H=﹣110.4kJ/mol ④C(s)+ O2(g)=CO2(g); △H=﹣393.5kJ/mol
回答下列各问:
(1)上述反应中属于放热反应的是
(2)C的燃烧热为
(3)燃烧10g H2生成液态水,放出的热量为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】(1)在25℃、101kPa下,1gCH4燃烧生成CO2和液态水时放热56kJ。CH4的燃烧热ΔH=___ kJ·mol-1,表示甲烷燃烧热的热化学方程式为___ 。
(2)在一定条件下N2与H2反应生成NH3,已知拆开1molH—H键、1molN—H键、1molN≡N键分别需要的能量是436kJ、391kJ、945.7kJ,则N2与H2反应生成NH3的热化学方程式为:___ 。
(3)已知:①2Zn(s)+O2(g)=2ZnO(s) ΔH1=-696.6kJ·mol-1
②Zn(s)+Ag2O(s)=ZnO(s)+2Ag(s) ΔH2=-317.3kJ·mol-1
则4Ag(s)+O2(g)=2Ag2O(s)ΔH=___ 。
(2)在一定条件下N2与H2反应生成NH3,已知拆开1molH—H键、1molN—H键、1molN≡N键分别需要的能量是436kJ、391kJ、945.7kJ,则N2与H2反应生成NH3的热化学方程式为:
(3)已知:①2Zn(s)+O2(g)=2ZnO(s) ΔH1=-696.6kJ·mol-1
②Zn(s)+Ag2O(s)=ZnO(s)+2Ag(s) ΔH2=-317.3kJ·mol-1
则4Ag(s)+O2(g)=2Ag2O(s)ΔH=
您最近一年使用:0次
【推荐1】已知氢气的燃烧热为285 kJ·mol−1,氨气在氧气中燃烧的热化学方程式为:4NH3(g) + 3O2(g)  2N2(g) + 6H2O(l) ΔH = -1526 kJ·mol−1
2N2(g) + 6H2O(l) ΔH = -1526 kJ·mol−1
回答下列问题:
(1)写出表示氢气燃烧热的热化学方程式_______ ,氢气作为未来理想燃料的优点是_______ 。
(2)根据上述信息可知:N2(g) + 3H2(g) 2NH3(g) ΔH =
2NH3(g) ΔH =_______ ,若H-H的键能为436 kJ·mol−1,N-H的键能为400 kJ·mol−1,则N≡N的键能为_______ kJ·mol−1。
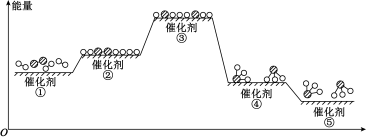
(3)工业上,合成氨反应在催化剂表面的变化如图所示,下列说法错误的是_______(填标号)。
 2N2(g) + 6H2O(l) ΔH = -1526 kJ·mol−1
2N2(g) + 6H2O(l) ΔH = -1526 kJ·mol−1回答下列问题:
(1)写出表示氢气燃烧热的热化学方程式
(2)根据上述信息可知:N2(g) + 3H2(g)
 2NH3(g) ΔH =
2NH3(g) ΔH =(3)工业上,合成氨反应在催化剂表面的变化如图所示,下列说法错误的是_______(填标号)。

| A.①→②表示催化剂的吸附过程,该过程吸收能量 |
| B.②→③→④的过程中有非极性键的断裂和形成 |
| C.合成氨反应正反应的活化能小于逆反应的活化能 |
| D.过程⑤中有化学键的断裂 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】①5.2g的气态乙炔(C2H2)在氧气中燃烧,生成二氧化碳和液态水,放出260kJ的热量,其热化学方程式为:___________________________________________________________ 。又知H2O(l)==H2O(g)△H= +44kJ/mol,则11.2L(标准状况)乙炔完全燃烧生成气态水时放出的热量是_________ kJ。
②已知:CH4 的燃烧热为890 kJ/mol,H2的热值为142.5kJ•g-1,现有标准状况下22.4 L CH4和H2的混合气体完全燃烧时,放出的热量为527kJ,求混合气体中CH4 和H2的体积比_____________
③将1mol NO2投入到1L容器中进行 2NO2(g) N2O4(g)反应,达到平衡后将体积压缩到原来的一半再次达到平衡,则第一次平衡体系的颜色比第二次平衡的颜色
N2O4(g)反应,达到平衡后将体积压缩到原来的一半再次达到平衡,则第一次平衡体系的颜色比第二次平衡的颜色_____________
②已知:CH4 的燃烧热为890 kJ/mol,H2的热值为142.5kJ•g-1,现有标准状况下22.4 L CH4和H2的混合气体完全燃烧时,放出的热量为527kJ,求混合气体中CH4 和H2的体积比
③将1mol NO2投入到1L容器中进行 2NO2(g)
 N2O4(g)反应,达到平衡后将体积压缩到原来的一半再次达到平衡,则第一次平衡体系的颜色比第二次平衡的颜色
N2O4(g)反应,达到平衡后将体积压缩到原来的一半再次达到平衡,则第一次平衡体系的颜色比第二次平衡的颜色
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】回答下列问题:
(1)处理含CO、SO2烟道气污染的一种方法是将其在催化剂作用下转化为单质硫和二氧化碳。已知:①CO(g)+
 O2(g)=CO2(g) ΔH=-283.0kJ·mol-1;②S(s)+O2(g)=SO2(g) ΔH=-296.0kJ·mol-1。该转化反应的热化学方程式为
O2(g)=CO2(g) ΔH=-283.0kJ·mol-1;②S(s)+O2(g)=SO2(g) ΔH=-296.0kJ·mol-1。该转化反应的热化学方程式为(2)氮氧化物是造成光化学烟雾的主要气体。已知:
CO(g)+NO2(g)=NO(g)+CO2(g) ΔH=-akJ·mol-1(a>0)
2CO(g)+2NO(g)=N2(g)+2CO2(g) ΔH=-bkJ·mol-1(b>0)
若用3.36L(标准状况下)CO将NO2还原为N2(CO完全反应),整个反应过程中转移电子的物质的量为
(3)用CH4催化还原NOx也可以消除氮氧化物污染。已知:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ΔH1=-574kJ·mol-1①
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ΔH2②
若1molCH4将NO2还原为N2,整个过程中放出的热量为867kJ,则ΔH2=
(4)某氮肥厂含氮废水中的氮元素多以NH
 和NH3·H2O形式存在,处理过程中NH
和NH3·H2O形式存在,处理过程中NH 在微生物的作用下经过两步反应被氧化为NO
在微生物的作用下经过两步反应被氧化为NO 。这两步反应过程中的能量变化如图所示:
。这两步反应过程中的能量变化如图所示:
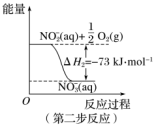
1molNH (aq)全部被氧化成NO
(aq)全部被氧化成NO (aq)的热化学方程式是
(aq)的热化学方程式是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子被称为活化分子,使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ/mol“表示。观察下图,回答问题:
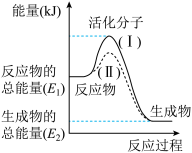
(1)图中所示反应是_______________ (填“吸热”或“放热”)反应。
(2)已知拆开1molH-H键、1molI-I、1molH-I键分别需要吸收的能量为436kJ、151kJ、299kJ,则由1mol氢气和1mol碘反应生成HI会______ (填“放出”或“吸收”)_____ kJ的热量。在化学反应过程中,将_____ 能转化为____ 能。
(3)下列反应中,属于放热反应的是_____________ ,属于吸热反应的是______________ 。
①物质燃烧;②炸药爆炸;③稀释浓硫酸;④二氧化碳通过炽热的碳⑤食物因氧化而腐败;⑥Ba(OH)2·8H2O与NH4Cl反应;⑦铁粉与稀盐酸反应

(1)图中所示反应是
(2)已知拆开1molH-H键、1molI-I、1molH-I键分别需要吸收的能量为436kJ、151kJ、299kJ,则由1mol氢气和1mol碘反应生成HI会
(3)下列反应中,属于放热反应的是
①物质燃烧;②炸药爆炸;③稀释浓硫酸;④二氧化碳通过炽热的碳⑤食物因氧化而腐败;⑥Ba(OH)2·8H2O与NH4Cl反应;⑦铁粉与稀盐酸反应
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】能源是人类生活和社会发展的基础,研究化学反应中的能量变化,有助于更好地利用化学反应为生产和生活服务,回答有关问题:
(1)在一定条件下,2H2O==2H2↑+O2↑,下图能正确表示该反应中能量变化的是________ (用A、B表示)。

从断键和成键的角度分析上述反应中能量的变化。化学键的键能如下表:则生成1mol水热量变化为________ kJ。
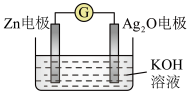
(2)在生产和生活中经常遇到化学能与电能的相互转化,银锌电池是一种常见化学电源,其反应原理:Zn+Ag2O+H2O=Zn(OH)2+2Ag,其工作示意如图所示。在装置中Ag2O作_______ 极(填正或负)溶液中的K+向_____ 电极移动(填“Zn”或“Ag2O”);Ag2O电极发生______ (还原或氧化反应),电极反应式为_____________________ 。
(3)一定温度下,将3molA气体和1molB气体通入一容积固定为1L的密闭容器中,发生如下反应:3A(g)+B(g)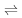 xC(g),反应1min时测得剩余1.8molA,C的浓度为0.4mol/L,则1min内,B的平均反应速率为
xC(g),反应1min时测得剩余1.8molA,C的浓度为0.4mol/L,则1min内,B的平均反应速率为_______ ;x为_________ ;此时反应物B的转化率为_________ 。若反应经2min达到平衡,平衡时C的浓度_____ 0.8mol/L(填“大于,小于或等于”)。
(1)在一定条件下,2H2O==2H2↑+O2↑,下图能正确表示该反应中能量变化的是

从断键和成键的角度分析上述反应中能量的变化。化学键的键能如下表:则生成1mol水热量变化为
| 化学键 | H—H | O=O | H—O |
| 键能kJ/mol | 436 | 496 | 463 |
(2)在生产和生活中经常遇到化学能与电能的相互转化,银锌电池是一种常见化学电源,其反应原理:Zn+Ag2O+H2O=Zn(OH)2+2Ag,其工作示意如图所示。在装置中Ag2O作

(3)一定温度下,将3molA气体和1molB气体通入一容积固定为1L的密闭容器中,发生如下反应:3A(g)+B(g)
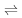 xC(g),反应1min时测得剩余1.8molA,C的浓度为0.4mol/L,则1min内,B的平均反应速率为
xC(g),反应1min时测得剩余1.8molA,C的浓度为0.4mol/L,则1min内,B的平均反应速率为
您最近一年使用:0次
【推荐3】根据要求回答问题:

(1)图1是1 mol NO2(g)和1 mol CO(g)反应生成CO2和NO过程中的能量变化示意图,若在反应体系中加入催化剂,反应速率增大,E1的变化是________ (填“增大”、“减小”或“不变”,下同),ΔH的变化是________ 。
(2)已知CH3OH(l)的燃烧热为726.5kJ·mol-1,CH3OH(l)+ 1/2O2(g)═CO2(g)+2H2(g)△H= -a kJ·mol-1,则a________ 726.5(填“>”、“<”或“=”)。
(3)科学家已获得了极具理论研究意义的N4分子,其结构为正四面体(如图2所示),与白磷分子相似。已知断裂1mol N-N键吸收193 kJ热量,断裂1 mol N≡N键吸收941 kJ热量,则1 mol N4气体转化为2 mol N2时的△H=________ 。
(4)在微生物作用的条件下,NH4+经过两步反应被氧化成NO3-。这两步的能量变化如图:
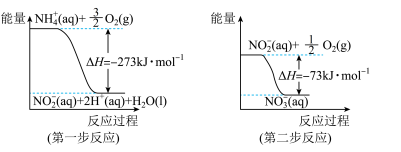
第二步反应是________ 反应(填“放热”或“吸热”)。1 mol NH4+(aq)全部氧化成NO3-(aq)的热化学方程式是_____________ 。

(1)图1是1 mol NO2(g)和1 mol CO(g)反应生成CO2和NO过程中的能量变化示意图,若在反应体系中加入催化剂,反应速率增大,E1的变化是
(2)已知CH3OH(l)的燃烧热为726.5kJ·mol-1,CH3OH(l)+ 1/2O2(g)═CO2(g)+2H2(g)△H= -a kJ·mol-1,则a
(3)科学家已获得了极具理论研究意义的N4分子,其结构为正四面体(如图2所示),与白磷分子相似。已知断裂1mol N-N键吸收193 kJ热量,断裂1 mol N≡N键吸收941 kJ热量,则1 mol N4气体转化为2 mol N2时的△H=
(4)在微生物作用的条件下,NH4+经过两步反应被氧化成NO3-。这两步的能量变化如图:

第二步反应是
您最近一年使用:0次



