根据要求,回答下列问题:
(1)写出离子反应方程式“Ba2+ + SO42- = BaSO4↓”对应的化学反应方程式____________ ;
(2)氧化还原反应“2Na + O2 Na2O2”,氧化产物是
Na2O2”,氧化产物是_______ ;氧化剂是_____ 。
(3)维生素C 又称“抗坏血酸”,在人体内有重要的功能。例如,能帮助人体将食物中摄取的不易吸收的Fe3+转变为易吸收的Fe2+,这说明维生素C 具有___ 。(填氧化性或还原性)
(4)某混合物中可能含有可溶性硫酸盐、碳酸盐及硝酸盐。为了检验其中是否含有硫酸盐,某同学取少量混合物溶于水后,向其中加入_________ 溶液,再加入______ 溶液发现有白色沉淀生成,并由此得出该混合物中含有硫酸盐的结论。
(1)写出离子反应方程式“Ba2+ + SO42- = BaSO4↓”对应的化学反应方程式
(2)氧化还原反应“2Na + O2
 Na2O2”,氧化产物是
Na2O2”,氧化产物是(3)维生素C 又称“抗坏血酸”,在人体内有重要的功能。例如,能帮助人体将食物中摄取的不易吸收的Fe3+转变为易吸收的Fe2+,这说明维生素C 具有
(4)某混合物中可能含有可溶性硫酸盐、碳酸盐及硝酸盐。为了检验其中是否含有硫酸盐,某同学取少量混合物溶于水后,向其中加入
更新时间:2018-01-05 16:56:13
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】弱电解质的电离
(1)写出碳酸氢钠的电离方程式_______ 。
(2)写出氢氧化铝的电离方程式_______ 。
(3)已知硼酸与足量氢氧化钠溶液反应的离子方程式为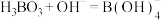 ,则硼酸的电离方程式为
,则硼酸的电离方程式为_______ 。
(4)已知酸性: ,写出下列反应的离子方程式
,写出下列反应的离子方程式
①足量 通入
通入 溶液
溶液_______ 。
②足量 与
与 溶液混合
溶液混合_______ 。
(1)写出碳酸氢钠的电离方程式
(2)写出氢氧化铝的电离方程式
(3)已知硼酸与足量氢氧化钠溶液反应的离子方程式为
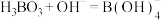 ,则硼酸的电离方程式为
,则硼酸的电离方程式为(4)已知酸性:
 ,写出下列反应的离子方程式
,写出下列反应的离子方程式①足量
 通入
通入 溶液
溶液②足量
 与
与 溶液混合
溶液混合
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】有以下几种物质:A.硝酸钾固体;B.稀盐酸;C.胆矾(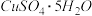 )晶体;D.熔融的
)晶体;D.熔融的 ;E.乙醇;F.氯气;G.干冰;H.铝;I.碳酸氢钠固体;J.硫酸钾溶液,按要求回答下列问题:
;E.乙醇;F.氯气;G.干冰;H.铝;I.碳酸氢钠固体;J.硫酸钾溶液,按要求回答下列问题:
(1)①以上物质中能导电的是_______ (填字母,下同)。
②以上物质中属于电解质的是_______ 。
③以上物质中属于氧化物的是_______ 。
④以上物质中属于混合物的是_______ 。
⑤以上物质中属于有机化合物的是_______ 。
(2)A溶于水的电离方程式为_______ ;
(3)B的水溶液与H反应的离子方程式为_______ 。
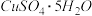 )晶体;D.熔融的
)晶体;D.熔融的 ;E.乙醇;F.氯气;G.干冰;H.铝;I.碳酸氢钠固体;J.硫酸钾溶液,按要求回答下列问题:
;E.乙醇;F.氯气;G.干冰;H.铝;I.碳酸氢钠固体;J.硫酸钾溶液,按要求回答下列问题:(1)①以上物质中能导电的是
②以上物质中属于电解质的是
③以上物质中属于氧化物的是
④以上物质中属于混合物的是
⑤以上物质中属于有机化合物的是
(2)A溶于水的电离方程式为
(3)B的水溶液与H反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】根据所学知识,回答下列问题:
(1)原子是保持物质化学性质的最小微粒。
①第二周期中,第一电离能最大的原子的元素符号是___________ ,电负性最大的原子的元素符号是___________ ;
②前四周期元素中,某元素基态原子 的正三价离子的3d轨道为半充满(即有5个电子),其元素符号为___________ ,其基态原子的价层 电子排布式为___________ ;
③Zn的第一电离能高于Ga的原因是___________ ;
(2)写出下列反应的离子方程式。
①用硫氰化钾溶液检验Fe3+___________ ;
②酸性KMnO4溶液和H2C2O4溶液反应___________ ;
(3)Mg(OH)2浊液中存在Mg(OH)2的沉淀溶解平衡,可表示为______ ,若向此浊液中加入浓的NH4Cl溶液,观察到的现象是_____ 。
(1)原子是保持物质化学性质的最小微粒。
①第二周期中,第一电离能最大的原子的元素符号是
②前四周期元素中,某元素
③Zn的第一电离能高于Ga的原因是
(2)写出下列反应的离子方程式。
①用硫氰化钾溶液检验Fe3+
②酸性KMnO4溶液和H2C2O4溶液反应
(3)Mg(OH)2浊液中存在Mg(OH)2的沉淀溶解平衡,可表示为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】按要求填空:
(1)在S2-、Fe2+、Fe3+、Mg2+、S、I-、H+中,只有氧化性的是________ ,只有还原性的是________ ,既有氧化性又有还原性的是________ 。
(2)某同学写出以下三个化学方程式(未配平)
①NO+HNO3→N2O3+H2O
②NH3+NO→HNO2+H2O
③N2O4+H2O→HNO3+HNO2
其中你认为一定不可能实现的是________ 。
(3)下列三个氧化还原反应中,氧化性最强的物质是______ 。
①2FeCl3+2KI=2FeCl2+2KCl+I2
②2FeCl2+Cl2=2FeCl3
③2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
(1)在S2-、Fe2+、Fe3+、Mg2+、S、I-、H+中,只有氧化性的是
(2)某同学写出以下三个化学方程式(未配平)
①NO+HNO3→N2O3+H2O
②NH3+NO→HNO2+H2O
③N2O4+H2O→HNO3+HNO2
其中你认为一定不可能实现的是
(3)下列三个氧化还原反应中,氧化性最强的物质是
①2FeCl3+2KI=2FeCl2+2KCl+I2
②2FeCl2+Cl2=2FeCl3
③2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
您最近一年使用:0次
【推荐2】
NaNO2因外观和食盐相似,又有咸味,容易使人误食中毒。已知NaNO2能发生反应:2NaNO2+4HI=2NO↑+I2+2NaI+2H2O。
(1)上述反应中氧化剂是________ 。
(2)根据上述反应,鉴别 NaNO2和NaCl。可选用的物质有①水、②碘化钾淀粉试纸、③淀粉、④白酒、⑤食醋,你认为必须选用的物质有________ (填序号)。
(3)请配平以下化学方程式:
____ Al+____ NaNO3+____ NaOH=____ NaAlO2+____ N2↑+___ H2O
(4)若反应过程中转移5 mol 电子,则生成标准状况下N2的体积为_________ L。
NaNO2因外观和食盐相似,又有咸味,容易使人误食中毒。已知NaNO2能发生反应:2NaNO2+4HI=2NO↑+I2+2NaI+2H2O。
(1)上述反应中氧化剂是
(2)根据上述反应,鉴别 NaNO2和NaCl。可选用的物质有①水、②碘化钾淀粉试纸、③淀粉、④白酒、⑤食醋,你认为必须选用的物质有
(3)请配平以下化学方程式:
(4)若反应过程中转移5 mol 电子,则生成标准状况下N2的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】无处不在的氧化还原反应
氧化还原反应是指在反应前后元素的氧化数有相应升降变化的化学反应。其由氧化反应和还原反应构成,并遵守电荷守恒定律。
氧化还原反应是一类非常重要的化学反应,广泛应用于工业、农业、生物、能源等领域。因此,认识氧化还原反应的实质与规律
(1)下表各组变化中,后者一定包括前者的是_____。
(2)下列关于氧化还原反应的叙述中正确的是_____。
(3)下列变化中,必须加入氧化剂才能发生的是_____。
(4)工业上制备84消毒液的一个重要反应为:Cl2+2NaOH═NaCl+NaClO+H2O。在此方程式中。氧化剂是_____ ,具有_____ 性:还原剂是_____ ,氧化产物是_____ 。
用单线桥法在下列给出的反应物中标出电子转移方向和数目。
Cl2+2NaOH_____
氧化还原反应是指在反应前后元素的氧化数有相应升降变化的化学反应。其由氧化反应和还原反应构成,并遵守电荷守恒定律。
氧化还原反应是一类非常重要的化学反应,广泛应用于工业、农业、生物、能源等领域。因此,认识氧化还原反应的实质与规律
(1)下表各组变化中,后者一定包括前者的是_____。
| A.氧化还原反应;分解反应 |
| B.置换反应;氧化还原反应 |
| C.氧化还原反应;化合反应 |
| D.分解反应;中和反应 |
(2)下列关于氧化还原反应的叙述中正确的是_____。
| A.失去电子的反应为还原反应 |
| B.含有氧元素的物质一定是氧化剂 |
| C.氧化剂得电子数目和还原剂失电子数目一定相等 |
| D.氧化剂和还原剂不可能是同一种物质 |
(3)下列变化中,必须加入氧化剂才能发生的是_____。
| A.SO2﹣S | B.I-﹣I2 | C.SO3﹣SO2 | D. |
(4)工业上制备84消毒液的一个重要反应为:Cl2+2NaOH═NaCl+NaClO+H2O。在此方程式中。氧化剂是
用单线桥法在下列给出的反应物中标出电子转移方向和数目。
Cl2+2NaOH
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】磷化氢(PH3)是粮食储备常用的高效熏蒸杀虫剂。
(1)A1P遇水发生复分解反应生成PH3气体和_________ (填化学式)。
(2)PH3具有强还原性,能与CuSO4溶液反应,配平该反应的化学方程式:______________ 。
□CuSO4+□PH3+□H2O = □Cu3P↓+□H3PO4+□H2SO4
(3)工业制备PH3的原理如图所示:

①白磷和烧碱溶液反应的化学方程式为_________ 。
②从分类来看,NaH2PO2属于_________ 。
A.正盐 B.酸式盐 C.强电解质 D.弱电解质
③NaH2PO2可将溶液中的Ag+还原为银,从而用于化学镀银。已知利用此原理进行化学镀银时氧化剂与还原剂的物质的量之比为4∶1,则氧化产物为_________ (填化学式)。
(1)A1P遇水发生复分解反应生成PH3气体和
(2)PH3具有强还原性,能与CuSO4溶液反应,配平该反应的化学方程式:
□CuSO4+□PH3+□H2O = □Cu3P↓+□H3PO4+□H2SO4
(3)工业制备PH3的原理如图所示:

①白磷和烧碱溶液反应的化学方程式为
②从分类来看,NaH2PO2属于
A.正盐 B.酸式盐 C.强电解质 D.弱电解质
③NaH2PO2可将溶液中的Ag+还原为银,从而用于化学镀银。已知利用此原理进行化学镀银时氧化剂与还原剂的物质的量之比为4∶1,则氧化产物为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】草木灰中含有钾盐(主要成分是 、
、 、KCl)。某同学设计实验提取草木灰中的钾盐。
、KCl)。某同学设计实验提取草木灰中的钾盐。
实验步骤:I.取适量的草木灰,加水搅拌,溶解,过滤,取滤液;
Ⅱ.经过蒸发结晶,得到白色固体。
(1)实验步骤I和II中均需要用到的玻璃仪器为___________ 。
(2)为检验草木灰中的离子,某实验小组设计了四组实验,其装置如图所示:
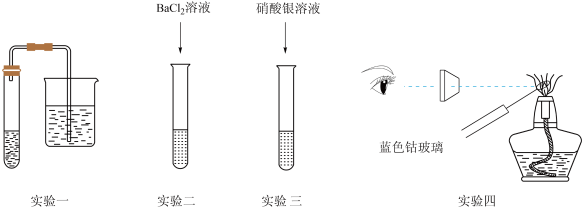
①实验一:往试管中先加入实验步骤I中的滤液,再加入稀盐酸,烧杯中加入澄清石灰水,可观察到___________ ,说明草木灰中含有 。
。
②实验二:取少量实验步骤I中的滤液,先加入稀盐酸酸化,无明显变化,再加入 溶液,有白色沉淀生成。得出的结论是
溶液,有白色沉淀生成。得出的结论是___________ 。
③实验三:取少量实验步骤I中的滤液,加入过量的 溶液后过滤,往滤液中滴加硝酸银溶液,有白色沉淀生成。根据实验现象,该小组同学得出结论:草木灰中含有
溶液后过滤,往滤液中滴加硝酸银溶液,有白色沉淀生成。根据实验现象,该小组同学得出结论:草木灰中含有 。你认为是否正确;
。你认为是否正确;___________ (填“是”或“否”);理由是___________ 。
④实验四:用洁净的铂丝蘸取实验步骤I中的滤液,___________ ,可确定原溶液中含有K+。
 、
、 、KCl)。某同学设计实验提取草木灰中的钾盐。
、KCl)。某同学设计实验提取草木灰中的钾盐。实验步骤:I.取适量的草木灰,加水搅拌,溶解,过滤,取滤液;
Ⅱ.经过蒸发结晶,得到白色固体。
(1)实验步骤I和II中均需要用到的玻璃仪器为
(2)为检验草木灰中的离子,某实验小组设计了四组实验,其装置如图所示:

①实验一:往试管中先加入实验步骤I中的滤液,再加入稀盐酸,烧杯中加入澄清石灰水,可观察到
 。
。②实验二:取少量实验步骤I中的滤液,先加入稀盐酸酸化,无明显变化,再加入
 溶液,有白色沉淀生成。得出的结论是
溶液,有白色沉淀生成。得出的结论是③实验三:取少量实验步骤I中的滤液,加入过量的
 溶液后过滤,往滤液中滴加硝酸银溶液,有白色沉淀生成。根据实验现象,该小组同学得出结论:草木灰中含有
溶液后过滤,往滤液中滴加硝酸银溶液,有白色沉淀生成。根据实验现象,该小组同学得出结论:草木灰中含有 。你认为是否正确;
。你认为是否正确;④实验四:用洁净的铂丝蘸取实验步骤I中的滤液,
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】黑火药爆炸时发生的反应:S+2KNO3+3C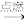 K2S+3CO2↑+N2↑
K2S+3CO2↑+N2↑
(1)上述反应涉及的元素中,非金属性最强的是___________ ,S在周期表中的位置是___________ 。
(2)氮元素对应的气态氢化物是___________ ,其水溶液显___________ 性,写出一水合氨的电离方程式___________ 。
(3)硫元素在自然界主要以硫酸盐的形式存在。写出检验SO 的方法:
的方法:___________
(4)氧、硫的非金属性强弱可通过比较这两种元素___________ (选填编号)
a.原子的得电子的能力b.含氧酸的酸性c.气态氢化物的酸性d.单质的熔沸点
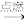 K2S+3CO2↑+N2↑
K2S+3CO2↑+N2↑(1)上述反应涉及的元素中,非金属性最强的是
(2)氮元素对应的气态氢化物是
(3)硫元素在自然界主要以硫酸盐的形式存在。写出检验SO
 的方法:
的方法:(4)氧、硫的非金属性强弱可通过比较这两种元素
a.原子的得电子的能力b.含氧酸的酸性c.气态氢化物的酸性d.单质的熔沸点
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】某溶液中可能含有下列6种离子中的某几种:Cl−、SO 、NH
、NH 、CO
、CO 、K+、Na+。为确认溶液组成进行如下实验:
、K+、Na+。为确认溶液组成进行如下实验:
①200 mL上述溶液,加入足量BaCl2溶液,反应后将沉淀过滤、洗涤、干燥,得沉淀4.30 g,向沉淀中加入过量的盐酸,有2.33 g沉淀不溶。
②向①的滤液中加入足量的NaOH溶液,加热,产生能促使湿润红色石蕊试纸变蓝的气体1.12 L(已换算成标准状况,假定产生的气体全部逸出)。
(1)溶液一定存在的离子有____ ,可能存在的离子有______ ;
(2)原溶液中c(CO )为
)为____ ,c(NH )
)____ c(SO ) (填“>、<或=”);
) (填“>、<或=”);
(3)如果上述6种离子都存在,则c(Cl−)__ c(SO ) (填“>、<或=”)。
) (填“>、<或=”)。
 、NH
、NH 、CO
、CO 、K+、Na+。为确认溶液组成进行如下实验:
、K+、Na+。为确认溶液组成进行如下实验:①200 mL上述溶液,加入足量BaCl2溶液,反应后将沉淀过滤、洗涤、干燥,得沉淀4.30 g,向沉淀中加入过量的盐酸,有2.33 g沉淀不溶。
②向①的滤液中加入足量的NaOH溶液,加热,产生能促使湿润红色石蕊试纸变蓝的气体1.12 L(已换算成标准状况,假定产生的气体全部逸出)。
(1)溶液一定存在的离子有
(2)原溶液中c(CO
 )为
)为 )
) ) (填“>、<或=”);
) (填“>、<或=”);(3)如果上述6种离子都存在,则c(Cl−)
 ) (填“>、<或=”)。
) (填“>、<或=”)。
您最近一年使用:0次



