氮氧化物污染日益严重,请分析下列有关NO、NO2等的试题,然后填空。
(1)如图1所示为N2(g)和O2(g)生成NO(g)过程中的能量变化。
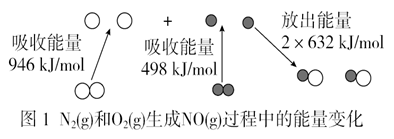
由图1写出N2(g)和O2(g)生成NO(g)的热化学反应方程式:_______________________ 。
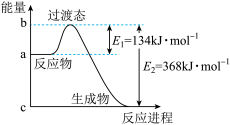
(2)图2所示是1 mol NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:__________________________________________________________ 。

(1)如图1所示为N2(g)和O2(g)生成NO(g)过程中的能量变化。

由图1写出N2(g)和O2(g)生成NO(g)的热化学反应方程式:
(2)图2所示是1 mol NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:

更新时间:2018-01-19 20:55:58
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】回答下列问题。
(1)如图是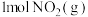 和
和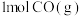 反应生成
反应生成 和
和 过程中的能量变化示意图。请写出
过程中的能量变化示意图。请写出 和
和 反应的热化学方程式
反应的热化学方程式__________ 。
(2)用如图所示装置进行中和热的测定实验。
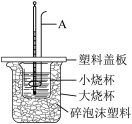
①仪器A的名称是__________ ,碎泡沫塑料的作用是__________ 。
②若实验过程中,未加塑料盖板,则实验测出的
__________ (填“偏大”或“偏小”或“无影响”)。
③理论上强酸强碱的中和热为 ,写出表示稀硫酸和稀
,写出表示稀硫酸和稀 溶液反应的中和热的热化学方程式
溶液反应的中和热的热化学方程式__________ 。
(3)甲醇是人们开发和利用的一种新能源。已知:


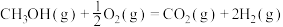
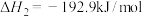
①甲醇蒸气完全燃烧生成二氧化碳气体和液态水的热化学方程式为__________ ;
② 的燃烧热为
的燃烧热为__________ 。
(1)如图是
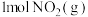 和
和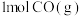 反应生成
反应生成 和
和 过程中的能量变化示意图。请写出
过程中的能量变化示意图。请写出 和
和 反应的热化学方程式
反应的热化学方程式
(2)用如图所示装置进行中和热的测定实验。

①仪器A的名称是
②若实验过程中,未加塑料盖板,则实验测出的

③理论上强酸强碱的中和热为
 ,写出表示稀硫酸和稀
,写出表示稀硫酸和稀 溶液反应的中和热的热化学方程式
溶液反应的中和热的热化学方程式(3)甲醇是人们开发和利用的一种新能源。已知:


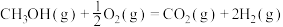
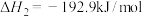
①甲醇蒸气完全燃烧生成二氧化碳气体和液态水的热化学方程式为
②
 的燃烧热为
的燃烧热为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】回答下列问题
(1)有机物M经过太阳光光照可转化成N,转化过程如图:
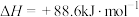 则M、N相比,较稳定的是
则M、N相比,较稳定的是_______ (用“M”或“N”表示),其中1molM与足量的 发生加成反应,最多消耗
发生加成反应,最多消耗
_______ mol
(2) 的燃烧热为
的燃烧热为 ,
,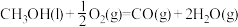
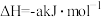 ,则a
,则a_______ 238.6(填“>”、“<”或“=”)。
(3)使 和
和 通过灼热的炭层,生成HCl和
通过灼热的炭层,生成HCl和 ,当有1mol
,当有1mol 参与反应时释放出145kJ热量,写出该反应的热化学方程式:
参与反应时释放出145kJ热量,写出该反应的热化学方程式:_______
(4)火箭和导弹表面的薄层是耐高温物质。将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料,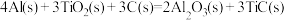
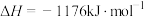 ,则反应过程中,每转移1mol电子放出的热量为
,则反应过程中,每转移1mol电子放出的热量为_______ kJ
(5)盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得,但可通过间接的方法测定。现根据下列3个热化学反应方程式:
①
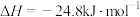
②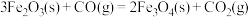
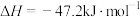
③
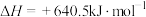
CO还原FeO固体得到Fe固体和 气体的热化学反应方程式为:
气体的热化学反应方程式为:_______
(1)有机物M经过太阳光光照可转化成N,转化过程如图:

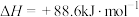 则M、N相比,较稳定的是
则M、N相比,较稳定的是 发生加成反应,最多消耗
发生加成反应,最多消耗
(2)
 的燃烧热为
的燃烧热为 ,
,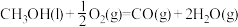
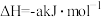 ,则a
,则a(3)使
 和
和 通过灼热的炭层,生成HCl和
通过灼热的炭层,生成HCl和 ,当有1mol
,当有1mol 参与反应时释放出145kJ热量,写出该反应的热化学方程式:
参与反应时释放出145kJ热量,写出该反应的热化学方程式:(4)火箭和导弹表面的薄层是耐高温物质。将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料,
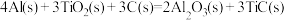
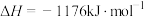 ,则反应过程中,每转移1mol电子放出的热量为
,则反应过程中,每转移1mol电子放出的热量为(5)盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得,但可通过间接的方法测定。现根据下列3个热化学反应方程式:
①

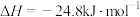
②
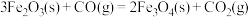
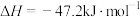
③

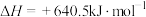
CO还原FeO固体得到Fe固体和
 气体的热化学反应方程式为:
气体的热化学反应方程式为:
您最近一年使用:0次
填空题
|
适中
(0.64)
【推荐3】(1)已知H-H 键能为436 kJ·mol-1,H-N键键能为391 kJ·mol-1,根据化学方程式: N2(g)+3 H2(g) 2NH3(g) ΔH=-92.4kJ·mol-1。则N≡N键的键能是
2NH3(g) ΔH=-92.4kJ·mol-1。则N≡N键的键能是_________________
(2)事实证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的是__________________ 。
A.C(s) + H2O(g) =" CO(g)" + H2(g) △H > 0
B.2H2(g)+O2(g)=2H2O(1) △H < 0
C.NaOH(aq) + HCl(aq) =" NaCl(aq)" + H2O(1) △H < 0
(3)以KOH溶液为电解质溶液,依据所选反应设计一个原电池,其正极的电极反应式___________ 。
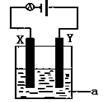
(4)电解原理在化学工业中有着广泛的应用。现将你设计的原电池通过导线与图中电解池相连,其中为 a电解液,X和Y均为惰性电极,则
①若a为CuSO4溶液,则电解时的化学反应方程式为______________ 。
②若电解含有0.04molCuSO4和0.04molNaCl的混合溶液400ml,当阳极产生的气体672mL(标准状况下)时,溶液的pH=_______ (假设电解后溶液体积不变)。
③若用此电解装置模拟工业精炼铜,则应将a改为________ 溶液
 2NH3(g) ΔH=-92.4kJ·mol-1。则N≡N键的键能是
2NH3(g) ΔH=-92.4kJ·mol-1。则N≡N键的键能是(2)事实证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的是
A.C(s) + H2O(g) =" CO(g)" + H2(g) △H > 0
B.2H2(g)+O2(g)=2H2O(1) △H < 0
C.NaOH(aq) + HCl(aq) =" NaCl(aq)" + H2O(1) △H < 0
(3)以KOH溶液为电解质溶液,依据所选反应设计一个原电池,其正极的电极反应式

(4)电解原理在化学工业中有着广泛的应用。现将你设计的原电池通过导线与图中电解池相连,其中为 a电解液,X和Y均为惰性电极,则
①若a为CuSO4溶液,则电解时的化学反应方程式为
②若电解含有0.04molCuSO4和0.04molNaCl的混合溶液400ml,当阳极产生的气体672mL(标准状况下)时,溶液的pH=
③若用此电解装置模拟工业精炼铜,则应将a改为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】在下列事实中,各是什么因素影响了化学反应速率。
(1)集气瓶中H2和Cl2的混合气体,在瓶外点燃镁条时发生爆炸:____ ;
(2)黄铁矿煅烧时要粉碎成矿粒:________ ;
(3)熔化的KClO3放出气泡很慢,撒入少量MnO2则很快产生气体 :____ ;
(4)同样大小的石灰石分别与0.1 mol·L-1盐酸和1 mol·L-1盐酸反应,速率不同:__________ 。
(5)夏天食品容易变质,而冬天不易发生该现象:_______________ 。
(6)从能量的角度看,断开化学键要______ 能量(填吸收或放出,下同),形成化学键要_____ 能量。当反应物的总能量高于生成物时,该反应为_______ 反应(填吸热或放热,下同);当反应物的总能量低于生成物时,该反应为__________ 反应。
(7)由铜、锌和稀硫酸组成的原电池中,正极是_______ (填名称),发生_______ 反应;负极是_______ (填名称),发生________ 反应,总反应的化学方程式是______________________ 。
(1)集气瓶中H2和Cl2的混合气体,在瓶外点燃镁条时发生爆炸:
(2)黄铁矿煅烧时要粉碎成矿粒:
(3)熔化的KClO3放出气泡很慢,撒入少量MnO2则很快产生气体 :
(4)同样大小的石灰石分别与0.1 mol·L-1盐酸和1 mol·L-1盐酸反应,速率不同:
(5)夏天食品容易变质,而冬天不易发生该现象:
(6)从能量的角度看,断开化学键要
(7)由铜、锌和稀硫酸组成的原电池中,正极是
您最近一年使用:0次
【推荐2】工业上用CO生产燃科甲醇,一定条件下发生反应:CO(g)+2H2(g) CH3OH(g), 反应过程中的能量变化情况如图所示。
CH3OH(g), 反应过程中的能量变化情况如图所示。
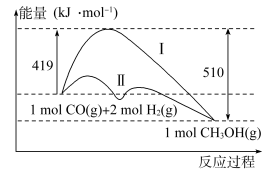
(1)曲线I和曲线II分别表示不使用催化剂和使用催化剂的两种情况。该反应是_______ (填“吸热”或“放热”反应。计算当反应生成1molCH3OH(g)时,能量变化值是_______ kJ。
(2)推测反应CH3OH(g) CO(g)+2H2(g)是
CO(g)+2H2(g)是_______ (填“吸热”或“放热”)反应。
(3)断开1 molH-H键、1molN-H键、1molN≡N键分别需要吸收能量为436kJ、391kJ、946kJ,则1molH2与足量N2反应生成NH3需_______ (填“吸收”或“放出”)能量_______ kJ。(小数点后保留两位数字)。
 CH3OH(g), 反应过程中的能量变化情况如图所示。
CH3OH(g), 反应过程中的能量变化情况如图所示。
(1)曲线I和曲线II分别表示不使用催化剂和使用催化剂的两种情况。该反应是
(2)推测反应CH3OH(g)
 CO(g)+2H2(g)是
CO(g)+2H2(g)是(3)断开1 molH-H键、1molN-H键、1molN≡N键分别需要吸收能量为436kJ、391kJ、946kJ,则1molH2与足量N2反应生成NH3需
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】长征系列部分火箭采用了肼 作燃料,
作燃料, 与
与 有相似的化学性质,试回答下列问题:
有相似的化学性质,试回答下列问题:
(1)已知肼分子中所有原子最外层都满足稀有气体原子结构,则肼的结构式为_______ 。
(2)通常把拆开1mol某化学键吸收的能量看做是该化学键的键能。下表是常见的键能数据
已知合成氨反应
 则a为
则a为_______ (取整数),肼蒸汽在 中燃烧生成
中燃烧生成 与
与 时的热化学方程式为
时的热化学方程式为_______ 。
(3)火箭推进剂通常选择液态的 作氧化剂,混合后会产生大量的气体从而推动火箭升空,试写出该反应的化学方程式
作氧化剂,混合后会产生大量的气体从而推动火箭升空,试写出该反应的化学方程式_______ 。
(4)已知每12.8g的液态肼与足量的液态双氧水反应生成气态产物时放出热量256kJ,已知1mol液态水转化为水蒸气需要吸收44kJ的热量,则1mol的液态肼发生上述反应放出的热量为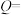
_______ 。
(5)常见的助燃剂有 、
、 、
、 等,若消耗等物质的量的肼,消耗物质的量最多的助燃剂为
等,若消耗等物质的量的肼,消耗物质的量最多的助燃剂为_______ ,实际的火箭选择的助燃剂是 ,主要考虑的因素可能是
,主要考虑的因素可能是_______ 。
 作燃料,
作燃料, 与
与 有相似的化学性质,试回答下列问题:
有相似的化学性质,试回答下列问题:(1)已知肼分子中所有原子最外层都满足稀有气体原子结构,则肼的结构式为
(2)通常把拆开1mol某化学键吸收的能量看做是该化学键的键能。下表是常见的键能数据
| 化学键 |  |  |  |  |  |  |
| 键能(kJ/mol) | 386 | 167 | 498 | 946 | 460 | a |

 则a为
则a为 中燃烧生成
中燃烧生成 与
与 时的热化学方程式为
时的热化学方程式为(3)火箭推进剂通常选择液态的
 作氧化剂,混合后会产生大量的气体从而推动火箭升空,试写出该反应的化学方程式
作氧化剂,混合后会产生大量的气体从而推动火箭升空,试写出该反应的化学方程式(4)已知每12.8g的液态肼与足量的液态双氧水反应生成气态产物时放出热量256kJ,已知1mol液态水转化为水蒸气需要吸收44kJ的热量,则1mol的液态肼发生上述反应放出的热量为
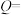
(5)常见的助燃剂有
 、
、 、
、 等,若消耗等物质的量的肼,消耗物质的量最多的助燃剂为
等,若消耗等物质的量的肼,消耗物质的量最多的助燃剂为 ,主要考虑的因素可能是
,主要考虑的因素可能是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】强还原剂液态肼(N2H4)和强氧化剂液态过氧化氢可构成火箭推进剂.当它们混合反应时,即产生大量氮气和水蒸气,并放出大量热.已知:0.4mol液态肼与足量的液态过氧化氢反应生成N2和水蒸气时放出256.0kJ的热量。
(1)该反应的热化学方程式为________________ ;
(2)则16g液态肼与液态过氧化氢反应生成气态水时放出的热量是________________ kJ;
(3)此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是________________ 。
(1)该反应的热化学方程式为
(2)则16g液态肼与液态过氧化氢反应生成气态水时放出的热量是
(3)此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列问题
(1)对烟道气中的 进行回收再利用具有较高的社会价值和经济价值。
进行回收再利用具有较高的社会价值和经济价值。
CO还原法:一定条件下,由 和CO反应生成S和
和CO反应生成S和 的能量变化如图所示,每生成16gS(s),该反应
的能量变化如图所示,每生成16gS(s),该反应_______ (填“放出”或“吸收”)的热量为_______ 。该反应的热化学方程式为_______ 。

(2)汽车尾气中排放的 和
和 污染环境,在汽车尾气系统中装置催化转化器,可有效降低
污染环境,在汽车尾气系统中装置催化转化器,可有效降低 和
和 的排放。已知:
的排放。已知:
①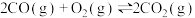

②
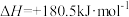
③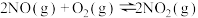
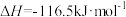
Ⅰ.CO的燃烧热为_______ 。若1mol (g)、1mol
(g)、1mol (g)分子中化学键断裂时分别需要吸收946kJ、498kJ的能量,则1mol NO(g)分子中化学键断裂时需吸收的能量为
(g)分子中化学键断裂时分别需要吸收946kJ、498kJ的能量,则1mol NO(g)分子中化学键断裂时需吸收的能量为_______ kJ。
Ⅱ.CO将 还原为单质的热化学方程式为
还原为单质的热化学方程式为_______ 。
(1)对烟道气中的
 进行回收再利用具有较高的社会价值和经济价值。
进行回收再利用具有较高的社会价值和经济价值。CO还原法:一定条件下,由
 和CO反应生成S和
和CO反应生成S和 的能量变化如图所示,每生成16gS(s),该反应
的能量变化如图所示,每生成16gS(s),该反应
(2)汽车尾气中排放的
 和
和 污染环境,在汽车尾气系统中装置催化转化器,可有效降低
污染环境,在汽车尾气系统中装置催化转化器,可有效降低 和
和 的排放。已知:
的排放。已知:①
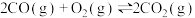

②

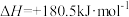
③
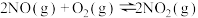
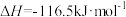
Ⅰ.CO的燃烧热为
 (g)、1mol
(g)、1mol (g)分子中化学键断裂时分别需要吸收946kJ、498kJ的能量,则1mol NO(g)分子中化学键断裂时需吸收的能量为
(g)分子中化学键断裂时分别需要吸收946kJ、498kJ的能量,则1mol NO(g)分子中化学键断裂时需吸收的能量为Ⅱ.CO将
 还原为单质的热化学方程式为
还原为单质的热化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】I.写出下列反应的热化学方程式。
(1)CuCl(s)与O2反应生成CuCl2(s)和一种黑色固体。在25 ℃、101 kPa下,已知该反应每消耗1 mol CuCl(s),放热44.4 kJ,该反应的热化学方程式是___________ 。
(2)在1.01×105 Pa时,16 g S固体在足量的氧气中充分燃烧生成二氧化硫,放出148.5 kJ的热量,则S固体燃烧热的热化学方程式为_____________ 。 (S相对原子质量为32)
II.研究NOx、SO2、CO等大气污染气体的处理具有重要意义。
(3)处理含CO、SO2烟道气污染的一种方法是将其在催化剂作用下转化为单质S固体。已知:
①CO(g)+ O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1
O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1
②S(s)+O2(g)=SO2(g) ΔH=-296.0 kJ·mol-1
此反应的热化学方程式是___________ 。
(1)CuCl(s)与O2反应生成CuCl2(s)和一种黑色固体。在25 ℃、101 kPa下,已知该反应每消耗1 mol CuCl(s),放热44.4 kJ,该反应的热化学方程式是
(2)在1.01×105 Pa时,16 g S固体在足量的氧气中充分燃烧生成二氧化硫,放出148.5 kJ的热量,则S固体燃烧热的热化学方程式为
II.研究NOx、SO2、CO等大气污染气体的处理具有重要意义。
(3)处理含CO、SO2烟道气污染的一种方法是将其在催化剂作用下转化为单质S固体。已知:
①CO(g)+
 O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1
O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1②S(s)+O2(g)=SO2(g) ΔH=-296.0 kJ·mol-1
此反应的热化学方程式是
您最近一年使用:0次



