某校课外小组的同学设计实验用甲烷还原二氧化硫制取单质硫。
(1)甲组同学分别利用如图所示装置制取SO2 和CH4。
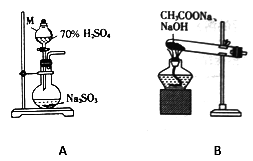
①仪器M的名称为______________ 。
②用A装置制备SO2,不宜使用稀硫酸,其原因是_________________ 。
③用B装置制取甲烷的化学方程式为CH3COONa+NaOH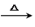 CH4↑+Na2CO3,实际实验中常用碱石灰(NaOH 和CaO的混合物)来代替NaOH,原因是
CH4↑+Na2CO3,实际实验中常用碱石灰(NaOH 和CaO的混合物)来代替NaOH,原因是____________________________________ 。
(2)乙组同学利用甲组制得的CH4和SO2进行实验,并验证产物中除单质硫外还含有CO2。为进行验证,选用甲组实验中的装置A、B和下图所示的装置进行实验,发现G中有淡黄色固体生成,C中澄清石灰水变浑浊。
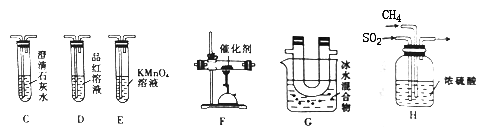
①乙组同学的实验装置中,依次连接的合理顺序为A、B→H→_____ → → → → 。
②E装置的作用是________________ ,G装置的作用是_______________ 。
③F装置中发生反应的化学方程式为____________________ 。
(1)甲组同学分别利用如图所示装置制取SO2 和CH4。

①仪器M的名称为
②用A装置制备SO2,不宜使用稀硫酸,其原因是
③用B装置制取甲烷的化学方程式为CH3COONa+NaOH
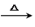 CH4↑+Na2CO3,实际实验中常用碱石灰(NaOH 和CaO的混合物)来代替NaOH,原因是
CH4↑+Na2CO3,实际实验中常用碱石灰(NaOH 和CaO的混合物)来代替NaOH,原因是(2)乙组同学利用甲组制得的CH4和SO2进行实验,并验证产物中除单质硫外还含有CO2。为进行验证,选用甲组实验中的装置A、B和下图所示的装置进行实验,发现G中有淡黄色固体生成,C中澄清石灰水变浑浊。

①乙组同学的实验装置中,依次连接的合理顺序为A、B→H→
②E装置的作用是
③F装置中发生反应的化学方程式为
更新时间:2018-01-31 16:29:40
|
相似题推荐
解答题-实验探究题
|
较难
(0.4)
【推荐1】FeCl3 为中学化学中经常使用的物质,长郡化学实验小组为探究 FeCl3 的性质,进行了如下实验。
(1)学习小组 A 为探究 FeCl3与 KI 溶液的反应,特设计如右图所示的原电池实 验装置。在实验过程中,学习小组 A 发现,灵敏电流计的指针先偏转,最后 示数为零。若此时向甲中加入适量 FeCl2 固体,灵敏电流计的指针又发生偏转 此时________ (填“甲”或“乙”)中石墨电极为负极,对应的电极反应方程式为_________
(2)学习小组 B 把 FeCl3 溶液分别加入Na2CO3 溶液和Na2SO3溶液中,发现有如下实验现象:
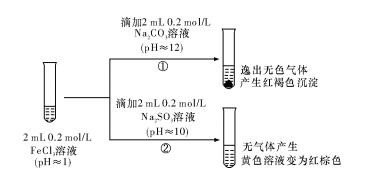

对于②中的实验现象,学习小组 B 的同学们有诸多猜测,继续进行实验: I.小明取②中的红棕色溶液少许,滴入盐酸酸化的 BaCl2溶液,产生白色沉淀。小明得出结论:FeCl3 与 Na2SO3 发生了氧化还原反应,离子方程式是_____ 。
Ⅱ,小红认为小明的实验不严谨,重新设计实验方案并进行实验,证实了小明的结论是正确的。其实验方 案是______________________________ 。
(3)学习小组 C 进一步探究 FeCl3 溶液与足量锌粉的反应。实验操作及实验现象如下表所示:
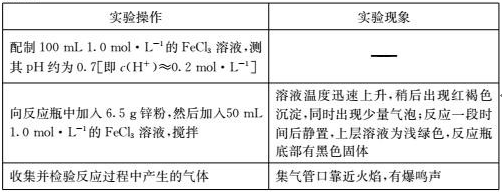
已知:Zn 的化学性质与 Al 相似,能发生反应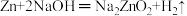
①结合实验现象和平衡移动原理解释出现红褐色沉淀的原因:______
②分离出黑色固体,经下列实验证实了其中含有的主要物质。
i.黑色固体可以被磁铁吸引
ii.向黑色固体中加入足量的 NaOH 溶液,产生气泡;
iii.将 ii 中剩余固体用蒸馏水洗涤后,加入稀盐酸,产生大量气泡; iv.向 iii 反应后的溶液中滴加 KSCN 溶液,无变化。 a.黑色固体中一定含有的物质是_____ 。
b.学习小组 C 认为上述实验无法确定黑色固体中是否含有 Fe3O4,理由是__________________
(4)为进一步探究 1.0 mol/L FeCl3 溶液中 Fe3+和 H+氧化性的相对强弱,学习小组 C 补充实验并观察到反应开始时的实验现象如下表所示:
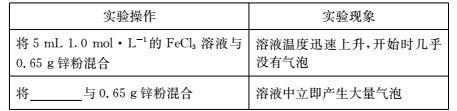
学习小组 C 得出结论:在 1.0 mol/L FeCl3 溶液中,Fe3+的氧化性比 H+强。则表格中横杠处应填____________
(1)学习小组 A 为探究 FeCl3与 KI 溶液的反应,特设计如右图所示的原电池实 验装置。在实验过程中,学习小组 A 发现,灵敏电流计的指针先偏转,最后 示数为零。若此时向甲中加入适量 FeCl2 固体,灵敏电流计的指针又发生偏转 此时
(2)学习小组 B 把 FeCl3 溶液分别加入Na2CO3 溶液和Na2SO3溶液中,发现有如下实验现象:


对于②中的实验现象,学习小组 B 的同学们有诸多猜测,继续进行实验: I.小明取②中的红棕色溶液少许,滴入盐酸酸化的 BaCl2溶液,产生白色沉淀。小明得出结论:FeCl3 与 Na2SO3 发生了氧化还原反应,离子方程式是
Ⅱ,小红认为小明的实验不严谨,重新设计实验方案并进行实验,证实了小明的结论是正确的。其实验方 案是
(3)学习小组 C 进一步探究 FeCl3 溶液与足量锌粉的反应。实验操作及实验现象如下表所示:

已知:Zn 的化学性质与 Al 相似,能发生反应
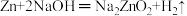
①结合实验现象和平衡移动原理解释出现红褐色沉淀的原因:
②分离出黑色固体,经下列实验证实了其中含有的主要物质。
i.黑色固体可以被磁铁吸引
ii.向黑色固体中加入足量的 NaOH 溶液,产生气泡;
iii.将 ii 中剩余固体用蒸馏水洗涤后,加入稀盐酸,产生大量气泡; iv.向 iii 反应后的溶液中滴加 KSCN 溶液,无变化。 a.黑色固体中一定含有的物质是
b.学习小组 C 认为上述实验无法确定黑色固体中是否含有 Fe3O4,理由是
(4)为进一步探究 1.0 mol/L FeCl3 溶液中 Fe3+和 H+氧化性的相对强弱,学习小组 C 补充实验并观察到反应开始时的实验现象如下表所示:

学习小组 C 得出结论:在 1.0 mol/L FeCl3 溶液中,Fe3+的氧化性比 H+强。则表格中横杠处应填
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐2】某学习小组在实验室制取CO2气体的过程中,不慎用到了浓盐酸,导致制得的CO2气体中混有HCl气体,他们设计了如下除去HCl气体并探究CO2与过氧化钠(Na2O2)反应的实验。请回答下列问题:

(1)装置A的作用是:____________ ;
(2)为确定反应后装置B硬质玻璃管中固体的成分,小组同学取适量固体于试管中,加入足量的蒸馏水溶解形成溶液M,无气泡产生,则该固体中不含____________ (填化学式),该小组同学继续进行探究。
【提出问题】反应后硬质玻璃管中固体的成分是什么?
【做出猜想】
猜想1:Na2CO3
猜想2:NaOH
猜想3:Na2CO3和NaOH,经过讨论,大家一致认为猜想2不合理,理由是:____________ (用化学方程式表示)。
【实验验证】小组同学取上述形成的溶液M于试管中,向其中加入过量____________ (填化学式)溶液,若产生白色沉淀,过滤,向滤液中滴加几滴酚酞试液,溶液变红,则证明猜想3成立。
【交流反思】小组中有同学认为,将上述滤液中滴加的酚酞试液换成硝酸铜溶液,也能得出同样的结论,你认为该同学的观点____________ (填“正确”或“错误”),理由是:____________ (用化学方程式表示)。
【拓展延伸】在盛有氯化铵(NH4Cl)浓溶液的试管中,加入足量的过氧化钠(Na2O2)固体,有气泡产生,产生的气体是:____________ (填化学式)。

(1)装置A的作用是:
(2)为确定反应后装置B硬质玻璃管中固体的成分,小组同学取适量固体于试管中,加入足量的蒸馏水溶解形成溶液M,无气泡产生,则该固体中不含
【提出问题】反应后硬质玻璃管中固体的成分是什么?
【做出猜想】
猜想1:Na2CO3
猜想2:NaOH
猜想3:Na2CO3和NaOH,经过讨论,大家一致认为猜想2不合理,理由是:
【实验验证】小组同学取上述形成的溶液M于试管中,向其中加入过量
【交流反思】小组中有同学认为,将上述滤液中滴加的酚酞试液换成硝酸铜溶液,也能得出同样的结论,你认为该同学的观点
【拓展延伸】在盛有氯化铵(NH4Cl)浓溶液的试管中,加入足量的过氧化钠(Na2O2)固体,有气泡产生,产生的气体是:
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐3】某小组通过实验探究NO的某些性质。
(1)从氮元素的价态角度分析,NO有___________ 性。
(2)设计实验探究NO的氧化性。
实验Ⅰ:用排水法收集一瓶NO,将其倒扣在盛有碱性 溶液的水槽中,振荡,观察到集气瓶中液面上升。
溶液的水槽中,振荡,观察到集气瓶中液面上升。
资料:ⅰ.NO与碱性 溶液会发生氧化还原反应,NO被还原为
溶液会发生氧化还原反应,NO被还原为 。
。
ⅱ. 与
与 反应生成黄色沉淀。
反应生成黄色沉淀。
①检验 的氧化产物。取少量实验Ⅰ反应后集气瓶中的溶液,
的氧化产物。取少量实验Ⅰ反应后集气瓶中的溶液,___________ (填操作和实验现象)。
②某同学认为,需通过进一步实验验证NO的氧化性,补充以下实验:
实验Ⅱ:取饱和 溶液,加入少量冰醋酸,再滴加5滴0.1mol/L的
溶液,加入少量冰醋酸,再滴加5滴0.1mol/L的 溶液,无明显变化。
溶液,无明显变化。
实验Ⅲ:取少量实验Ⅰ反应后集气瓶中的溶液,加入少量冰醋酸,再滴加5滴0.1mol/L的 溶液,
溶液,___________ (填实验现象)。
上述实验证明NO有氧化性。
实验Ⅱ的目的是___________ 。
③写出NO与碱性 溶液反应的离子方程式
溶液反应的离子方程式___________ 。
实验Ⅳ:用排水法收集两瓶NO,将其分别倒扣在饱和 溶液和加有NaOH的饱和
溶液和加有NaOH的饱和 溶液中,后者集气瓶中液面上升更快。
溶液中,后者集气瓶中液面上升更快。
根据上述实验所得结论:___________ 。
(3)某同学结合所学知识设计处理工业废气中 和NO的实验方案,达到消除污染,保护环境的目的。
和NO的实验方案,达到消除污染,保护环境的目的。
①先用饱和纯碱溶液吸收废气中的 ,反应的化学方程式是
,反应的化学方程式是___________ 。
②再向生成的溶液中加入一定量___________ ,以此溶液来吸收NO气体。
(1)从氮元素的价态角度分析,NO有
(2)设计实验探究NO的氧化性。
实验Ⅰ:用排水法收集一瓶NO,将其倒扣在盛有碱性
 溶液的水槽中,振荡,观察到集气瓶中液面上升。
溶液的水槽中,振荡,观察到集气瓶中液面上升。资料:ⅰ.NO与碱性
 溶液会发生氧化还原反应,NO被还原为
溶液会发生氧化还原反应,NO被还原为 。
。ⅱ.
 与
与 反应生成黄色沉淀。
反应生成黄色沉淀。①检验
 的氧化产物。取少量实验Ⅰ反应后集气瓶中的溶液,
的氧化产物。取少量实验Ⅰ反应后集气瓶中的溶液,②某同学认为,需通过进一步实验验证NO的氧化性,补充以下实验:
实验Ⅱ:取饱和
 溶液,加入少量冰醋酸,再滴加5滴0.1mol/L的
溶液,加入少量冰醋酸,再滴加5滴0.1mol/L的 溶液,无明显变化。
溶液,无明显变化。实验Ⅲ:取少量实验Ⅰ反应后集气瓶中的溶液,加入少量冰醋酸,再滴加5滴0.1mol/L的
 溶液,
溶液,上述实验证明NO有氧化性。
实验Ⅱ的目的是
③写出NO与碱性
 溶液反应的离子方程式
溶液反应的离子方程式实验Ⅳ:用排水法收集两瓶NO,将其分别倒扣在饱和
 溶液和加有NaOH的饱和
溶液和加有NaOH的饱和 溶液中,后者集气瓶中液面上升更快。
溶液中,后者集气瓶中液面上升更快。根据上述实验所得结论:
(3)某同学结合所学知识设计处理工业废气中
 和NO的实验方案,达到消除污染,保护环境的目的。
和NO的实验方案,达到消除污染,保护环境的目的。①先用饱和纯碱溶液吸收废气中的
 ,反应的化学方程式是
,反应的化学方程式是②再向生成的溶液中加入一定量
您最近一年使用:0次



