X、Y、Z、W是元素周期表前四周期中的四种常见元素,其相关信息如下表:
(1)Y位于元素周期表第________ 周期第________ 族,Y和Z的最高价氧化物对应的水化物的酸性较强的是________ (写化学式)。
(2)W的基态原子核外电子排布式是___________________________________ 。
(3)W2Y在空气中煅烧生成W2O的化学方程式是________________________ 。
| 元素 | 相关信息 |
| X | X的基态原子核外3个能级上有电子,且每个能级上的电子数相等 |
| Y | 常温常压下,Y单质是淡黄色固体,常在火山口附近沉积 |
| Z | Z和Y同周期,Z的电负性大于Y |
| W | W的一种核素的质量数为63,中子数为34 |
(1)Y位于元素周期表第
(2)W的基态原子核外电子排布式是
(3)W2Y在空气中煅烧生成W2O的化学方程式是
更新时间:2018-02-10 13:56:58
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】A、B、C、D四种元素原子的核电荷数依次增大,它们的简单离子的电子层数相同且最外层电子数均为8。A元素原子的第二层电子数与第一、第三层电子数之和相等,D元素原子的第一、第二层电子数之和等于电子总数的一半。试回答下列问题。
(1)四种元素的符号依次是A___ ,B___ ,C__ ,D__ ;它们的原子半径由大到小的顺序是___ 。
(2)试写出四种元素的离子结构示意图:A___ ,B___ ,C___ ,D___ 。它们的离子半径由大到小的顺序是___ (用离子符号表示)。
(3)分别写出四种元素的最高价氧化物对应水化物的化学式:__ 。
(4)分别写出A、B两元素的气态氢化物的化学式:__ 。
(1)四种元素的符号依次是A
(2)试写出四种元素的离子结构示意图:A
(3)分别写出四种元素的最高价氧化物对应水化物的化学式:
(4)分别写出A、B两元素的气态氢化物的化学式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】指出下列元素在周期表中的位置:
①Ne:___ 周期______ 族; ②C:____ 周期_______ 族;
③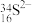 微粒中的质子数是
微粒中的质子数是_______ ,中子数是_______ ,核外电子数是_______ 。
①Ne:
③
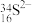 微粒中的质子数是
微粒中的质子数是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】A、D、E、W是中学常见的四种元素,原子序数依次增大,A的原子最外层电子数是次外层的2倍,D的氧化物属于两性氧化物,D、E位于同周期,A、D、E的原子最外层电子数之和为14,W是人体必需的微量元素,缺乏W会导致贫血症状。
(1)A在元素周期表中的位置是____________ 。
(2)下列事实能用元素周期律解释的是(填字母序号)________ 。
a. D的最高价氧化物对应水化物的碱性弱于Mg(OH)2
b. E的气态氢化物的稳定性小于HF
c. WE3的溶液可用于刻蚀铜制的印刷电路板
(3)E的单质可以从NaBr溶液中置换出Br2单质,从原子结构的角度解释其原因是____________ 。
(4)①工业上用电解法制备D的单质,反应的化学方程式为____________ 。
②家用“管道通”的有效成分是烧碱和D的单质,使用时需加入一定量的水,此时发生反应的化学方程式为________ 。
(5)W的单质可用于处理酸性废水中的NO3-,使其转换为NH4+,同时生成有磁性的W的氧化物X,再进行后续处理。上述反应的离子方程式为____________ 。
(1)A在元素周期表中的位置是
(2)下列事实能用元素周期律解释的是(填字母序号)
a. D的最高价氧化物对应水化物的碱性弱于Mg(OH)2
b. E的气态氢化物的稳定性小于HF
c. WE3的溶液可用于刻蚀铜制的印刷电路板
(3)E的单质可以从NaBr溶液中置换出Br2单质,从原子结构的角度解释其原因是
(4)①工业上用电解法制备D的单质,反应的化学方程式为
②家用“管道通”的有效成分是烧碱和D的单质,使用时需加入一定量的水,此时发生反应的化学方程式为
(5)W的单质可用于处理酸性废水中的NO3-,使其转换为NH4+,同时生成有磁性的W的氧化物X,再进行后续处理。上述反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】U、V、W、X、Y、Z是原子序数依次增大的六种常见元素。Y的单质在W2中燃烧的产物可使品红溶液褪色。Z和W元素形成的化合物Z3W4具有磁性。U的单质在W2中燃烧可生成UW和UW2两种气体。X的单质是一种金属,该金属在UW2中剧烈燃烧生成黑、白两种固体。
请回答下列问题:
⑴.V的单质分子的结构式为_______________ ;XW的电子式为____________ ;U元素在周期表中的位置是_____________ 。
⑵.U元素形成的同素异形体的晶体类型可能是(填序号)__________ 。
①原子晶体 ②离子晶体 ③分子晶体 ④金属晶体
⑶.U、V、W形成的10电子氢化物中,U、V、W的氢化物沸点最高的是(写化学式)____________ ;V、W的氢化物分子结合H+能力较强的是(写化学式)______________ ,用一个离子方程式加以证明___________________________________________ 。
请回答下列问题:
⑴.V的单质分子的结构式为
⑵.U元素形成的同素异形体的晶体类型可能是(填序号)
①原子晶体 ②离子晶体 ③分子晶体 ④金属晶体
⑶.U、V、W形成的10电子氢化物中,U、V、W的氢化物沸点最高的是(写化学式)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】A、B、C、D、E五种短周期元素,它们的原子序数依次增大。B原子的最外层电子数是其次外层电子数的2倍。A的一种原子中,质量数与质子数之差为零。D元素原子的最外层电子数为m,次外层电子数为n。E元素原子的L层上电子数为(m+n),M层上电子数为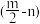 。请回答下列问题:
。请回答下列问题:
(1)B元素是________ ,D元素在周期表中的位置是________ 。
(2)C与E形成的化合物E3C属于________ (填“原子”“离子”或“分子”)晶体。
(3)由A、D、E元素组成的化合物中存在的化学键类型是________ 。
(4)写出一个E和D形成的化合物与水反应的离子方程式:_________________________ 。
(5)已知:甲+H2O→丙+丁,该反应不是氧化还原反应。若甲是由N和Cl元素组成的化合物,其分子结构模型如下图所示,丙具有漂白性。丁与H2O有相同的电子总数,则丁的电子式为_________________ 。

(6)与D同主族且上下相邻的元素M、N,原子电子层数M>N>D,三种元素的氢化物的稳定性由大到小的顺序是________________________ (填化学式)。
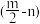 。请回答下列问题:
。请回答下列问题:(1)B元素是
(2)C与E形成的化合物E3C属于
(3)由A、D、E元素组成的化合物中存在的化学键类型是
(4)写出一个E和D形成的化合物与水反应的离子方程式:
(5)已知:甲+H2O→丙+丁,该反应不是氧化还原反应。若甲是由N和Cl元素组成的化合物,其分子结构模型如下图所示,丙具有漂白性。丁与H2O有相同的电子总数,则丁的电子式为

(6)与D同主族且上下相邻的元素M、N,原子电子层数M>N>D,三种元素的氢化物的稳定性由大到小的顺序是
您最近一年使用:0次



