高铁酸钠(Na2FeO4)是一种新型绿色水处理剂。工业上可用电解浓NaOH溶液制备Na2FeO4,其工作原理如右图所示,两端隔室中离子不能进入中间隔室。下列说法错误的是
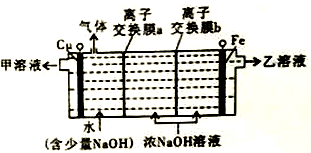

| A.电解时,铜电极连接电源负极 | B.甲溶液可回用于该电解池 |
| C.离子交换膜a是阴离子交换膜 | D.阳极电极反应式:Fe-6e-+8OH-=FeO42-+4H2O |
更新时间:2018/03/06 16:33:21
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】现在污水治理越来越引起人们重视。可以通过膜电池除去废水中的乙酸钠和对氯苯酚( )同时利用此装置的电能在铁上镀铜,下列说法不正确的是
)同时利用此装置的电能在铁上镀铜,下列说法不正确的是

 )同时利用此装置的电能在铁上镀铜,下列说法不正确的是
)同时利用此装置的电能在铁上镀铜,下列说法不正确的是
A.A极的电极反应式为 +e-=Cl-+ +e-=Cl-+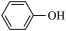 |
| B.当乙中铜电极质量减少6.4g,甲中A极区增加的H+的个数为0.1NA |
| C.膜电池不适合在较高温度环境下工作 |
| D.反应过程中乙中电解质溶液c(Cu2+)不变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】设 为阿伏加德罗常数的值.下列说法正确的是
为阿伏加德罗常数的值.下列说法正确的是
 为阿伏加德罗常数的值.下列说法正确的是
为阿伏加德罗常数的值.下列说法正确的是A.电解精炼铜时,若阴极析出 铜,则阳极失电子数大于 铜,则阳极失电子数大于 |
B. 蔗糖溶液中所含分子数等于 蔗糖溶液中所含分子数等于 |
C.氢氧燃料电池工作时,正极消耗 气体,电路中转移电子数为 气体,电路中转移电子数为 |
D. 时, 时, 的 的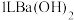 溶液中含有的 溶液中含有的 数目为 数目为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
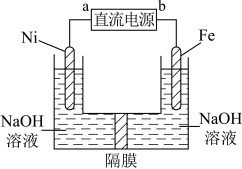
【推荐1】高铁酸盐在能源环保领域有广泛用途。用镍(Ni)、铁作电极电解浓 溶液制备高铁酸盐
溶液制备高铁酸盐 的装置如图所示。下列推断正确的是
的装置如图所示。下列推断正确的是
 溶液制备高铁酸盐
溶液制备高铁酸盐 的装置如图所示。下列推断正确的是
的装置如图所示。下列推断正确的是
| A.a为电源的正极 |
| B.电解一段时间后,撤去隔膜,混合后的溶液与原溶液比较,pH减小 |
C.若电路中通过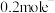 ,则阴极产生气体 ,则阴极产生气体 |
D.铁是阳极,电极反应为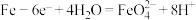 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】如图是工业电解饱和食盐水的装置示意图,下列有关说法中不正确的是( )


| A.装置中出口①处的物质是氯气,出口②处的物质是氢气 |
| B.该离子交换膜只能让阳离子通过,不能让阴离子通过 |
C.装置中发生反应的离子方程式为Cl-+2H+ Cl2↑+H2↑ Cl2↑+H2↑ |
| D.该装置是将电能转化为化学能 |
您最近一年使用:0次
单选题
|
适中
(0.65)
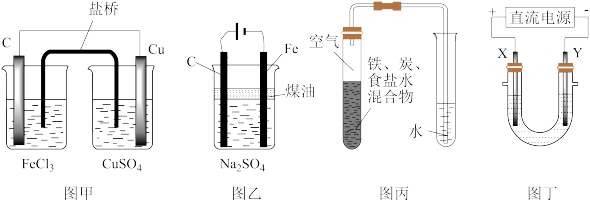
【推荐1】利用如图装置模拟铁的电化学保护。下列说法正确的是
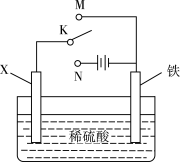

| A.若X为锌棒,开关K置于M处,为外加电流阴极保护法 |
| B.若X为碳棒,开关K置于N处,为牺牲阳极阴极保护法 |
| C.若X为锌棒,开关K置于M处,Zn极发生:Zn-2e→Zn2+ |
| D.若X为碳棒,开关K置于N处,X极发生还原反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】如图所示的电解池I和II中,a、b、c和d均为Pt电极。电解过程中,电极b和d上没有气体逸出,但质量均增大,且增重b<d。符合上述实验结果的盐溶液是
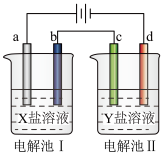

| 选项 | X | Y |
| A. | CuSO4 | AgNO3 |
| B. | AgNO3 | NaCl |
| C. | FeSO4 | Al2(SO4)3 |
| D. | MgSO4 | CuSO4 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】通过电解废旧锂电池中的LiMn2O4可获得难溶性的Li2CO3和MnO2,电解示意图如下(其中滤布的作用是阻挡固体颗粒,但离子可自由通过。电解过程中溶液的体积变化忽略不计)。下列说法不正确 的是
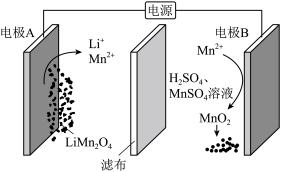
| A.电极A的电极反应式:LiMn2O4+3e-+8H+=Li++2Mn2++4H2O |
| B.电极B附近溶液氢离子浓度增大 |
| C.电解一段时间后溶液中Mn2+浓度保持不变 |
| D.该装置将电能转化为化学能 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】电化学方法制备碘仿的原理及主要原料如图,选择性交换膜只允许Na+通过,已知生成CHI3的反应: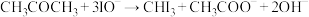 。下列叙述不正确的是
。下列叙述不正确的是
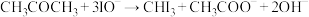 。下列叙述不正确的是
。下列叙述不正确的是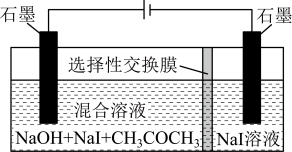
| A.丙酮可溶于水,制备过程中不需要搅拌,丙酮便可与离子充分接触反应 |
B.左室生成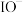 的反应: 的反应: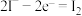 、 、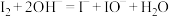 |
C.制备1mL碘仿实际消粍的电量大于理论值,可能的原因是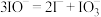 |
| D.电解一段时间后,应定时将右室混合溶液的一部分移至左室 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】下列对应的离子方程式书写或离子共存正确的是
A | 电解 溶液 溶液 | 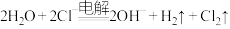 |
B | 向AgCl沉淀中加入过量氨水使AgCl溶解 | 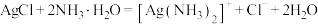 |
C | 由水电离出的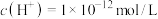 溶液中 溶液中 |  、 、 、 、 、 、 一定能大量共存 一定能大量共存 |
D | 0.1mol/L的 溶液中 溶液中 |  、 、 、 、 、 、 一定能大量共存 一定能大量共存 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次

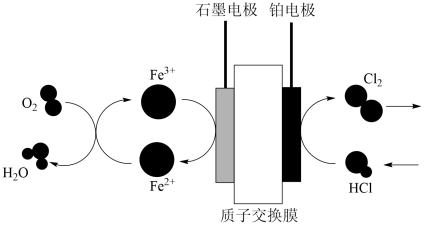
 透过交换膜从铂电极向石墨电极移动
透过交换膜从铂电极向石墨电极移动 ,
,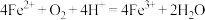

 极上有6.4g
极上有6.4g 析出时,b极产生2.24L(标准状况)气体
析出时,b极产生2.24L(标准状况)气体 溶液的
溶液的 逐渐减小
逐渐减小 溶液换成
溶液换成 溶液,则b极现象和电解的总的离子方程式相同
溶液,则b极现象和电解的总的离子方程式相同

