Ⅰ.某混合物的无色溶液中,可能含有以下离子中的若干种:K+、Ca2+、Fe3+、NH4+、Cl-、CO32-和SO42-。现每次取10.00mL进行实验:
①第一份加入AgNO3溶液有沉淀产生;
②第二份加入足量NaOH后加热,收集到气体448mL(标准状况下);
③第三份加入足量BaCl2溶液后,生成白色沉淀,过滤、干燥,得到固体4.30g,该固体经足量盐酸洗涤,干燥后剩余2.33g。
(1)c(CO32-)=______ mol·L−1;
(2)某同学认为该溶液中一定存在K+,浓度范围是_________________ ;
(3)根据以上实验,某离子可能存在。检验该离子是否存在的方法是___________________________ ;
(4)写出③中固体加入足量盐酸洗涤的离子方程式________________________________ 。
Ⅱ.四种物质有如下相互转化关系:

(5)若化合物A是红棕色粉末状固体,化合物B是一种既可以与强酸溶液反应又可以与强碱溶液反应的氧化物,则该反应的化学方程式为____________________ ;
(6)若甲是活泼金属,化合物B是强碱,则该反应的离子方程式为____________ ;
(7)若乙是黑色固体,化合物B是优质的耐高温材料。则该反应的化学方程式为____________________ ;
(8)若化合物A可作光导纤维材料,乙是一种重要的半导体材料。则该反应的化学方程式为____________________ 。
①第一份加入AgNO3溶液有沉淀产生;
②第二份加入足量NaOH后加热,收集到气体448mL(标准状况下);
③第三份加入足量BaCl2溶液后,生成白色沉淀,过滤、干燥,得到固体4.30g,该固体经足量盐酸洗涤,干燥后剩余2.33g。
(1)c(CO32-)=
(2)某同学认为该溶液中一定存在K+,浓度范围是
(3)根据以上实验,某离子可能存在。检验该离子是否存在的方法是
(4)写出③中固体加入足量盐酸洗涤的离子方程式
Ⅱ.四种物质有如下相互转化关系:

(5)若化合物A是红棕色粉末状固体,化合物B是一种既可以与强酸溶液反应又可以与强碱溶液反应的氧化物,则该反应的化学方程式为
(6)若甲是活泼金属,化合物B是强碱,则该反应的离子方程式为
(7)若乙是黑色固体,化合物B是优质的耐高温材料。则该反应的化学方程式为
(8)若化合物A可作光导纤维材料,乙是一种重要的半导体材料。则该反应的化学方程式为
更新时间:2018/03/10 21:40:47
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】已知某无色透明溶液中可能含有下列离子中的若干种:K+、Mg2+、Fe3+、Ba2+、 、OH-、
、OH-、 和Cl-,现取该溶液进行如下实验:(已知AgOH为白色沉淀)
和Cl-,现取该溶液进行如下实验:(已知AgOH为白色沉淀)
I.取少量原溶液,滴入紫色石蕊试液,溶液呈蓝色;
Ⅱ.取少量原溶液,滴入BaCl2溶液,无明显现象;
Ⅲ.取少量原溶液,先滴加足量稀硝酸,再加入AgNO3溶液,有白色沉淀产生;
Ⅳ.取少量原溶液,滴入少量稀H2SO4,有白色沉淀产生。
(1)某同学提出,不用实验即可判断原溶液中不存在的离子是_____ (填离子符号,下同)。
(2)由Ⅱ可以判断出原溶液中不存在的离子是_____ 。
(3)Ⅲ是为了判断_____ 离子的存在,先滴加足量稀硝酸的目的是_____ 。写出Ⅲ中发生反应的离子方程式_____ 。
(4)原溶液中一定含有的离子是_____ (填离子符号)。
(5)原溶液中可能含有的离子是_____ (填离子符号),为确认该离子的存在,可通过_____ (填实验名称)来检验。
 、OH-、
、OH-、 和Cl-,现取该溶液进行如下实验:(已知AgOH为白色沉淀)
和Cl-,现取该溶液进行如下实验:(已知AgOH为白色沉淀)I.取少量原溶液,滴入紫色石蕊试液,溶液呈蓝色;
Ⅱ.取少量原溶液,滴入BaCl2溶液,无明显现象;
Ⅲ.取少量原溶液,先滴加足量稀硝酸,再加入AgNO3溶液,有白色沉淀产生;
Ⅳ.取少量原溶液,滴入少量稀H2SO4,有白色沉淀产生。
(1)某同学提出,不用实验即可判断原溶液中不存在的离子是
(2)由Ⅱ可以判断出原溶液中不存在的离子是
(3)Ⅲ是为了判断
(4)原溶液中一定含有的离子是
(5)原溶液中可能含有的离子是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】有A、B、C、D、E 五瓶透明溶液,分别是HCl、BaCl2、NaHSO4、Na2CO3和AgNO3中的一种。已知:
①A与过量B反应有气体生成;
②B与C反应有沉淀生成;
③C与D反应有沉淀生成;
④D与E反应有沉淀生成;
⑤A与过量E反应有气体生成;
⑥在②和③的反应中生成的沉淀是同一种物质。
(1)在②和③的反应中,生成的沉淀物质的化学式(分子式)是___________
(2)A是___________ ,B是___________ ,C是___________
(3)D与E反应的离子反应方程式为___________
①A与过量B反应有气体生成;
②B与C反应有沉淀生成;
③C与D反应有沉淀生成;
④D与E反应有沉淀生成;
⑤A与过量E反应有气体生成;
⑥在②和③的反应中生成的沉淀是同一种物质。
(1)在②和③的反应中,生成的沉淀物质的化学式(分子式)是
(2)A是
(3)D与E反应的离子反应方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】某钠盐溶液可能含有阴离子 NO 、CO
、CO 、SO
、SO 、SO
、SO 、Cl-、Br-、I-。为鉴定这些离子,分别取少量溶液进行以下实验:
、Cl-、Br-、I-。为鉴定这些离子,分别取少量溶液进行以下实验:
①测得溶液呈碱性;
②加HCl后,生成无色、无味气体。该气体能使饱和石灰水溶液变浑浊;
③加CCl4,滴加少量氯水,振荡后,CCl4层未变色;
④加BaCl2溶液产生白色沉淀,分离,在沉淀中加入足量盐酸,沉淀不能完全溶解;
⑤加HNO3酸化后,再加过量AgNO3溶液,溶液中析出白色沉淀。
分析上述5个实验,写出每一实验鉴定离子的结论(用“一定有”或“可能有”或“一定没有”来描述,说明理由。)。
(1)实验①_____________________________ ;
(2)实验②______________________________ ;
(3)实验③____________________________ ;
(4)实验④____________________________ ;
(5)实验⑤____________________________ 。
 、CO
、CO 、SO
、SO 、SO
、SO 、Cl-、Br-、I-。为鉴定这些离子,分别取少量溶液进行以下实验:
、Cl-、Br-、I-。为鉴定这些离子,分别取少量溶液进行以下实验:①测得溶液呈碱性;
②加HCl后,生成无色、无味气体。该气体能使饱和石灰水溶液变浑浊;
③加CCl4,滴加少量氯水,振荡后,CCl4层未变色;
④加BaCl2溶液产生白色沉淀,分离,在沉淀中加入足量盐酸,沉淀不能完全溶解;
⑤加HNO3酸化后,再加过量AgNO3溶液,溶液中析出白色沉淀。
分析上述5个实验,写出每一实验鉴定离子的结论(用“一定有”或“可能有”或“一定没有”来描述,说明理由。)。
(1)实验①
(2)实验②
(3)实验③
(4)实验④
(5)实验⑤
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】有A、B、C、D四种化合物,分别由Ba2+、K+、SO42-、OH-、CO32-、SO32-中的两种所组成,它们各具有下列性质:①A既不溶于水,又不溶于盐酸,②B不溶于水,但可溶于盐酸并放出无色无味气体;③C的水溶液呈碱性,与稀硫酸反应生成A④D溶于水,与硫酸作用时放出的气体E可使溴水褪色。
(1)推断A、B、C、D、E各为何种物质,写出它们的化学式。
A:________ ,B:________ ,C:________ ,D:________ ,E:________ 。
(2)写出下列离子方程式:
B与盐酸反应____________________________________________________ ;
C与硫酸反应____________________________________________________ ;
D与硫酸反应____________________________________________________ ;
E与溴水反应____________________________________________________ 。
(1)推断A、B、C、D、E各为何种物质,写出它们的化学式。
A:
(2)写出下列离子方程式:
B与盐酸反应
C与硫酸反应
D与硫酸反应
E与溴水反应
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】下列图示中,A为一种常见的单质,B、C、D、E是含有同一种元素的常见化合物,B为淡黄色固体,B和A都可以与水反应生成C。
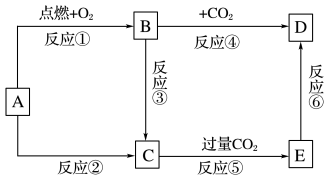
回答下列问题:
(1)写出化学式:B_______ 、C_______ 。
(2)写出基本反应类型:反应①是_______ ,反应⑥是_______ 。
(3)反应⑤的化学方程式为_______ 。
(4)反应④的化学方程式为_______ 。

回答下列问题:
(1)写出化学式:B
(2)写出基本反应类型:反应①是
(3)反应⑤的化学方程式为
(4)反应④的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】已知由短周期常见元素形成的纯净物A、B、C、D转化关系如图1琐事,物质A与物质B之间的反应不再溶液中进行。
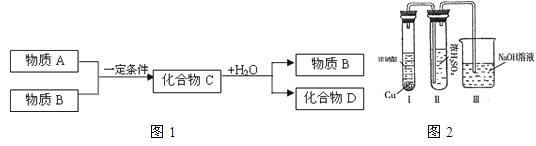
(1) 若A为金属单质,C是淡黄色固体,D是一元强碱。
①物质B是__________ (填化学式)。
②化合物C的电子式为_________ ;化合物D中所含化学键的类型是_________ 。
③在常温下,向PH=a的醋酸溶液中加入等体积pH=b的D溶液,且a+b=14,则充分反应后,所得溶液中各种离子的浓度由大到小的顺序是:__________ .
(2)若A为非金属单质,C是有色气体,D是一元强酸.
①B为__________ (填化学式)。
②化合物C与H2O反应化学方程式___________ ,氧化剂与还原剂的量比为_________ 。
(3)某同学用图2装置完成有关探究实验。
Ⅰ试管中发生反应的离子方程式为__________ 。
Ⅱ试管中观察到__________ 的实验现象时,说明NO2能溶于浓硫酸中,浓硫酸不能干燥NO2。

(1) 若A为金属单质,C是淡黄色固体,D是一元强碱。
①物质B是
②化合物C的电子式为
③在常温下,向PH=a的醋酸溶液中加入等体积pH=b的D溶液,且a+b=14,则充分反应后,所得溶液中各种离子的浓度由大到小的顺序是:
(2)若A为非金属单质,C是有色气体,D是一元强酸.
①B为
②化合物C与H2O反应化学方程式
(3)某同学用图2装置完成有关探究实验。
Ⅰ试管中发生反应的离子方程式为
Ⅱ试管中观察到
您最近一年使用:0次



